
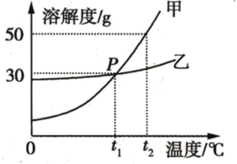
【题目】已知如图为甲、乙两种物质(不含结晶水)的溶解度曲线图,将t1℃时甲、乙的饱和溶液升温至t2℃,则两种溶液的溶质质量分数的关系为甲______(选填“>”“<”或“=”)乙;t2℃时,若甲溶液中溶质与溶剂的质量比为2 : 5,则该溶液为__ (选填“饱和”“不饱和”)溶液;t1℃将130 g乙溶液加水稀释为10%的溶液,需加水的质量为______g。
【答案】= 不饱和 170
【解析】
因为t1℃时甲、乙的溶解度相同,所以甲、乙的饱和溶液的溶质质量分数也相同,将t1℃时甲、乙的饱和溶液升温至t2℃,虽然甲、乙的溶解度都增大了,但溶质和溶剂均无改变,所以两种溶液的溶质质量分数的关系为相等。t2℃时,甲溶液中溶质与溶剂的质量比为2 : 5,根据溶解度概念,将溶质、溶剂质量等比例扩大20倍,则甲溶液中溶质与溶剂的质量比为40 : 100,即向100g水中加入的甲质量为40 g,但此时甲的溶解度为50g,因此该溶液为不饱和溶液。浓溶液加水稀释的过程中,不变的是溶质质量,因此建立等量关系:浓溶液质量×浓溶液溶质质量分数=稀溶液质量×稀溶液溶质质量分数。但此时缺少浓溶液的溶质质量分数,但题中关键词为“饱和溶液”,根据溶液曲线图可知,t1℃时溶液的溶解度为30g,则此时乙的饱和溶液的溶质质量分数为![]() ,设需加水的质量为x,则
,设需加水的质量为x,则![]() ,解得x=170 g。
,解得x=170 g。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】下图是一定条件下某反应的微观模拟示意图,按图分析下列说法错误的是

A.反应前后,原子种类、数目不变
B.该反应中的甲、乙、丙、丁四种物质的分子个数比为2:2:1:2
C.该反应是置换反应
D.反应物和生成物都是由分子构成的
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】上右图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )

A. t2℃时,甲、乙两种物质的溶解度相等
B. 甲的溶解度随温度的升高而增大
C. 分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙
D. t1℃时,丙的饱和溶液中溶质的质量分数为40%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】SO2是造成酸雨的主要气体之一,其水溶液叫亚硫酸(H2SO3)溶液。H2S是一种具有臭鸡蛋气味 的剧毒气体,其水溶液叫氢硫酸溶液。已知相同的条件下,氢硫酸的酸性弱于亚硫酸。室温下,向饱和的亚硫酸溶液中通入过量的硫化氢气体,发生反应如下:![]() 。则下图中溶液的 pH 随通入硫化氢体积的变化曲线示意图正确的是( )
。则下图中溶液的 pH 随通入硫化氢体积的变化曲线示意图正确的是( )
A.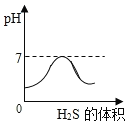
B.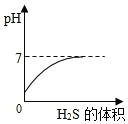
C.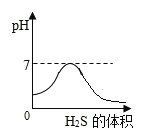
D.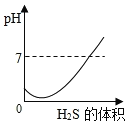
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成。用它制备氢氧化镁的流程示意图如下:

部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀 | 1.9 | 4.2 | 9.1 |
完全沉淀 | 3.2 | 6.7 | 11.1 |
(1)熟石灰主要成分的化学式是____________。
(2)溶液A中的阳离子是___________________(填离子符号)。
(3)沉淀C的成分是_____________________。
(4)溶液B与熟石灰反应的化学方程式是____________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用电解饱和氯化钠溶液的方法来制取氢氧化钠、氯气(![]() )和氢气,并以它们为原料生产一系列化工产品,称为氯碱工业。请用化学用语填空:
)和氢气,并以它们为原料生产一系列化工产品,称为氯碱工业。请用化学用语填空:
(1)构成氯化钠的阴离子____________________。
(2)水中氧元素的化合价为-2价___________________。
(3)电解饱和氯化钠溶液的化学方程式___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】回收利用是保护金属资源的一条有效途径。 某工业废料含氧化铜,氧化铁和不溶于酸的杂质,经过处理后可得到铜和硫酸亚铁溶液[![]() ]
]
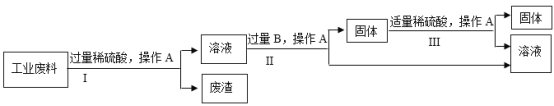
(1)步骤Ⅰ、Ⅱ、III都需进行操作A,操作A的名称为_______________。
(2)步骤Ⅰ中为加快反应速率,可采取的一种措施是_______________。
(3)步骤Ⅱ中除溶液颜色变化外,还可观察到_____________,判断加入B是否过量的方法是_______________。
(4)步骤III中发生反应的化学方程式为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用下列实验来制取CO2并进行相关实验探究。
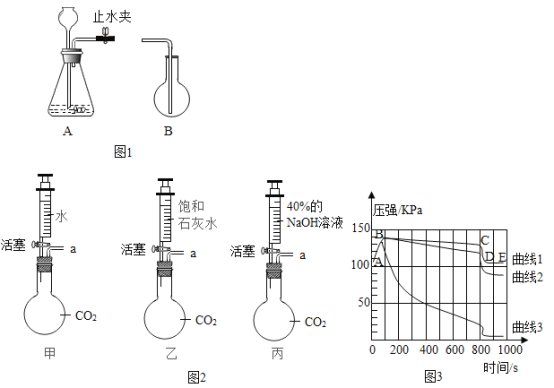
(1)制取CO2。
①简述检查A装置气密性的方法:_____。
②用B装置(烧瓶)收集CO2时,如何证明CO2已经收集满了?_____
(2)探究CO2的性质,实验步骤如下:
步骤1:图2所示装置的气密性良好(图中a处连接气体压力传感器),甲、乙、丙一个烧瓶容积均为250 mL,分别收集满CO2,三个注射器内各装有85mL液体。
步骤2:同时迅速将注射器内液体全部注入烧瓶中,关闭活塞;一段时间后,同时振荡烧瓶。
步骤3:利用“数字化实验”得到如图3所示的甲、乙、丙三个烧瓶内压强与时间的对应关系曲线1、2、3。
①烧瓶乙中有白色沉淀生成,该反应的化学方程式为:_____。
②曲线1中 BC段气压逐渐变小的原因是_____,曲线2与曲线3差别较大的原因是什么?_____。
③对比曲线1与曲线3,不能得出的结论是_____(填序号)。
a.CO2能溶于水 b.CO2能与水发生反应 c.CO2能与 NaOH 溶液发生反应
④请设计实验,证明反应进行到400s时,烧瓶丙的溶液中溶质的成分。
(3)向盛有12g石灰石(杂质不参与反应)样品的锥形瓶中加入100g稀盐酸,充分反应后,测得溶液呈酸性,锥形瓶内固体与溶液的总质量为107.6g,请计算样品中碳酸钙的质量分数(结果精确到0.1%)。_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在氢氧化钠溶液中逐滴滴加稀盐酸。实验过程中溶液温度的变化及实验操作如图一、图二所示:
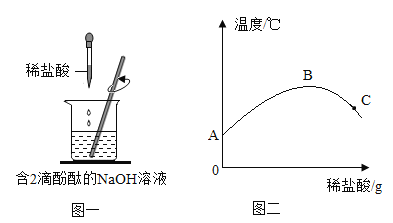
(1)在氢氧化钠溶液中滴加无色酚酞的作用是_____。
(2)根据图二所示:AB段曲线上升的原因是_____;C点时溶液中所含的阳离子有__。
(3)已知氢氧化钠稀溶液的浓度和相应的pH值如下表所示:
①根据下表推断,当溶液的pH值近似为12时,氢氧化钠溶液的溶质质量分数为___。
溶液中氢氧化钠的质量分数 | 近似pH值 |
4% | 14 |
0.4% | 13 |
12 | |
0.004% | 11 |
0.0004% | 10 |
②计算在50g溶质质量分数为4%的氢氧化钠溶液中,加入30g浓度为3.65%的稀盐酸,充分反应后所得溶液中氢氧化钠的质量分数为________,所得溶液的pH范围是_____ (填字母)。
A 10~11 B 11~12 C 12~13 D 13~14
(4)某造纸厂有10 t含NaOH的质量分数为3.2%的废水,现要用溶质质量分数为3.65%盐酸进行处理至中性后排放,需要这种盐酸的多少吨____?(废水中其他物质不与盐酸反应,写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com