
 如图是甲﹑乙两种固体物质的溶解度曲线,下列说法正确的是( )
如图是甲﹑乙两种固体物质的溶解度曲线,下列说法正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 升高温度能使接近饱和的甲溶液变为饱和溶液 | |
| C. | t℃时,甲﹑乙饱和溶液中溶质的质量分数相等 | |
| D. | 10℃时,分别用100 g水配制甲﹑乙的饱和溶液,所需甲的质量大于乙的质量 |
分析 A、某种物质的溶解度的大小由温度来决定.
B、t℃时,甲、乙两条曲线相交于一点,说明此时两种物质的溶解度相同.
C、从图象可以看出.甲物质的溶解度随着温度的升高而增大.
D、根据10℃时,甲、乙两种物质的溶解度大小即可.
解答 解:A、由两种物质的溶解度曲线可以看出,当0~t℃时,乙的溶解度大于甲的溶解度,故错误;
B、由甲物质的溶解度曲线可以看出,甲物质的溶解度随着温度的升高而增大,所以升高温度不能使接近饱和的甲溶液变为饱和溶液,故错误;
C、t℃时,二者的溶解度相等,饱和溶液中溶质的质量分数也相等,故正确;
D、过10℃做一条垂直于温度的虚线,看虚线与曲线的交点高低,从图象可以看出,此时乙的溶解度大于甲的溶解度,故错误.
故选:C.
点评 主要考查了对固体溶解度的概念的理解和固体溶解度曲线的意义,以此培养学生的理解能力、培养学生分析问题、解决问题的能力.


科目:初中化学 来源: 题型:选择题
| A. | 水和过氧化氢化学性质不同--分子构成不同 | |
| B. | 水沸腾后壶盖被顶起--温度升高,分子体积变大 | |
| C. | 50mL水和50mL酒精混合,液体总体积小于100mL--分子之间有间隔 | |
| D. | 春天百花盛开,花香四溢--分子在不断的运动 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
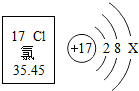
| A. | 氯原子的质子数是 17 | B. | 氯原子核外有 3个电子层 | ||
| C. | 当 X=8时,该微粒是阴离子 | D. | 在化学变化中,氯原子易失电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
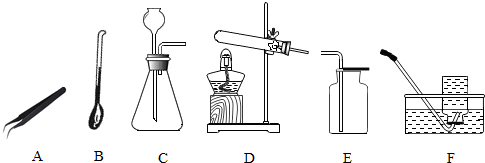
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
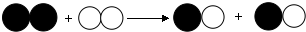
| A. | 该反应生成两种物质 | B. | 化学反应前后原子的种类不变 | ||
| C. | 该反应是复分解反应 | D. | 分子在化学变化中是不可分的 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com