
【题目】同学们在实验室完成实验探究后得到废液 A,其中含有稀硫酸、硫酸亚铁和硫酸铜。老师将同学们分成甲乙两组,继续进行如下实验,请完成相关问题:
(甲组任务)将废液转化成硫酸亚铁晶体。实验流程如图1:
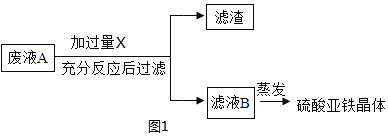
①实验流程中X 是_____(写物质名称),过量的目的是_____,反应现象是_____,写出一个涉及的化学方程式是_____,该反应的基本类型_____。
(乙组任务)利用废液来探究金属铝的化学性质。实验流程如图2:
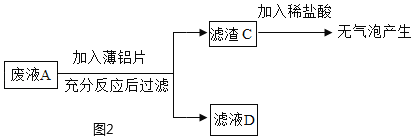
②滤渣 C 中一定没有_____。
③滤液 D 中一定含有的溶质是_____(填化学式,下同),可能含有的溶质是_____。
【答案】铁 将稀硫酸、硫酸铜完全转化为硫酸亚铁 有气泡冒出,固体逐渐转化为红色 Fe+H2SO4=FeSO4+H2↑或Fe+CuSO4=FeSO4+Cu 置换反应 铁和铝 FeSO4和Al2(SO4)3 CuSO4和H2SO4
【解析】
①废液 A中含有稀硫酸、硫酸亚铁和硫酸铜,需要将废液转化成硫酸亚铁晶体,所以实验流程中X 是铁,铁与硫酸反应生成硫酸亚铁和氢气,铁与硫酸铜反应生成硫酸亚铁和铜,过量的目的是将稀硫酸、硫酸铜完全转化为硫酸亚铁,现象为有气泡冒出,固体逐渐转化为红色,化学方程式为Fe+H2SO4=FeSO4+H2↑、Fe+CuSO4=FeSO4+Cu,该反应符合“单质+化合物=新单质+新化合物”属于置换反应;
②滤渣C中加入稀硫酸没有气泡产生,所以滤渣C中一定没有铁和铝;
③铝与硫酸铜反应生成硫酸铝和铜,滤渣C中加入稀硫酸没有气泡产生,所以硫酸亚铁没有与铝反应,由于滤液D中一定含有的溶质是:硫酸铝和硫酸亚铁,可能含有的溶质是:CuSO4和H2SO4;因为铝太少;


科目:初中化学 来源: 题型:
【题目】中国是把香椿当做蔬菜的唯一国家,它不仅营养丰富,而且具有极高的药用价值,如香椿中含有的皂甙,具有抗菌、防癌的作用,皂甙的化学式为C27H42O3,请你计算:
(1)皂甙属于_______________(填“有机物”或“无机物”);
(2)皂甙中各元素的质量之比是____________________(最简整数比);
(3)含氢元素8.4 g的皂甙的质盆为________________克(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲和乙两种物质的溶解度曲线如图所示。下列叙述正确的是( )
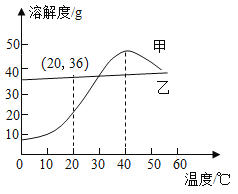
①甲的溶解度随温度的升高而增大
②40℃时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法
③20℃时,向125g溶质质量分数为20%的乙溶液中加入15g乙固体并振荡,有固体不溶解
④将相同质量的甲和乙的饱和溶液分别从40℃降温至10℃,甲析出晶体的质量大
A. ①②B. ③④C. ①③④D. ②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某密闭容器中物质变化过程的微观示意图(已知:●代表氧原子,〇代表硫 原子)请回答:
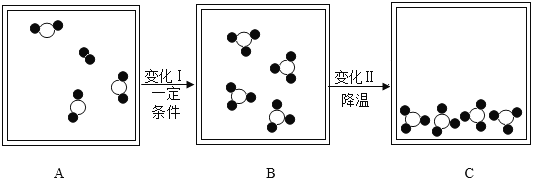
(1)请将A中缺少的分子模型补画完整_______________。
(2)化学反应前后发生改变的微粒是________________(填“分子”或“原子”)。
(3)写出图中反应的化学方程式____________________,此反应属__________________(填基本反应类型)。
(4)A、B、C 中属于混合物的是__________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】室温时几种物质的溶解度如表所示。室温下向 396g 硝酸钾饱和溶液中投入 20g 食盐,下列推断正确的是( )
物质 | S(g/100g 水) |
氯化钠 | 36 |
硝酸钾 | 32 |
硝酸钠 | 86 |
氯化钾 | 37 |
A.食盐不溶解
B.食盐溶解,无晶体析出
C.食盐溶解,溶液中有少量晶体析出
D.食盐溶解,硝酸钾变为不饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组为研究一氧化碳的性质进行了如图所示实验。下列关于该实验叙述正确的是()

A.该实验验证了一氧化碳具有氧化性
B.丙过程中能观察到铜丝从红色变成了黑色
C.装置中石灰水的作用是吸收剩余的一氧化碳
D.待反应结束冷却后软质塑料瓶会变扁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测量某石灰石矿中碳酸钙的含量,进行了如下实验:称取10g石灰石样品,反复灼烧至质量不再改变,称量剩余固体质量为6.7g(反应的化学方程式为:CaCO3![]() CaO+CO2↑,假设杂质不参与反应)请计算:
CaO+CO2↑,假设杂质不参与反应)请计算:
(1)反应生成的CO2的质量为_____g。
(2)该石灰石样品中碳酸钙的质量分数_____(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某纯净物X在空气中完全燃烧,反应的化学方程式为:X+2O2![]() CO2+2H2O,下列关于X的说法正确的是( )
CO2+2H2O,下列关于X的说法正确的是( )
A.X由碳、氢、氧三种元素组成
B.X的相对分子质量为10
C.X中碳、氢元素的质量比为1:4
D.X属于有机化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类历史发展的不同阶段曾以不同金属材料的使用作为标志。

(1)金、银在自然界有单质形式存在,说明它们的化学性质都______。
(2)在生产生活实践中,人类逐渐掌握了多种金属的治炼技术。
①比较两种铁矿石磁铁矿(主要成分Fe3O4)和菱铁矿(主要成分FeCO3),从化学的角度分析“磁铁矿作炼铁原科更具优势”。其主要原因是________。
②近代工业上采用电解熔融氧化铝(Al2O3)的方法治炼铝,Al2O3分解后得到两种单质,该反应的化学方程式为________。
(3)镁铝合金被誉为“21世纪绿色金属结构材料”,一种镁铝合金Mg17Al12是特殊的储氢材料,完全吸收氢气后得到MgH2和Al,该反应的化学方程式为_________。
(4)钛和钛合金是21世纪重要的金属材料,钛合金制品放在海水中数年,取出后仍光亮如新,是因为其_____(填字母序号)非常好。
A 可塑性
B 机械性能
C 抗腐蚀性能
(5)铁制品表面生成的铁锈很______,不能像铝表面致密氧化膜一样保护内部金属不再被进一步氧化。请你写出一条常见的防锈方法:__________。
(6)利用“活泼金属”可以制得H2,H2可用作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有___(填字母序号)。
A 金属原料的成本
B 生成过程中的能耗和污染
C 金属的回收利用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com