
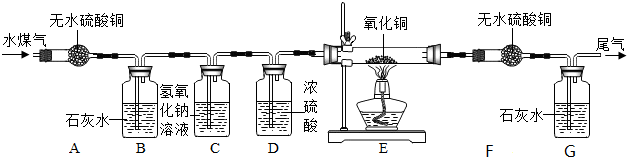
| 称量项目 | 反应前 | 反应后 |
| F玻璃管及所盛固体的质量 | 86.3g | 89.9g |
| G洗气瓶和所盛石灰水的质量 | 284.2g | 293.0g |
分析 (1)根据水能使白色硫酸铜变蓝分析,
(2)根据二氧化碳能使澄清石灰水变浑浊分析;
(3)根据用氢氧化钠溶液吸收二氧化碳分析;
(4)根据浓硫酸具有吸水性解答;
(5)根据水能使白色硫酸铜变蓝,二氧化碳能使澄清石灰水变浑浊分析.
解答 解:(1)水能使白色硫酸铜变蓝,先通过无水硫酸铜是检验是否含有水;故填:检验是否含有水;
(2)二氧化碳能使澄清石灰水变浑浊,再通过石灰水是检验是否含有二氧化碳的,B中的澄清石灰水变浑浊说明混合气体中含有二氧化碳,故填:二氧化碳;
(3)通过氢氧化钠是除去原来的二氧化碳气体,故填:除去原来的二氧化碳气体;
(4)前面的装置A是为了检验是否有水生成,后面的装置A是为了检验是否有水生成,从而确定是否有氢气存在.浓硫酸具有吸水性,则装置D的作用是:除去水蒸气;故填:除去水蒸气;
(5)若F中无水硫酸铜白色粉末不变蓝,说明没有氢气;G中的澄清石灰水变浑浊,则可燃气体中一定含有一氧化碳;若F中无水硫酸铜白色粉末变蓝,说明没有氢气,G中的澄清石灰水不变浑浊,说明没有一氧化碳,则可燃气体中一定含有甲烷.
若F中无水硫酸铜白色粉末变蓝,说明有氢气;G中的澄清石灰水变浑浊,说明有一氧化碳,根据表中实验数据,可燃气体的组成可能为氢气和一氧化碳或氢气、一氧化碳和甲烷.故填:一氧化碳;甲烷;2.
点评 本题以实验探究的形式考查常见气体氢气、一氧化碳、二氧化碳和水蒸气的性质,同学们要具有综合的化学知识才能做好此题.


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | pH为零的溶液既不显示酸性又不显示碱性 | |
| B. | 打开盛浓硫酸的试剂瓶塞,就可以看到白雾 | |
| C. | 把锌粒投入装有稀硫酸的试管中,试管壁发烫,说明金属与酸的反应是放热反应 | |
| D. | 能使紫色石蕊试液变红的溶液是酸性溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入石蕊试液 | 溶液变红 | 猜想三成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 判断 | 依据 |
| 不是KMNO4 | KMNO4能溶于水形成紫红色溶液 |
| 不是K2MnO4(填化学式) | 冲洗试管时出现深绿色溶液,说明该物质能溶于水 |
| 是MnO2 | 其他实验用过MnO2,知道它是不溶于水的黑色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 ”和“
”和“ ”分别表示不同质子数的原子在化学变化前后的微观模拟示意图下.请回答下列问题:
”分别表示不同质子数的原子在化学变化前后的微观模拟示意图下.请回答下列问题: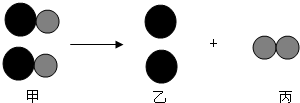
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com