
| A. | 0.9g | B. | 1.0g | C. | 6.5g | D. | 11.6g |
分析 锌与FeSO4溶液反应生成铁和硫酸锌,反应生成铁的质量小于消耗锌的质量,因此,反应后所得固体质量是减少的;利用反应的化学方程式,根据固体减少量可计算反应生成锌的质量.
解答 解:反应后置换出来的铁覆盖在锌片上,且生成铁的质量小于反应掉的锌的质量,锌片质量减少了10.9g-10g=0.9g.
设析出铜的质量为x.
Zn+FeSO4=ZnSO4+Fe 锌片质量减少
65 56 65-56=9
x 0.9g
$\frac{65}{x}=\frac{65-56}{0.9g}$
x=6.5g
故选C.
点评 利用反应前后固体质量的差,根据反应的化学方程式计算反应生成金属的质量,可以把复杂的计算过程简单化.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
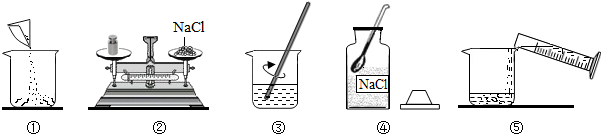
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸中都含有氢元素,所以含有氢元素的化合物一定是酸 | |
| B. | 锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气 | |
| C. | 碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性 | |
| D. | 酸能使紫色石蕊试液变红,CO2也能使紫色的石蕊试液变红,所以CO2是酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
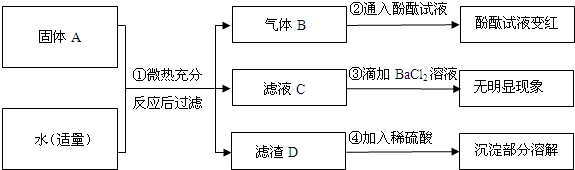
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
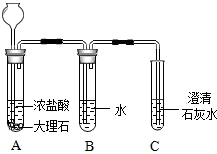 已知盐酸是HCl气体溶于水所形成的溶液.在实验室制取二氧化碳并检验其性质的实验中,如果用浓盐酸代替稀盐酸,并将产生的气体通入澄清的石灰水,看不到溶液变浑浊的现象.现有一同学用下列装置进行实验,却看到了澄清石灰水变浑浊的现象.请回答下列问题:
已知盐酸是HCl气体溶于水所形成的溶液.在实验室制取二氧化碳并检验其性质的实验中,如果用浓盐酸代替稀盐酸,并将产生的气体通入澄清的石灰水,看不到溶液变浑浊的现象.现有一同学用下列装置进行实验,却看到了澄清石灰水变浑浊的现象.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
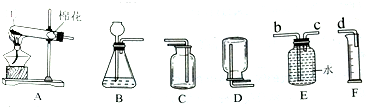
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 奥美拉唑肠溶胶囊是一种药物.如图摘录的是其说明书的一部分信息.
奥美拉唑肠溶胶囊是一种药物.如图摘录的是其说明书的一部分信息.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com