
【题目】在现代生活中,人们越来越注重微量元素的摄取.碘元素对人体健康有至关重要的作用.下表是某地市场销售的一种“加碘食盐”包装袋上的部分说明.
配料 | 氯化钠、碘酸钾(KIO3) |
含碘量 | (20mg~30mg)/kg |
保质期 | 18个月 |
食用方法 | 勿长时间炖炒 |
贮存方法 | 避光、避热、蜜蜂、防潮 |
请回答下列问题:
(1)由食用方法和贮藏指南可推测碘酸钾(KIO3)的化学性质之一是_____;
(2)计算碘酸钾(KIO3)中,钾元素、碘元素、氧元素的质量比_____;
(3)计算碘酸钾(KIO3)中,碘元素的质量分数是多少?_____.
【答案】不稳定,易分解 39:127:48 59.35%
【解析】
(1)根据加碘食盐的食用方法是勿长时间炖炒以及贮藏指南是避光、避热、密封、防潮可知碘酸钾(KIO3)的化学性质不稳定,易分解进行解答;
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答;
(3)根据化合物中某元素质量分数公式计算即可.
(1)加碘食盐的食用方法是勿长时间炖炒以及贮藏指南是避光、避热、密封、防潮可知碘酸钾(KIO3)的化学性质不稳定,易分解;故填:不稳定,易分解;
(2)由化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得碘酸钾(KIO3)中钾元素、碘元素、氧元素的质量比=39:127:48;故填:39:127:48;
(3)碘酸钾(KIO3)中,碘元素的质量分数=![]() ×100%=59.35%;故填:59.35%.
×100%=59.35%;故填:59.35%.


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:初中化学 来源: 题型:
【题目】如图所示,通过长颈漏斗向该装置中慢慢加入x,可观察到气球逐渐胀大,再慢慢加入y,又看到气球逐渐变小,则x、y可能分别为( )
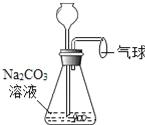
A.盐酸、硫酸铜溶液B.盐酸、饱和澄清石灰水
C.硫酸、氢氧化钠溶液D.硫酸、氯化镁溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取CaCl2和CaCO3的混合物12.5g于烧杯中,向其中滴加一定溶质质量分数的稀盐酸,请加稀盐酸的质量与产生气体质量的关系如图所示。求:
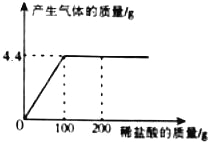
(1)混合物CaCO3中的质量为 ;
(2)稀盐酸中的溶质质量分数为 ;
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数?(写出计算过程,计算结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶未知浓度的氯化钠溶液,小丽要测定其溶质的质量分数。
实验步骤:
(1)取样:小丽测得该NaCl溶液的密度为1.2g/cm3,决定量取出50克氯化钠溶液作为样品量取时用到的仪器有_____。
(2)获取溶质:从氯化钠溶液中得到氯化钠的方法是______。
(3)称量食盐:小丽加了一个砝码,待天平静止时,出现如图所示的情况,小丽接下来的操作是:______。读数,得到氯化钠的质量。
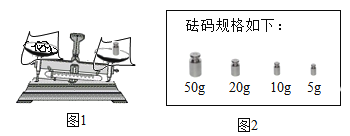
(4)小丽发现有少量氯化钠粘在玻璃棒等器皿上,这对测定结果的影响是___(写“偏大”或“偏小”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列反应的化学方程式:
(1)铁丝在氧气中燃烧_____;
(2)双氧水与二氧化锰混合_____;
(3)氢氧化钠溶液与稀盐酸反应_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】你注意过吗?家庭使用的铁制工具隔一段时间不用就变得锈迹斑斑,而街心广场矗立的不锈钢雕塑,几经风霜雨雪总能保持原有的本色.锰(Mn)就是不锈钢的主要添加元素之一,它可以提高不锈钢的耐腐蚀性.
(1)铁与空气中的水和_____直接接触会导致铁制品的锈蚀.
(2)不锈钢属于_____(填序号).
A纯净物 B金属材料 C合成材料 D复合材料
(3)某化学兴趣小组的同学为了探究锰、镁、铜三种金属的活动性,他们首先将锰片插入到氯化镁溶液中,一段时间后,观察到锰片表面无明显变化;将锰片插入到氯化铜溶液中,一段时间后观察到锰片表面有红色物质生成.
①根据以上实验判断,三种金属的活动性由强到弱的顺序是_____.
②写出单质锰(Mn)与氧化铜溶液反应的化学方程式_____(该化合物中Mn元素显+2价).
(4)向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,反应停止后过滤,得到滤渣和滤液,向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有_____(填化学式),滤液中一定含有的溶质是_____(填化学式).
(5)在高温下,利用焦炭与氧气反应生成的一氧化碳可把铁从铁矿石里还原出来.某炼铁厂现用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是_____t.(计算结果精确到0.1)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某纯碱样品中含有少量的氯化钠,为了测定该纯碱中碳酸钠的质量分数,取一定量的该纯碱样品全部溶解在100g水中,再加入氯化钙溶液141g,恰好完全反应.(反应方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl)经过滤、干燥后称的沉淀质量为10g,所得滤液中氯化钠的质量分数为5%.请计算:
①氯化钙溶液中溶质的质量分数_____.
②纯碱样品中碳酸钠的质量分数_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科普阅读
热敏纸
双酚A(Bisphenol A,化学式C15H16O2)白色针状晶体。
![]()
双酚A (简写为BPA)可在热敏纸上充当显影剂和无色染料,浓度高达每克纸约20毫克。这种热敏纸可用于飞机票,ATM机、加油机和收银机的凭据以及其它类型的小票。热敏纸上显影剂的显色反应是可逆的,有色产物会不同程度地自行分解,字迹颜色会慢慢退色越来越浅淡,直至自然退色到字迹完全消失在白纸之中。研究者们首次证明,消费小票(热敏纸)上喷涂的双酚A(BPA),通过接触先粘附在手上,然后经过手的皮肤被人体吸收,使人体内的BPA含量显著提高。


在快餐店等场所,人们经常在进食前使用手部免洗消毒液,然后点餐时又会接触到小票,免洗消毒液中含肉豆蔻酸异丙酯、丙二醇和乙醇等成分。研究者们试图了解这一做法会对人体吸收BPA有何影响,为此做如下实验。在实验中,先让被测试者一只手擦拭免洗消毒液,在还未干透的情况下,用手掌直接握住热敏纸;另一只手未使用消毒液,用干燥的手掌握住同样大小的热敏纸。随后,对手掌表面残留的BPA进行提取和分析。结果如下图。
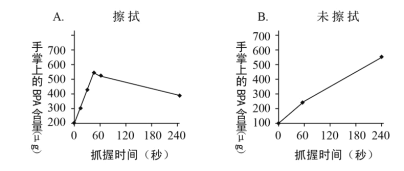
根据以上资料,回答下列问题:
(1)双酚A属于_____(填“有机物”或“无机物”)。一个双酚A分子中含有_____个氧原子。
(2)“小票”能否作为重要的证据长期保存,并说明原因_____。
(3)分析坐标图可以看出,在使用免洗消毒液后,手掌上BPA的含量的变化趋势是_____,与未使用消毒液的对比, 说明免洗消毒液能_____人体对BPA的吸收。
(4)虽然关于双酚A的毒理学研究已有很多,但它对于人体的毒性目前还没有权威、确切的结论。研究人员认为,应该开发更安全的材料或方法来代替热敏纸。现有条件下,你认为在快餐厅就餐前谨慎的做法是_____,以防双酚A趁虚而入。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com