
【题目】某工厂欲测定铝土矿中Al2O3 的含量,将矿石粉碎(其中杂质既不溶于水也不与酸反应),进行如下实验:
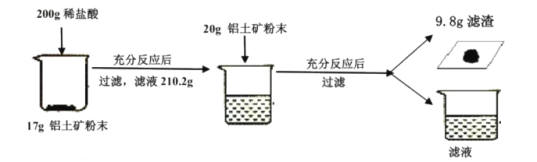
请回答下列问题:
(1)上述实验过程中发生反应的化学方程式为_____________。
(2)铝土矿中Al2O3的质量分数为_________________。
(3)根据已知条件列出求解200g稀盐酸中溶质质量(X)的比例式_________。
(4)若将最终所得溶液蒸发掉20. 4g水,所得不饱和溶液中溶质的质量分数为________。
(5)该炼铝厂每天用上述铝土矿170t来生产铝合金,则理论上日产含镁46%的铝镁合金的质量为_____________。
【答案】(1)![]()
(2)60%
(3)![]()
(4)12.5%
(5)103t
【解析】
(1)铝土矿中参与反应的只有氧化铝,氧化铝与盐酸反应生成氯化铝和水,据此书写化学方程式;
故答案为:![]() 。
。
(2)氧化铝与盐酸反应生成氯化铝和水,不会引起溶液质量变化,只有不能反应的杂质,被过滤后才能减少质量,根据上述实验过程,200g稀盐酸与17g铝土矿粉末反应后,滤液再加入20g铝土矿粉末,铝土矿粉末还能溶解,说明在200g稀盐酸加入17g铝土矿粉末中盐酸过量,所以在200g盐酸与17g铝土矿混合溶液反应后过滤,减少的质量为杂质质量=200g+17g-210.2g=6.8g,反应的氧化铝质量=17g-6.2g=10.2g,所以其中氧化铝的质量分数=![]() ;
;
故答案为:60%。
(3)根据(2)中可知铝土矿中氧化铝质量分数为60%,所以20g铝土矿中氧化铝质量=20g×60%=12g,残渣质量=20g-12g=8g,所以过滤后的残渣中有未反应的氧化铝,消耗掉氧化铝的质量=20g-9.8g=10.2g,因此200g盐酸总共消耗氧化铝的质量=17g×60%+10.2g=20.4g,

![]()
故答案为:![]() 。
。
(4)最终溶液质量=230.2g-9.8g=220.4g,此时蒸发20.4g水,溶液质量=220.4g-20.4g=200g,设生成氯化铝的质量为m,

![]() m=25g,溶液溶质质量分数=
m=25g,溶液溶质质量分数=![]() ;
;
故答案为:12.5%。
(5)根据题目要求,铝的含量为100%-46%=54%,根据铝元素质量守恒,铝土矿中铝元素的质量=铝合金中铝元素的质量,设铝合金质量为y,175t×60%×![]() =y×54%,y=103t;
=y×54%,y=103t;
故答案为:103t。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:初中化学 来源: 题型:
【题目】图3的Ⅰ所示为80℃时将一定质量的甲溶液进行降温操作后的变化情况;图3的Ⅱ所示为t2°C时将13g固体乙加入10g水中的溶解情况;图4所示为甲、乙两种固体的溶解度曲线。下列说法正确的是
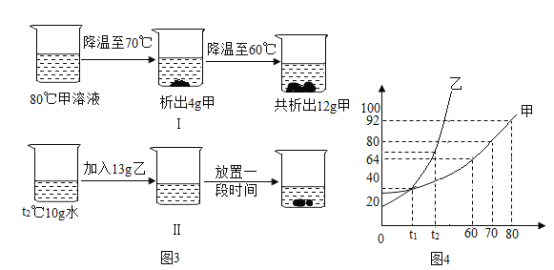
A.80℃的甲溶液是不饱和溶液
B.乙溶于水过程中一定吸收热量
C.60℃时,13g乙在10g水中一定不能全部溶解
D.t2℃时分别将溶有等质量溶质的甲、乙饱和溶液降到t1℃所得溶液质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图中 A、B 分别是某微粒的结构示意图,回答下列问题:
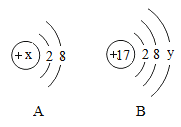
(1)若A是某阳离子的结构示意图,则 x可能是下列选项中的_____(填字母序号)。
a 8 b 10 c 11 d 12
(2)若A中 x=12,则 A、B 所表示的元素形成化合物的名称为_____。
(3)若A中 x=8,写出其对应元素形成的单质在实验室制备的反应方程式(只写一种):_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(3分)下图是甲烷在一定条件下发生分解的微观模拟图。

(1)在图B中将相关粒子图形补充完整;
(2)A是化合物,你判断的微观依据是 ;
(3)结合该图示从微观角度解释由B到C变化的实质是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲乙两种固体物质的溶解度曲线,回答:
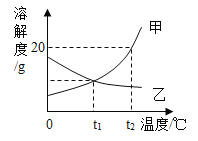
(1)t2℃时,甲的溶解度为______
(2)下列说法正确的是 ______
At2℃时,100克的水中溶解20克的甲能达到饱和
B甲中含有少量的乙可采用蒸发溶剂结晶的方法提纯甲
C将t1℃甲乙的升温至t2℃时,甲乙溶液的溶质质量分数都不变.
Dt2℃时,将等质量的甲乙两物质分别加水配成饱和溶液,甲溶液的质量比乙溶液的质量大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们利用下图所示装置进行气体的制备实验(A~F为装置编号)
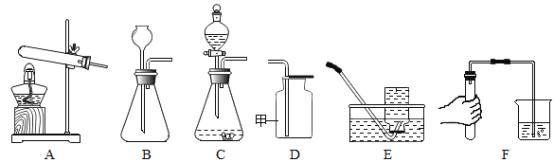
①写出上图D装置中甲仪器的名称_____。
②用A装置加热氯酸钾和二氧化锰的混合物制取氧气,化学方程式为_____,其中二氧化锰起_____作用;收集氧气可选择_____(填装置编号)。
③实验室制备二氧化碳通常选择下列药品中的_____(填药品序号)。
a.稀盐酸 b.熟石灰 c.块状石灰石 d.稀硫酸
通常检验二氧化碳气体的反应可用化学方程式表示为_____。
④常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体,若要控制滴加液体的速率,可选择的发生装置是_____(填装置编号)。
⑤制取气体前应先检查装置的气密性,若按F图所示操作,结果在导管口未看到气泡,其可能原因与下列因素无关的是_____(填序号)。
a.将烧杯换成水槽 b.导管伸入水中位置过深,气体无法逸出
c.将水换成冰水 d.先用手捂住试管壁,再将导管另一端插入水中
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁是生活中最常见的金属。请你用所学知识解答下列问题
(1)用赤铁矿石炼铁的原理是_____(写化学方程式)
(2)做铁丝燃烧实验时,铁丝末端螺旋状缠绕在一根火柴上,火柴的作用_____;细铁丝在氧气中能燃烧,生成黑色固体是_____(写化学式);小明在做铁丝燃烧实验时,瓶底有水集气瓶也炸裂的原因是_____。
(3)常用稀盐酸除去铁锈,原因_____(写化学方程式);
(4)将铁片放入盛有硫酸铜溶液的试管中,反应一段时间后,观察到铁片表面_____析出,发生反应的方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图,是甲、乙两种固体物质(均不含结晶水)在水中的溶解度曲线。下列说法不正确的是( )
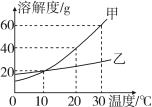
A.10℃时,甲、乙的溶液中溶质的质量分数可能相同
B.保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液
C.30℃时,将40g 甲物质加入50g水中,充分溶解后溶液的质量为80g
D.10℃ 时,将两种物质的饱和溶液升温至30℃ ,溶液中溶质的质量分数都增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com