
【题目】取氯化钠和碳酸钠的混合物10.6克于烧杯中,完全溶解于一定量的水中,向所得溶液中滴加10%的稀盐酸,所加稀盐酸与生成气体质量如图所示,求:

(1)写出图中A点表示的溶质的化学式_______。
(2)图中BC段表示的意义是________。
(3)原混合物中碳酸钠的质量分数____________
【答案】NaCl 、Na2 CO3 盐酸过量 50%
【解析】
(1)向氯化钠和碳酸钠的混合溶液中滴加盐酸,盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,所以图中A点表示碳酸钠没有反应完毕,所以A点中的溶质有氯化钠、碳酸钠,化学式分别为:NaCl、Na2CO3;
(2)向氯化钠和碳酸钠的混合溶液中滴加盐酸,盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,碳酸钠反应完毕后二氧化碳的质量不再改变,所以图中BC段表示的意义是碳酸钠反应完毕后二氧化碳的质量不再改变即盐酸过量;
(3)分析图像中的信息可以知道当生成的气体达到2.2g后,气体的质量不再增加,所以可以判断生成气体的最大值为2.2g。
设:生成2.2克二氧化碳,需要碳酸钠的质量为x。

![]() 解得:x=5.3g;
解得:x=5.3g;
原混合物中碳酸钠的质量分数=![]() 。
。


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:初中化学 来源: 题型:
【题目】观察下列课内实验回答问题。
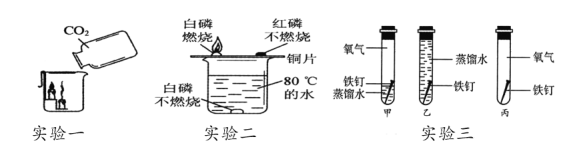
(1)实验一得出CO2的化学性质有_________________;
(2)实验二中的,通过铜片上的白磷和红磷实验现象的对比,可得出的燃烧的条件之一是___________。
(3)实验三中能验证铁生锈需要氧气的试管是___________(选填甲、乙、丙)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学用语与对应表述相符的是( )
A. 2个硫酸根离子——2SO![]() B. 2个铁离子——2Fe2+
B. 2个铁离子——2Fe2+
C. 3个氧原子——O3D. 氧化镁——MgO2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~E是初中化学常见物质。图中“﹣”表示相连的物质能发生反应,“→”表示物之间的转换关系。
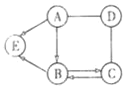
其中A是人体胃液中含有的酸,B和C组成元素相同,D是铁锈的主要成分。E物质的名称是_____,A和D的化学方程式为_____,C和D反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,无色液体A和黑色粉末B混合后,生成无色液体C和能使带火星的木条复燃的气体D,将烧得红热的银白色金属E伸入集满气体D的集气瓶中,火星四射,生成黑色固体F.下列有关说法中错误的是

A. 上述物质中共有四种氧化物
B. 上述反应中有两个分解反应
C. F为氧化铁
D. 做反应④的实验时,集气瓶底应事先放少量水或细沙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将宏观、微观及化学符号联系在一起是化学学科的特点。某化学反应微观示意图如图所示,下列叙述正确的是
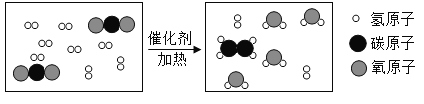
A. 反应前后各元素化合价不变
B. 该化学变化中发生改变的微粒是原子
C. 该反应不符合质量守恒定律
D. 参加反应的CO2和H2分子个数比为1:3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钢铁的使用十分普遍,但世界上每年有将近总产量十分之一的钢铁因锈蚀而损失。为探究铁锈蚀的原因,分别取 3 枚洁净无锈的铁钉放入试管中,进行如下实验:

(1)进行实验一时,采用的是经煮沸后迅速冷却的蒸馏水,将水煮沸的目的是_____。
(2)大多数同学都观察到了实验一、实验二中铁钉无锈,实验三中铁钉生锈的现象,得出铁生锈的条件是______。某同学却发现本组实验二中的铁钉表面出现了少量铁锈,经仔细检查后发现胶塞已塞紧, 产生这种现象的原因可能是______。
(3)实验室中可用盐酸除铁锈,其原理是________(用化学方程式表示)。
(4)工业上用锈蚀的废铁可以回炉炼铁,其原理是________(用化学方程式表示)。
(5)写出一种防止铁生锈的方法_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种物质在水中的溶解度曲线.

(1)t2℃时,甲的溶解度为________;
(2)t3℃时,等质量甲、乙、丙的饱和溶液降温到t2℃,所得溶液质量的大小关系是_________________;
(3)t1℃时,丙的饱和溶液中含有少量的甲,现要提纯丙并得到丙的固体,可以采用的操作方法是______________________;
(4)下列说法正确的是___________.
A 将甲、乙、丙的溶液分别从t1℃升温到t2℃,不考虑水分的蒸发,则溶质质量分数可能都不变
B t2℃时,向100g甲的饱和溶液中加入100g水,充分搅拌后溶质质量分数为10%
C t3℃时,等质量的甲、乙、丙分别制成饱和溶液,需要水的质量最多的是丙
D t2℃时,升高丙溶液的温度,一定有晶体析出.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组为了测定“碳还原氧化铜”实验中所用的氧化铜样品中的CuO含量,进行如下实验:用过量的稀盐酸溶解5g样品(杂质不与盐酸反应且不溶于水),过滤,取100g滤液,向其中加入NaOH溶液,所得实验数据如图:
(1)从图可知,加入的NaOH先跟滤液中 _________ 反应,后跟 _________ 反应.(写化学式)
(2)该样品中CuO的质量是 _________ .
(3)计算所加氢氧化钠溶液中溶质的质量分数.(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com