
���� ����ϡ���ᷴӦ�������������������������������������Լ����������������������������Լ���̼����������һ�����Լ���̼Ԫ�ص������������Ӷ������ж����Ͻ�����࣮
��� �⣺��11.5g���Ͻ�����������Ϊx��
Fe+H2SO4�TFeSO4+H2����
56 2
x 0.4g
$\frac{56}{x}$$\frac{2}{0.4g}$��
x=11.2g��
̼Ԫ����������Ϊ��$\frac{11.5g-11.2g}{11.5g}$��100%=2.6%��
��Ϊ2.0%��2.6%��4.3%�����ԸúϽ���������
�𣺸����Ͻ���������
���� ������Ҫ����ѧ�����ü��跨�ͻ�ѧ����ʽ���м�����ƶϵ�����������ʱҪע��淶�Ժ�ȷ�ԣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
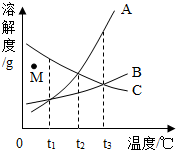 ��ͼΪA��B��C���ֹ������ʵ��ܽ������ͼ��A��B��C��������ʱ�������ᾧˮ������������ͼ��ʾ������˵����ȷ���ǣ�������
��ͼΪA��B��C���ֹ������ʵ��ܽ������ͼ��A��B��C��������ʱ�������ᾧˮ������������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | t2��ʱ���ܽ������������A | |
| B�� | ����M�㴦C�IJ�������Һ��Ϊ������Һ������ѡ��ķ����ǽ����¶� | |
| C�� | t2��ʱ������������A��B��C�ı�����Һ�����µ�t3�棬��Һ���ܼ������Ĵ�С��ϵ�ǣ�����ˮ�Ļӷ���B��A=C | |
| D�� | t1��ʱ����A��B��C���ֹ������ʷֱ�����ˮ������Һ��������������C��A=B |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
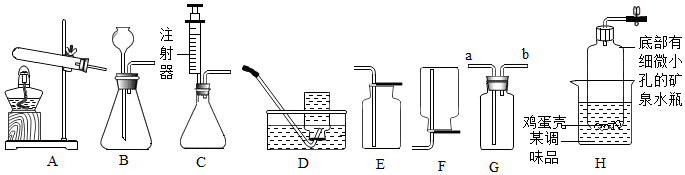
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
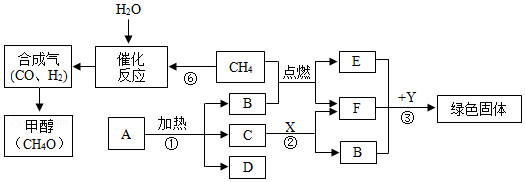
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��Ϊ�ǽ���Ԫ�� | B�� | ��ԭ�ӵ����ԭ������Ϊ32.06g | ||
| C�� | ��ԭ�Ӻ���������Ϊ16 | D�� | ��Ԫ�صķ���ΪS |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ֽ����©���ڱ� | B�� | ����ʱҺ�治Ҫ������ֽ��Ե | ||
| C�� | ����������������ֽһ�� | D�� | ©���¶˽����ձ��ڱ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
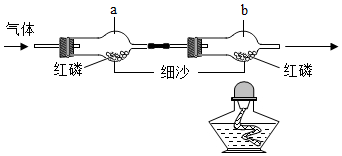 ͬѧ����ʵ�����а�ͼ��ʾװ��̽��ȼ�յ����������г���������ȥ��
ͬѧ����ʵ�����а�ͼ��ʾװ��̽��ȼ�յ����������г���������ȥ���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com