
【题目】某工厂产生的烧渣(主要含FeO、Fe2O3,还有一定量的SiO2)可用于制备七水合硫酸亚铁晶体(FeSO47H2O),其工艺流程如下:

查阅资料:SiO2不溶于水,也不与稀硫酸反应。
(1)“浸取”步骤中,FeO、Fe2O3和稀硫酸发生反应的化学方程式分别为FeO+H2SO4=FeSO4+H2O、_____。
(2)为提高“浸取”步骤的反应速率,可采取的具体措施有_____(写1条,不考虑“搅拌”和“使用催化剂”)。
(3)“过滤”操作需要使用的玻璃仪器有烧杯、玻璃棒和_____,“过滤”后得到的滤液中的溶质有_____(填化学式)。
(4)“还原”步骤的目的是将Fe3+转化为Fe2+,试剂X可用SO2或Fe。
①若试剂X是SO2,转化原理为SO2+Fe2 (SO4)3+2Y═2FeSO4+2H2SO4,则Y的化学式是_____。
②若试剂X是Fe,转化原理为Fe+Fe2 (SO4)3═3FeSO4.测得“还原”后溶液的pH明显增大,其原因是_____。
【答案】Fe2O3+3H2SO4═Fe2(SO4)3+3H2O 。把烧渣研碎漏斗 ,FeSO4、Fe2(SO4)3、H2SO4 (填化学式)。H2O 。铁消耗过量的硫酸,导致溶液酸性减弱 。
【解析】
化学反应遵循质量守恒定律,即反应前后元素种类、原子个数、原子质量都不变;稀硫酸和氧化亚铁反应生成硫酸亚铁和水,和氧化铁反应生成硫酸铁和水;反应物接触越充分、温度越高,反应速率越快;铁和稀硫酸反应生成硫酸亚铁和氢气。
(1)氧化铁与硫酸反应生成硫酸铁和水,SiO2不溶于水,也不与稀硫酸反应。“浸取”步骤中,FeO、Fe2O3和稀硫酸发生反应的化学方程式分别为FeO+H2SO4=FeSO4+H2O、Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
(2)反应物接触越充分、温度越高,反应速率越快。为提高“浸取”步骤的反应速率,可采取的具体措施有将烧渣研碎、升高温度等;
(3)“过滤”操作需要使用的玻璃仪器有烧杯、玻璃棒和漏斗,根据第(1)题的分析可知,“过滤”后得到的滤液中的溶质有反应生成的硫酸亚铁、硫酸铁和过量的硫酸化学式分别为FeSO4、Fe2(SO4)3、H2SO4;
(4)①由化学方程式可知,反应前后,硫原子都是4个,铁原子都是2个,反应后氢原子是4个,根据质量守恒定律可知,氢原子反应前应该是4个,包含在2Y中,反应后的氧原子是16个,反应前应该是16个,其中2个包含在2Y中,反应的化学方程式为:SO2+Fe2 (SO4)3+2H2O═2FeSO4+2H2SO4,则Y的化学式是H2O;
②pH增大,溶液的酸性减弱。测得“还原”后溶液的pH明显增大,其原因是铁消耗过量的硫酸,导致溶液酸性减弱。


 智慧小复习系列答案
智慧小复习系列答案科目:初中化学 来源: 题型:
【题目】汽车是现代生活中常见的一种交通工具.
⑴CNG双燃料(汽油和天然气)环保汽车已投入使用,天然气的主要成分甲烷发生完全燃烧的化学反应方程式_________。
⑵汽油是石油_______的一种产品。燃烧化石燃料会带来严重的环境问题,如______(举一例)。
⑶汽车的外壳是钢铁材料,下列关于钢的叙述正确的是(_________)
A.钢是铁和碳等元素形成的合金 B.钢有良好的导电导热性
C.钢的硬度比纯铁大 D.高炉炼铁的产品是钢
⑷ “火立熄”是一种小型灭火用品。“火立熄”灭火时释放的粉末覆盖在燃烧物上,同时放出不可燃烧气体,使火焰熄灭。“火立熄”的灭火原理是(_______)
A.清除可燃物 B.使燃烧物与氧气隔绝 C.降低燃烧物的着火点
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属钛(Ti)抗腐蚀性能好,露置于空气中数年,仍光亮如初。以金红石(主要成分是 TiO2)为原料生产金属钛的步骤主要有:①在高温下,向金红石与焦炭的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;②在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2。下列说法不正确的是( )
A. ①中的反应为TiO2+C+2Cl2![]() TiCl4+CO2
TiCl4+CO2
B. ②中的稀有气体的作用是隔绝空气
C. ②中发生的反应为置换反应
D. 金属钛在常温下不与O2反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是A、B、C三种物质的溶解曲线回答下列问题:
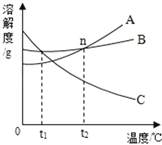
(1)温度在t1℃时,这三种物质的溶解度由大到小的顺序为_____;
(2)点n表示的意义为______________________;
(3)从B溶液中得到B的晶体,采用最合理的方法是____________________.
(4)将A、B、C饱和溶液从t2℃降温到t1℃时,溶质质量分数保持不变的是__________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为验证“加热碳酸氢铵”所发生的变化,两同学分别用甲、乙所示装置进行实验,发现两实验中碳酸氢铵固体均消失,乙实验中还观察到无水硫酸铜变蓝、浸有酚酞试液的棉球变红、澄清石灰水变浑浊。
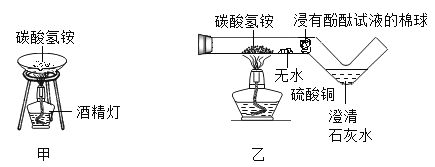
资料:无水硫酸铜呈白色,遇水后呈蓝色。
下列说法错误的是
A. 甲实验不如乙实验环保
B. 只根据甲实验“固体消失” 这一现象,可验证碳酸氢铵发生了分解
C. 乙实验有利于学生分析“固体消失” 的原因
D. 只根据乙实验的现象,可验证NH4HCO3![]() NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源,也是人类最宝贵的资源。请回答下列有关问题:
(1)活性炭常用于净水,是利用其__________。
(2)建设新农村后,村民已经用上自来水,加入_________可检验自来水是否为硬水。日常生活中通过________的方法可降低水的硬度。
(3)实验室通常用下图装置来电解水,该装置中,A试管的电极与电源的______极相连;当A试管中产生的气体体积为10mL时,B试管中产生的气体体积为______mL。
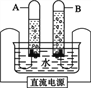
(4)下列做法有利于节水的是________(填字母序号)。
A.农业上改漫灌为滴灌 B.用大量水冲洗汽车
C.用淘米水浇花 D.用洗衣服水冲厕所
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种物质的溶解度曲线图1.请回答:

①t1℃时,溶解度相等的两种物质是_____。
②物质A中混有少量的物质B,现要得到较纯的A物质,可采用的结晶方法是_____。
③如图2所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是_____,乙试管内的溶液为_____溶液(填“饱和”或“不饱和”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下表回答问题:
温度(℃) | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 100℃ | |
溶解度 (g/100g 水) | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 246 |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 39.8 | |
① 20℃时,50 克水中最多能溶解 NaCl______ g。
② 将硝酸钾的不饱和溶液转化为饱和溶液的方法________。(任写一种方法)若硝酸钾溶液中混有少量氯化钠,可通过______的方法提纯。
③ 硝酸钾和氯化钠溶解度相同的温度范围为______。(填编号)
I. 0℃-10℃ II. 10℃-20℃ III. 20℃-30℃ IV. 30℃-40℃
④ 30℃时,在两个各盛有 100 克水的烧杯中,分别加入相同质量的硝酸钾和氯化钠,充分溶解后,其结果如图所示。

I. 两烧杯中的溶质质量分数大小关系为 A________ B。(填“>”“<”或“=”)
II. 加入的甲物质是________。
III. 对 B 中乙溶液的分析,正确的是______。
a. 加水,溶质质量分数一定变小
b. 一定是该温度下的不饱和溶液
c. 溶解的固体质量一定大于 36.3g,小于 45.8g d. 降温至 10℃,一定有晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“分解”与“化合”是两种研究物质组成的方法。
研究问题 | 探究水的元素组成 | 探究氧化汞的元素组成 |
研究方法 | 水的分解 | 汞与氧气的化合 |
搜集证据 |
用燃着的木条检验a端气体,气体燃烧发出________色火焰,发生反应的化学方程式为________;用带火星的木条检验b端气体,观察到________。 | 汞与氧气化合的微观过程示意图
请将上图中反应后缺少的微粒补画完整________。 |
结论 | 水是由________元素组成的。 | 氧化汞是由氧、汞元素组成的。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com