
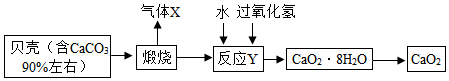
分析 (1)气体X是CO2,其固态常用于人工降雨、制造舞台云雾等;
将过氧化钙晶体与溶液分离的方法是过滤;
(2)冰水混合物的温度是0℃;
根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
氧化钙能和水反应生成氢氧化钙,氢氧化钙微溶于水;
(3)根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)气体X是CO2,其固态常用于人工降雨,制造舞台云雾等,将过氧化钙晶体与溶液分离的方法是过滤.
故填:人工降雨等;过滤.
(2)反应Y需控制温度在0~5℃,可将反应容器放在冰水混合物中;
氧化钙和水、过氧化氢反应生成过氧化钙晶体,反应的化学方程式为:CaO+7H2O+H2O2=CaO2•8H2O;
过氧化钙晶体中常含有Ca(OH)2杂质,原因是氧化钙和水反应生成氢氧化钙,氢氧化钙微溶于水.
故填:冰水混合物;CaO+7H2O+H2O2=CaO2•8H2O;氧化钙和水反应生成氢氧化钙,氢氧化钙微溶于水.
(3)设样品中过氧化钙晶体的质量为x,
2CaO2•8H2O$\frac{\underline{\;\;△\;\;}}{\;}$CaO+O2↑+16H2O↑,
432 32
x 3.2g
$\frac{432}{x}$=$\frac{32}{3.2g}$,
x=43.2g,
样品中CaO2•8H2O的质量分数为:$\frac{43.2g}{50g}$×100%=86.4%,
故填:86.4%.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 空气中的铁比铝更易锈蚀,是因为铁比铝的金属活动性更强 | |
| B. | 生活中用活性炭净化水,是因为活性炭有杀菌作用 | |
| C. | 煤粉碎后燃烧更彻底,是因为粉碎后降低了煤的着火点 | |
| D. | 石灰水能使酚酞试液变红,是因为溶液里含有OH- |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2 | B. | O2 | C. | H2O | D. | H2O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
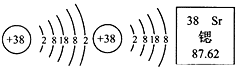
| A. | 锶的相对原子质量为87.62g | B. | 锶原子核外共有38个电子 | ||
| C. | 锶元素属于金属元素 | D. | 硫酸锶的化学式可表示为SrSO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
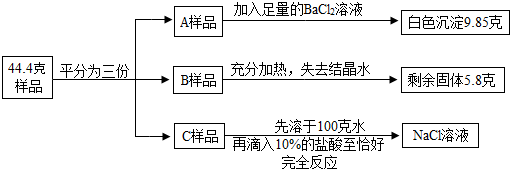
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
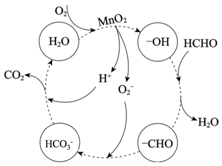 MnSO4在工业中有重要应用,可用软锰矿浆(主要成分为MnO2和水,含有Fe2O3、FeO、Al2O3和少量PbO等杂质)浸出制备MnSO4.
MnSO4在工业中有重要应用,可用软锰矿浆(主要成分为MnO2和水,含有Fe2O3、FeO、Al2O3和少量PbO等杂质)浸出制备MnSO4.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com