
【题目】根据下列实验装置图,回答有关问题。
a. 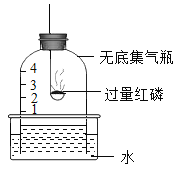 测定空气中氧气的含量
测定空气中氧气的含量
b. 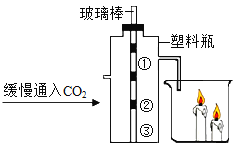 探究二氧化碳的性质
探究二氧化碳的性质
c. 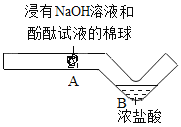 探究中和反应
探究中和反应
(1)A实验中使用过量红磷的目的是________,该实验能得出的结论是________。
(2)B图所示实验中,①③为湿润的石蕊试纸,②为干燥石蕊试纸。将高、矮蜡烛点燃。塑料瓶中发生反应的化学方程式为_________。该实验能说明二氧化碳具有的化学性质是_________。
(3)C图所示实验能说明发生了中和反应的现象是__。该实验的优点是____________(写一点)。
【答案】将氧气充分耗尽 氧气约占空气体积的五分之一 ![]() 二氧化碳能与水反应生成弱酸(碳酸);不燃烧不支持燃烧 棉球由红色变为无色 节约药品、环保
二氧化碳能与水反应生成弱酸(碳酸);不燃烧不支持燃烧 棉球由红色变为无色 节约药品、环保
【解析】
(1)实验A是测定空气中氧气的含量,需要完全将瓶内的氧气完全消耗,然后在大气压的作用下,瓶中的水上升,瓶中水上升的体积就是瓶中空气中氧气的体积,因此A实验中使用过量红磷的目的是将氧气充分耗尽,该实验能得出的结论是氧气约占空气体积的五分之一。
(2)实验B探究二氧化碳的性质,塑料瓶中湿润的石蕊试纸变为红色,干燥石蕊试纸不变色,说明二氧化碳能与水反应生成酸,反应的方程式为![]() ;塑料瓶中石蕊试纸的变化说明二氧化碳能与水反应生成弱酸(碳酸),烧杯中的蜡烛燃烧说明二氧化碳气体不能燃烧也不支持燃烧。
;塑料瓶中石蕊试纸的变化说明二氧化碳能与水反应生成弱酸(碳酸),烧杯中的蜡烛燃烧说明二氧化碳气体不能燃烧也不支持燃烧。
(3)实验C探究中和反应,浸有氢氧化钠溶液和酚酞溶液的棉球呈红色,酸碱中和反应之后,碱性减弱直至消失,因此酚酞逐渐褪色,现象是棉球由红色变为无色。该实验都在容器内进行因此优点是节约药品、环保


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:初中化学 来源: 题型:
【题目】将甲烷在高温等条件下转化为其它有机物是重要的研究课题,某研究发现使用特殊催化剂(CeO2、Cu2O、Cu的混合物),在反应混合物中加入乙能够更有效地将甲烷转化为丙,该反应原理如下图所示,下列说法错误的是
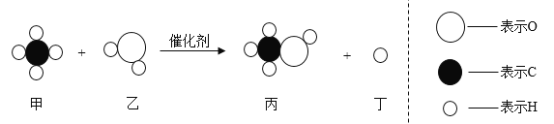
A.甲烷是重要的化石能源
B.丙的化学式是CH3OH
C.乙是氧化物
D.参加反应的甲和乙的质量比是1:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类历史上,出现过多次由不同病毒引起的大规模传染病,2019年12月爆发的新型冠状病毒(2019-nCoV),可以通过打喷嚏,咳嗽以及接触被病毒污染的物品等方式引发感染,专家提示:乙醚、75%的乙醇溶液,含氯的消毒剂、过氧乙酸等,均可有效灭活病毒,其中过氧乙酸的化学式为C2H4O3。下列关于过氧乙酸的说法正确的是
A.过氧乙酸是无机化合物
B.过氧乙酸由三个元素组成
C.过氧乙酸中氧元素的质量分数最大
D.过氧乙酸中碳、氢、氧元素的质量比为2:4:3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A-I是初中化学常见的物质。常温下A、D、H、I为气体,E为液体,其他为固体。A、B、C、D是单质,B为红色。F与G,H与I组成元素相同。G中两元素的质量比为7:3。这些物质之间相互关系如图所示,图中“-”表示能相互反应;“→”表示转化关系;部分反应物、生成物及反应条件已略去。
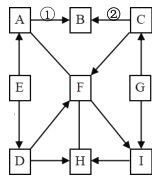
(1)写出化学式:B________,E________,G________。
(2)E→D反应的化学方程式是____________________。
(3)F→I反应的化学方程式是____________________。
(4)反应①②的基本反应类型相同,该反应类型为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学利用以下实验装置准确测定出某混合气体中(成分:CO、CO2、H2)各组分的质量分数。实验时先通一段时间氮气,再继续实验(已知: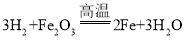 ,实验中供选用的试剂:①NaOH溶液,②澄清石灰水,③浓硫酸,且装置中试剂均足量)。下列说法正确的是(______)
,实验中供选用的试剂:①NaOH溶液,②澄清石灰水,③浓硫酸,且装置中试剂均足量)。下列说法正确的是(______)
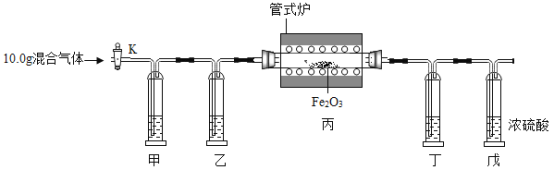
A 实验时,应先打开活塞K,再用管式炉加热
B 装置戊的作用是吸收反应生成的水蒸气
C 测得装置甲、装置丁反应前后的质量差即可求出各组分的质量分数
D 甲、乙、丁中依次盛装试剂的编号为_______(从①②③中选,可重复利用)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在宏观、微观和符号之间建立联系是化学特有的思维方式。如下图是几种粒子的结构示意图和D元素在周期表中的信息,根据图示回答下列问题:

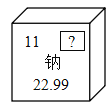
(1)钠元素的相对分子质量是__________;属于___________(填“金属”或“非金属”)元素。
(2)________表示的是阳离子(填序号),其离子符号为___________。
(3)ABCD表示的是_____种不同元素(填数字);_____所表示的粒子化学性质相似(填序号)。
(4)C、D两种元素形成化合物的化学式为__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】含次氯酸钠(NaClO)的溶液是一种在抗击新冠疫情中经常用到的抗菌消毒剂。请根据其化学式进行下列计算:
(1)次氯酸钠的相对分子质量;
(2)次氯酸钠中氯原子和氧原子的质量比(最简比);
(3)次氯酸钠中,钠元素的质量分数是(结果保留至0.1%);
(4)与149g次氯酸钠含有相同质量氯元素的氯化钙质量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海洋中蕴藏着丰富的化学资源,从海水中提取金属镁的主要步骤如下:资料:海滩贝壳的主要成分是CaCO3

(1)为节约资源,试剂A常用海滩贝壳为原料制得,则试剂X为__________(填化学式)。
(2)操作Y的名称为_____________________。
(3)在熔融状态下的MgCl2,通电后会生成镁与一种气体单质,该反应的化学方程式为___________;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(2018唐山路南区二模)兴趣小组用如图1、2所示进行镁条在空气中燃烧的实验。图1实验中,当燃烧停止、冷却后打开弹簧夹,进入集气瓶中水的体积约占瓶内原液面以上容积的70%。图2实验中,发现镁条燃烧除生成白色固体外,还生成少量淡黄色固体。
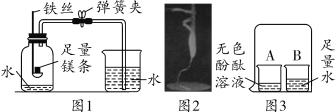
(问题与思考)(1)图1实验说明镁条与氮气发生了反应,依据是:_____。
(2)图2实验中淡黄色固体除含镁元素外还有什么元素?
(查阅资料)①镁能与氮气剧烈反应生成黄色的氮化镁固体;
②氮化镁可与水剧烈反应产生氨气。
(作出猜想)图2实验中淡黄色固体是氮化镁。
(实验一)按图3进行实验,取少量图2实验中淡黄色固体放入B烧杯中,观察到B烧杯中产生白色沉淀并有气泡产生,A烧杯中无色酚酞溶液变成_____色。确定淡黄色固体中含有氮元素,理论依据是_____。
(实验二)将实验一中的白色沉淀分离、洗涤后加入稀盐酸,沉淀溶解,在老师的指导下进一步确定白色沉淀为氢氧化镁。写出沉淀溶解过程中发生反应的化学方程式_____。
(推理)已知氮化镁与水反应过程中没有元素化合价的改变,试写出氮化镁的化学式_____。
(讨论交流)(1)同学们都知道空气中氮气与氧气的体积比,图2实验中生成的氧化镁却远多于氮化镁,请你解释其原因_____。
(2)镁条在空气中久置表面会变黑,欲进一步证明镁条表面的黑色物质中含有碳酸盐,所需的试剂是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com