
【题目】人类的生活和生产离不开金属,我们要合理的利用开发金属及其矿物资源。
(1)请你写出赤铁矿(主要成分Fe2O3)为原料炼铁的化学方程式为_____
(2)如图是镓在元素周期表中的部分信息,则镓的相对原子质量是_____
![]()
(3)金属资源的储量有限,而且不能再生,因此要加强废旧金属的回收。回收废旧手机中的金属材料的意义是_____(答一点即可)
科目:初中化学 来源: 题型:
【题目】在“宏观-------微观--------符号” 之间建立联系,是化学学科特有的思维方式。以下是某化学反应的微观示意图:
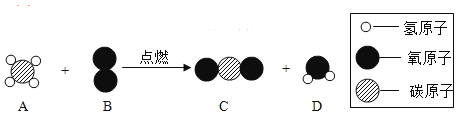
请回答以下问题:
(1)该反应前后涉及的化合物共有______种。
(2)分析微观示意图,你能获得的信息还有(各写一条):
宏观方面:______________________________;
微观方面:______________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知FeCl3也可以催化H2O2的分解,现向一定量的H2O2溶液中滴入几滴一定溶质质量分数的FeCl3溶液,充分反应(忽略水的挥发).下列图象正确的是( )
A. 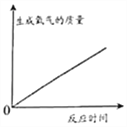 B.
B. 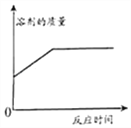
C. 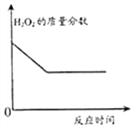 D.
D. 
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】日常生活中接触的金属材料,大多属于合金。其中黄铜是以锌作主要添加元素的铜合金。已知组成某弹壳的黄铜中只含有锌和铜,现将22g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示。试计算:
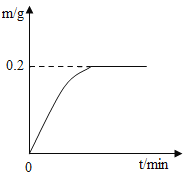
(1)实验室中将100g溶质质量分数98%的浓硫酸,加水稀释成19.6%的稀硫酸,加水的质量是_____。
(2)弹壳中铜的质量(写出解题过程)。
(3)实验过程中将弹壳粉碎的目的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组的同学准备进行常见酸、碱盐的性质实验时,发现实验台上摆放的药品中,有一瓶装有溶液的试剂瓶未盖瓶盖且标签破损(如图所示),于是决定对这瓶溶液进行实验探究。
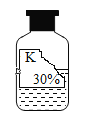
[提出问题]这瓶试剂可能是什么溶液呢?
[查阅资料]
I.初中化学常见的含钾化合物有KCl、KOH、K2CO3、KHCO3。
II. K2CO3和KHCO3溶液都呈碱性。
III.20℃时,测得四种物质的溶解度数据如下:
物质 | KCl | KOH | K2CO3 | KHCO3 |
溶解度/g | 34 | 112 | 111 | 33.7 |
[初步探究]小山根据试剂瓶标注的溶质质量分数30%和上表中的溶解度数据判断,这瓶试剂不可能是__________,理由是_________________。
[做出猜想]试剂瓶中溶液的溶质可能是①KOH;②K2CO3;③…….
[设计实验]小西取待测液于试管中滴加氢氧化钙溶液,观察到有白色沉淀产生,由此他认为猜想②正确。
[反思评价]小强不完全认同小西的结论,理由是______________。他另取样品,进行了如下实验:
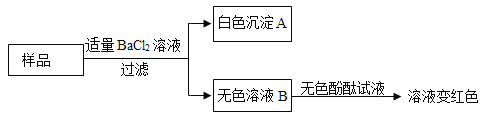
生成白色沉淀A的化学方程式为____________;通过实验可以判断样品中含有的溶质有_____________。
[得出结论]原瓶中的溶质是___________,且已变质。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学方程式书写正确的是( )
A.Fe+2AgNO3═Fe(NO3)2+2AgB.2NaOH+K2CO3═2KOH+Na2CO3
C.2H2O2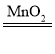 2H2↑+O2↑D.Fe2O3+2H2SO4═2FeSO4+2H2O
2H2↑+O2↑D.Fe2O3+2H2SO4═2FeSO4+2H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是甲、乙两种固体物质的溶解度曲线,回答下列问题:
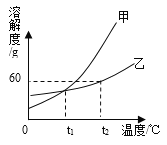
(1)p点的含义____________________________。
(2)若甲中含有少量的乙,则提纯甲可以采用的方法是___________。
(3)t2℃时,把50g乙物质放入50g水中,充分搅拌,所得溶液质量是_____g。
(4)t2℃时,配制等质量的甲乙两种饱和溶液需要水的质量:甲____乙(>;<;=)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】计算题:.将一定质量金属Mg和稀盐酸恰好完全反应,产生气体的质量0.4g。
(1)反应后溶液中溶质MgCl2 的质量为_____g。
(2)向反应后的溶液中逐滴加入NaOH 溶液,当加入的NaOH 溶液质量为40g 时,恰好完全反应,此时生成沉淀的质量为_____g。
(3)计算所加NaOH 溶液的溶质质量分数是多少?_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示为实验室常见气体制备、净化、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。某学校两个化学实验探究小组的同学欲用他们完成各自的探究实验。
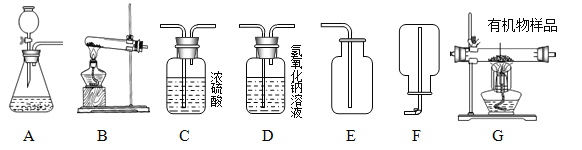
(1)甲组同学以锌粒和稀盐酸为原料制取氢气,因盐酸挥发出少量的氯化氢气体,导致制取的气体不纯,现欲制备并收集一瓶比较干燥、纯净的氢气,回答下列问题:
①所选仪器的连接顺序为 。
②反应装置中生成氢气的化学方程式 。
③锌与稀盐酸混合后,随着反应的进行,溶液的质量将 。(填 “增大”“减小”“不变” “无法判断”之一)
(2)乙组的同学以过氧化氢溶液为原料(MnO2为催化剂)制备氧气,并对某有机物固体样品(CxHy)的组成进行分析探究,所选仪器按“A→C1→G→C2→D→碱石灰干燥管”的顺序连接,(C1,C2为浓硫酸洗气瓶),实验前检验装置气密性,所设计的实验装置中气体流向是从左向右。使该有机物固体样品在纯氧气中充分燃烧,观察现象,收集有关实验数据,试回答下列问题:
①仪器A中所发生反应的化学方程式为: 。
②若装置中没有连接仪器C1,利用C2反应前后的质量变化测算出的该有机物样品中氢元素的质量与实际值比较将 (填“偏小”“偏大”“基本一致”之一)。
③仪器G的玻璃管中放入一定质量的有机物固体样品,有机物样品充分燃烧后,测得仪器C2质量增加ag,仪器D质量增加bg,则试推算该有机物样品(CxHy)的化学式中x、y的比值:x/y=__________.(用含a和b的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com