
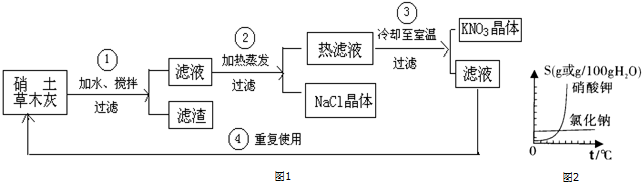
���� ��1�����ݸ��ֽⷴӦ�����������������е�����þ������ƿ����ľ̿����Ҫ�ɷ�̼��ط�����Ӧ������̼��þ��̼��Ƴ���������أ�
��2�������Ƿ����Һ�����ij��õIJ����������ò�����ɵõ���Һ������������Ϲ�����Ҫ������������
��3����ȴ�����¹����У��ȵ�����ر�����Һ��������ʱ�����в���������ܽ�����Һ�У����ٴβ�����ȡ����أ���������ص���ȡ��
��4�������ܽ������ͼ����ȷ�������ʵ��ܽ�����¶�Ӱ��IJ�ͬ���������������������������������ᾧ�õ�NaCl���壬������ȴ�ᾧ�õ�KNO3�����ԭ��
��� �⣺��1�������е�����þ���ľ����Ҫ�ɷ�̼��ط�Ӧ������̼��þ����������أ���ѧ����ʽΪMg��NO3��2+K2CO3�TMgCO3��+2KNO3��
��2�����ݲ���٢ڢ���ɺ�õ���Һ�����������������жϲ���aΪ���˲�������Ҫ�IJ����������ձ�����������©����
��3�����½ᾧ������������Һ��Ϊ�����ʵı�����Һ����ˣ���Һ�л����н϶������أ�ͨ���ٴβ����ɼ����������ؾ��壻
��4�������ܽ������ͼ���Ȼ��Ƶ��ܽ�����¶�Ӱ�첻���ڻ���Ȼ��ƾ���ʱӦ��ȡ�����ᾧ�ķ�����������ص��ܽ�����¶ȸı�仯�ϴ�ȡ���½ᾧ�������ؾ����Ϊ���㣻
�ʴ�Ϊ����1��Mg��NO3��2+K2CO3�TMgCO3��+2KNO3����2����������©������3����Һ�к��н϶��K2CO3�������ظ�������Һ�е�K2CO3����Լԭ�ϣ���
��4��NaCl���ܽ�����¶ȱ仯Ӱ���С��KNO3���ܽ�����¶ȱ仯Ӱ��ϴ�
���� ��������ͼ�����������Ͳ�ľ����ԭ������ȡ����ص���Ҫ�������̣���ȷ�������漰�IJ����ͷ����ķ�Ӧ�����˽�������һ���˼��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
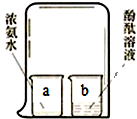 ��ͼ��ʾ����a�ձ���ʢ�з�̪��Һ����b�ձ���ʢ��Ũ��ˮ���й�����ͽ�����ȷ���ǣ�������
��ͼ��ʾ����a�ձ���ʢ�з�̪��Һ����b�ձ���ʢ��Ũ��ˮ���й�����ͽ�����ȷ���ǣ�������| ѡ�� | ���� | ���� |
| A | a�ձ���Һ���ɫ | b�з�̪�����˶���a�� |
| B | a�ձ���Һ���ɫ | a�а������˶���b�� |
| C | b�ձ���ҺΪ��ɫ | a�а������˶���b�� |
| D | b�ձ���ҺΪ��ɫ | b�з�̪����û�˶� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ǵ�ľ���ֱ�����ƿ�� | B�� | ������ֱ�ͨ�����ʯ��ˮ | ||
| C�� | ������ͨ�����ȵ�����ͭ | D�� | ��ȼ�ŵ�ľ���ֱ�����ƿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com