
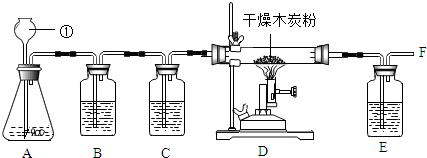
分析 (1)根据实验室常用仪器解答
(2)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳书写化学方程式;
(3)根据碳酸氢钠溶液和浓硫酸的吸水性分析;
(4)根据若F处的气体能点燃并产生了使石灰水变浑浊的气体进行分析,
(5)检验二氧化碳要用澄清石灰水,检验一氧化碳根据其燃烧后的生成物.
解答 解:(1)根据实验室常用仪器可知:①长颈漏斗;
(2)石灰石中的主要成分碳酸钙与稀盐酸反应生成氯化钙,水和二氧化碳,反应的化学方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)B中装有饱和碳酸氢钠溶液,其作用是除去CO2气体中混有的少量HCl气体;C中装有浓硫酸,浓硫酸有吸水性,其作用是吸水作干燥剂.
(4)若F处的气体能点燃并产生了使石灰水变浑浊的气体,则CO2在高温条件下与木炭反应生成了CO.
(5)二氧化锰和过氧化氢溶液混合生成O2,反应的化学方程式为 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.碳和氧气充分反应生成二氧化碳,不充分反应生成一氧化碳,此时要检验该实验条件下D中木炭所发生反应的生成物,还需要补充和完善的实验是 在D、E之间增加一个装有澄清石灰水的洗气瓶,石灰水变浑浊,则说明有二氧化碳生成;再在F出点燃气体,若产生蓝色火焰,且在火焰上方罩一内壁涂有石灰水的烧杯,石灰水变浑浊,则证明有CO生成
故答案为:
(1)长颈漏斗;
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)除去CO2气体中混有的少量HCl气体;浓硫酸;
(4)A;
(5)①2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
②在D、E之间增加一个装有澄清石灰水的洗气瓶,石灰水变浑浊,则说明有二氧化碳生成;再在F出点燃气体,若产生蓝色火焰,且在火焰上方罩一内壁涂有石灰水的烧杯,石灰水变浑浊,则证明有CO生成.
点评 本实验侧重考查学生的观察与思考能力,对碳以及碳的氧化物一些性质及气体的检验方法进行了考查,属于难度较大的题目.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用足量氢气还原氧化铜后留下的红色物质 | |
| B. | 盛放石灰水后留下的白色固体 | |
| C. | 氯化铁溶液与氢氧化钠溶液反应后留下的红褐色物质 | |
| D. | 用一氧化碳还原氧化铁后留下的黑色物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 把溶剂蒸发掉$\frac{1}{2}$ | B. | 加入7.5g硝酸钠固体 | ||
| C. | 把溶剂蒸发掉30g | D. | 加入20%的硝酸钠溶液30g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入适量的稀盐酸,塞上带导管的单孔塞,把导管插入另一试管里的石灰水中. | 有气体产生,气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后的试管中加少量品红溶液. | 品红溶液褪色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/mL | 反应所需时间/s |
| ① | 5 | 12 | 20 | 0.2 | 125 | 11 |
| ② | 30 | 12 | 20 | 0.2 | 125 | 2 |
| ③ | 30 | 12 | 40 | / | 125 | 148 |
| ④ | 30 | 12 | 90 | / | 125 | 82 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 春节期间农村大量燃放烟花爆竹,对空气质量没有影响 | |
| B. | 二氧化碳、臭氧都能造成温室效应 | |
| C. | 不规范的建筑施工会增加空气中PM2.5的含量 | |
| D. | 回收废旧电池不但节约金属资源,还可减少土壤污染 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com