
【题目】在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图。下列说法正确的是( )
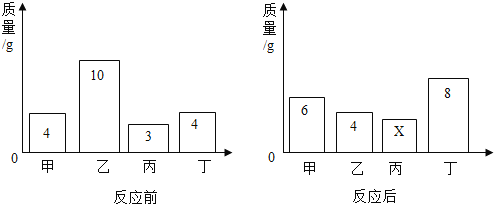
A.该反应为化合反应B.丙一定是该反应的催化剂
C.参加反应的乙、丁质量比3:2D.丁的相对分子质量是甲的2倍
科目:初中化学 来源: 题型:
【题目】请结合下图回答问题:
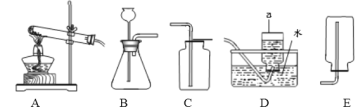
(1)标号a的仪器名称___________。
(2)实验室用氯酸钾和二氧化锰制取氧气的化学方程式为________,选用A、D装置制取O2,A装置中试管口略向下倾斜的原因是__________________,可用D装置收集O2的原因是__________________。
(3)写出实验室用大理石与稀盐酸反应制取二氧化碳的化学方程式________________________,用排空气法收集二氧化碳,可选用的收集装置为___________(填字母)。
(4)工业上可用煅烧石灰石制得二氧化碳,若要制取7.7t二氧化碳,需要含碳酸钙87.5%的石灰石质量是多少?(假设杂质不反应)___________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(7分)某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题。
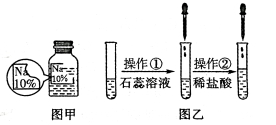
【猜想与假设】其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
【资料查阅】上述四种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
【探究过程】
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是 ;
在进行操作②时有无色无味得到气体产生,由此又可排除假设物质中的 。
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的 ,你的判断依据是 。
【探究反思】
(1)若上述探究结论是正确的,操作②产生的气体应是 (写化学式),实验室检验该气体的实验操作及现象是 。
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述表列信息。
请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图.下列说法中不正确的是( )
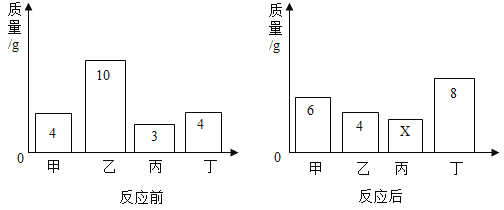
A.该反应为分解反应
B.丙可能为该反应的催化剂
C.反应中乙和丁的质量变化之比为3:2
D.丁相对分子质量是甲的2倍
查看答案和解析>>
科目:初中化学 来源: 题型:
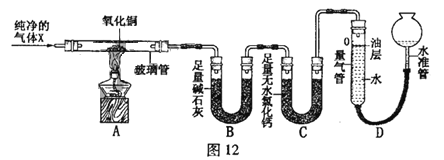
【题目】(10分)为探究气体X的组成,某兴趣小组进行图12所示实验(固定装置未画出)。
【资料在线】
(1)加热条件下,气体X能与氧化铜反应生成铜、水和氮气。
(2)碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应。
无水氯化钙可吸收气体X。
(3)本实验条件下,氮气密度为1.15g·L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计。
【实验步骤】
(1)连接仪器,并检查装置气密性。
(2)取一定量氧化铜,准确称得其质量为2.40g。
(3)按图12所示装入药品,测量并记录相关数据Ⅰ(见表1)。
(4)连接A、B、C装置, 将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热。当A装置中氧化铜反应完全,停止加热,继续通入气体 X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表1)。
【实验装置】
【相关数据】

【回答问题】
(1)B装置中氧化钙吸水的原理为 (用化学方程式表示)。
(2)实验过程中,当观察到 ,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是 。
(3)分析实验测量的数据,生成水的质量为 g,氧化铜中氧元素的质量为 g。
由此推知,气体X中一定 (填“有”或 “没有”)氧元素。
(4)通过计算推导出气体X的化学式。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室要配制一定溶质质量分数的氯化钠溶液。
(1)用20.0g粗盐经过提纯后得到16.0g精盐,则精盐的产率为__________。
(2)若用上述精盐来配制15%的氯化钠溶液,其中操作错误的步骤是__________(填选项)。
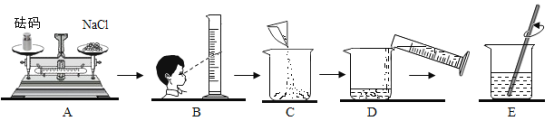
(3)E中玻璃棒的作用是__________。
(4)经检测,小强配制的溶液溶质质量分数偏小,其原因可能是__________(填选项)。
a.氯化钠固体不纯 b.装瓶时,有少量溶液洒出 c.量取水时,仰视读数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在靠近粉笔的粗端滴上一滴蓝墨水,然后将粉笔插入盛有酒精的容器中。一段时问后发现随着酒精沿粉笔上升,蓝墨水也在粉笔上不断移动,最后在粉笔上分为两个区域,上半部分是浅蓝色,下半部分是紫色(如图所示)。根据上述现象判断,下列说法错误的是:

A.蓝墨水是一种混合物
B.相同条件下不同分子运动速率不同
C.颜色改变是因为墨水中物质互相反应了
D.该实验原理可用于分离某些混合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】孔雀石是冶炼金属铜的主要原料,其主要成分是Cu2(OH)2CO3〔可看成是Cu(OH)2CuCO3〕,还含少量氧化铁和二氧化硅(不溶于水,也不与酸反应).以下为“湿法炼铜”并制备其它副产品氯化钠和铁红(氧化铁)的工业流程.
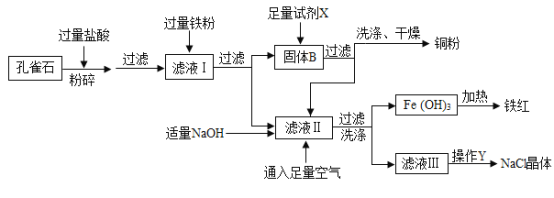
资料:
①Cu2(OH)2CO3与盐酸反应生成氯化铜、水和二氧化碳气体;
②铁能与氯化铁溶液反应,反应方程式为2FeCl3+Fe=3FeCl2
③氢氧化亚铁易被氧气氧化,反应方程式为4Fe(OH)2+2H2O+O2═4Fe(OH)3
回答下列问题:
(1)实验室在获取NaCl晶体的操作Y中,使用的仪器有:铁架台、玻璃棒、酒精灯、___;
(2)写出盐酸与Cu2(OH)2CO3反应的化学方程式:_______________________________;
(3)在滤液Ⅰ中加入过量铁粉,搅拌至充分反应,其中发生的置换反应有______个;
(4)滤液Ⅱ的溶质为:_______________________; 试剂X 是________________;
(5)在洗涤、干燥获取铜粉时,洗涤的目的是_____________________________________
(6)孔雀石也可以制取CuSO4·xH2O,现测定硫酸铜晶体(CuSO4·xH2O)中结晶水的x值:称取2.4g硫酸铜晶体,加热会使结晶水失去,当加热至质量不再改变时,称量粉末的质量为1.6g。则计算得x=______(计算结果精确到0.1)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小颖同学将铁粉投入硫酸铜溶液中时,发现生成红色固体的同时有较多的气泡放出,小颖对产生气泡的现象提出疑问,邀请兴趣小组的同学们展开了如下探究实验。
(提出问题)产生的气体是什么呢?
(作出猜想)兴趣小组的同学分别作出了如下猜想:小军的猜想:O2;小红的猜想:SO2;小颖的猜想:H2;小伟的猜想:N2。
(交流讨论)同学们经过讨论一致认为小伟的猜想不正确,依据是_____。
(查阅资料)SO2具有刺激性气味,易溶于水,能与NaOH溶液发生反应生成Na2SO3和水。
(实验探究)同学们收集气体,并分别对各自的猜想进行验证。
实验操作 | 实验现象 | 实验结论 | |
小军 | 将带火星的木条伸入到收集的气体中 | _____ | 猜想不正确 |
小红 | 将产生的气体通入盛有NaOH溶液的洗气瓶中,称量质量 | 通气前后洗气瓶的质量不变 | 猜想_____(填“正确”或“不正确”) |
小颖 | 将产生的气体用尖嘴玻璃管导出后点燃,并用冷而干燥的烧杯罩在火焰的上方 | 气体燃烧,产生淡蓝色火焰,烧杯内壁_____ | 猜想正确 |
写出小颖实验中发生反应的化学方程式_____。
(评价与改进)
(1)小红认为小军和小颖的实验方案都存在安全隐患,理由是_____。
(2)实验结束后,老师认为不需要进行实验即可通过更简便的方法验证小红的猜想,你认为所选择更为简便方法的依据是_____。
(拓展与延伸)
(1)由实验探究推测,可知硫酸铜溶液中可能含有呈酸性的物质,一般不用紫色石蕊溶液检验硫酸铜溶液酸碱性的原因是_____。
(2)据老师介绍,CuSO4可做催化剂,能加快过氧化氢的分解速率。为了验证老师的说法,需要进行的探究内容有:①是否能加快过氧化氢的分解;②_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com