
分析 (1)根据金属的物理性质进行分析;
(2)根据合金的性质比组成其纯金属的性质优良进行分析;
(3)根据锌会与硝酸铜、硝酸亚铁反应生成硝酸锌、铜、铁进行分析;
解答 解:(1)铝块能制成铝箔是利用了铝的延展性;
(2)黄铜是铜锌合金,其硬度比纯铜大;
(3)由于金属的活动性大小是:锌>铁>铜,将一定质量的锌粒投入含有Cu(NO3)2和Fe(NO3)2的混合溶液中,锌先与硝酸铜反应生成了硝酸锌和铜,当硝酸铜完全反应后锌再与硝酸亚铁反应生成了硝酸锌和铁,充分反应后过滤,若滤液中只含一种溶质,应该是硝酸锌,所以滤渣中一定含有铜、铁;发生反应的化学方程式是:Zn+Cu(NO3)2═Zn (NO3)2+Cu (或Zn+Fe(NO3)2═Zn (NO3)2+Fe).
故答为:(1)延展; (2)大; (3)铜、铁;(3)Zn+Cu(NO3)2═Zn (NO3)2+Cu (或Zn+Fe(NO3)2═Zn (NO3)2+Fe).
点评 活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快;化合价相同的等质量金属完全反应放出氢气的质量与金属的相对原子质量成反比,据此结合图象细心分析解答.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
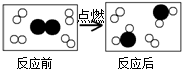 如图是某个化学反应前后各种物质的微观模拟图,图中“
如图是某个化学反应前后各种物质的微观模拟图,图中“ ”表示氢原子、“
”表示氢原子、“ ”表示氧原子,请写出该反应的化学方程式:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
”表示氧原子,请写出该反应的化学方程式:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | a处 | B. | c处 | C. | d处 | D. | e处 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化合物是由不同种元素组成的纯净物,所以只含一种元素的物质一定不是化合物 | |
| B. | 在同一化合物中,金属元素显正价,所以非金属元素一定显负价 | |
| C. | 分子由原子构成,所以分子的质量和体积一定比原子的质量和体积大 | |
| D. | 溶液中有晶体析出时,溶质质量减少,所以溶液的溶质质量分数一定减少 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A.解释说明 | B.安全常识 |
| ①氮气作粮食的保护气--化学性质稳定 ②CO、CO2化学性质不同--分子结构不同 | ①长时间堆放的柴草--要定期翻动 ②进入陌生的溶洞前--先做灯火实验 |
| C.燃烧与灭火 | D.方程式表示所述内容 |
| ①木柴架空有利于木柴的完全燃烧 ②用水灭火降低了可燃物着火点 | ①酸雨形成CO2+H2O═H2CO3 ②治疗胃酸过多 Al(OH)3+3HCl═AlCl3+3H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com