
| A、6克 | B、8 克 |
| C、12克 | D、4克 |
 小题狂做系列答案
小题狂做系列答案科目:初中化学 来源: 题型:
 |
 |
 |
 |
| A.植物油 | B.蔬菜 | C.米饭 | D.牛奶 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、用米汤检验食用加碘盐中是否含碘元素 |
| B、用食醋鉴别食盐和纯碱 |
| C、用洗洁精溶解餐具上的油污 |
| D、用明矾鉴别软水和硬水 |
查看答案和解析>>
科目:初中化学 来源: 题型:
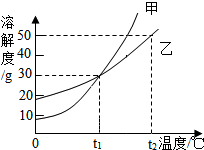
| A、t1℃时,甲和乙的溶解度均为30 |
| B、t1℃时,甲和乙的饱和溶液中溶质质量一定相等 |
| C、t2℃时,分别在100g水中各溶解20g甲、乙,降温后,乙溶液的溶质质量分数可能会大于甲溶液的溶质质量分数 |
| D、t2℃时,在100g水中放入60g乙,其溶质的质量分数为37.5% |
查看答案和解析>>
科目:初中化学 来源: 题型:

| A、它们表示四种不同的元素 |
| B、①④表示的是阳离子 |
| C、③表示的元素是非金属元素 |
| D、②表示的元素在化合物中通常显-2价 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
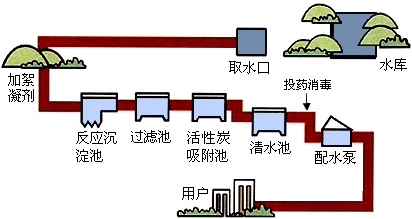
查看答案和解析>>
科目:初中化学 来源: 题型:
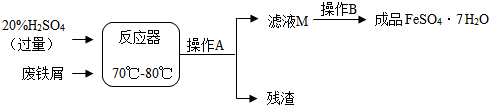
查看答案和解析>>
科目:初中化学 来源: 题型:
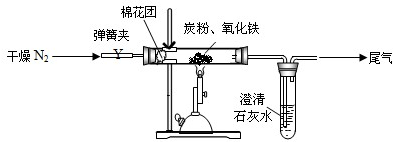
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com