
 分别称取36gNaCl、KNO3固体放入两只烧杯中,在20℃时分别加入100g水,充分搅拌后,有如图所示现象,请结合溶解度表,判断下列说法不正确的是( )
分别称取36gNaCl、KNO3固体放入两只烧杯中,在20℃时分别加入100g水,充分搅拌后,有如图所示现象,请结合溶解度表,判断下列说法不正确的是( )| 溶解度/g | 20℃ | 20℃ | 20℃ | 20℃ |
| NaCl | 35.8 | 36.0 | 36.6 | 37.3 |
| KNO3 | 20.9 | 31.6 | 63.9 | 110 |
| A. | 甲烧杯内为硝酸钾,乙烧杯内为氯化钠 | |
| B. | 甲烧杯内为饱和溶液,乙烧杯内为不饱和溶液 | |
| C. | 将温度升高40℃时,两溶液中溶质的质量分数相等 | |
| D. | 可用冷却热饱和溶液的方法得到大量的KNO3晶体 |
分析 根据20℃时两种物质的溶解度大小即可知道甲乙中所盛有的物质;升高到40℃时比较溶液中溶质质量大小即可比较溶质质量分数的大小,据此解答.
解答 解:分别称取36gNaCl、KNO3固体放入两只烧杯中,在20℃时分别加入100g水,充分搅拌后,甲中有剩余,说明甲中盛有的是硝酸钾,乙中盛有的是氯化钠;
A、甲烧杯内为硝酸钾,乙烧杯内为氯化钠,正确;
B、甲烧杯内是饱和溶液,乙烧杯内是饱和溶液,错误;
C、将温度升高40℃时,两溶液中溶质的质量相等,溶剂的质量相等,故溶质质量分数相等,正确;
D、硝酸钾的溶解度随温度的升高而增大变化明显,故可用冷却热饱和溶液的方法得到大量的KNO3晶体,正确;
故选B.
点评 本题考查了溶解度的应用,完成此题,可以依据溶解度的概念进行.


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 调查课题及内容 | 调查结论或建议 | |
| A | 使用塑料袋对环境的影响 | 减少使用并回收塑料袋,以减少污染、节约资源 |
| B | 周围人群的身体缺钙情况 | 每天服用补钙药品,而且多多益善 |
| C | 家庭用水现状 | 使用节水新技术,改变生活习惯,节约用水 |
| D | 本市一周空气质量状况 | 使用清洁能源,积极植树造林 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 洗洁精可使餐具上的油污乳化 | |
| B. | 汽油可溶解衣服上的油渍 | |
| C. | 水能洗去铁器上的铁锈 | |
| D. | 用稀盐酸可洗去试剂瓶内壁附着的碳酸钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
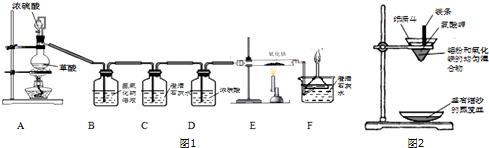
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 黑色粉末变成红色 固体部分溶解,有气泡产生,水溶液呈无色. | Zn和CuO能发生置换反应. |
| 实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 发生爆炸,黑色粉末变成红色. 固体部分溶解,有气泡产生,水溶液呈无色. | 镁与氧化铜发生了置换反应 |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热. | 粉末无变化 | Cu、Fe2O3不能反应. |
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸 | 200g | 150g | 150g |
| 加入的铁样品 | 9g | 9g | 14g |
| 烧杯+剩余物质质量 | 208.7g | 158.7g | 163.7g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 可以用同一套气体发生装置 | B. | 可以用同一种气体收集方法 | ||
| C. | 都需用到催化剂二氧化锰 | D. | 反应条件相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com