
| A、H2(HCl气体),先通过NaOH溶液,再通过浓硫酸 |
| B、NaOH溶液[Ca(OH)2溶液],先加入过量的Na2CO3溶液,再过滤 |
| C、CaCl2溶液(NaCl溶液),先加入适量的Na2CO3溶液,再过滤 |
| D、CaO固体(CaCO3固体),加入适量的稀盐酸 |


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| A、反应条件相同的是①③ |
| B、属于复分解反应的是③④ |
| C、属于有热量放出的反应的是①③④ |
| D、属于有元素化合价变化的是②④ |
查看答案和解析>>
科目:初中化学 来源: 题型:

| A、操作Ⅰ、Ⅱ、Ⅲ、Ⅳ都是过滤 |
| B、①中反应为:CaS04+2NH4HC03=CaC03↓+(NH4)2S04+H20+C02↑ |
| C、滤渣2可以循环利用 |
| D、反应④后需要热过滤的原因是加快过滤速率 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、不导电 | B、容易燃烧 |
| C、密度比空气大 | D、容易气化 |
查看答案和解析>>
科目:初中化学 来源: 题型:
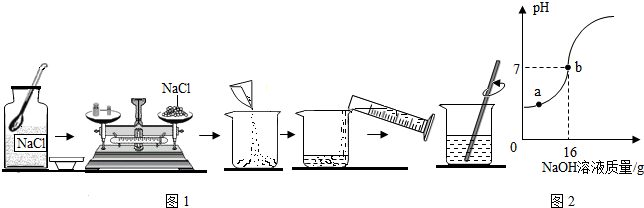
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com