
【题目】如图所示,进行中和反应实验:
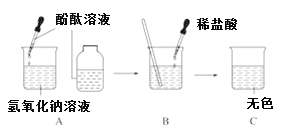
(1)在A的实验中,滴入酚酞溶液后,溶液由无色变为________色。
(2)写出C的溶液中溶质可能存在的几组情况____________________________。(用化学式表示)
(3)若73 g质量分数为20%的盐酸与127 g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数。__________
科目:初中化学 来源: 题型:
【题目】往300g FeCl3、CuCl2的混合溶液中加入铁粉。已知反应的先后顺序和分别为:2FeCl3+Fe=3FeCl2、CuCl2+Fe=FeCl2+Cu.如图为加入铁粉的质量与反应后剩余固体质量关系。则下列说法不正确的是( )
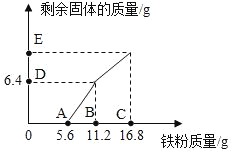
A. 点E对应纵坐标为12.0
B. 该 300g 溶液中的 CuCl2质量分数为6.75%
C. B 点后溶液的颜色为浅绿色
D. 取 DE 两点间的剩余固体加入盐酸,均有气泡产生
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室里常用大理石与稀盐酸反应来制取二氧化碳,某同学认真研究了课本中的实验装置(如下图甲),对其中的气体发生装置进行了改进(如下图乙)。请回答下列问题:
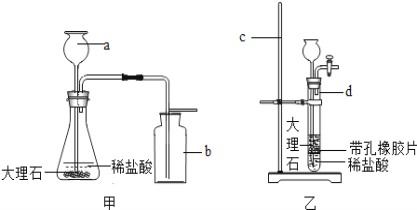
(1)写出实验室制取二氧化碳的化学反应方程式_____;
(2)写出标号仪器的名称:a_____,b_____,c_____,d_____;
(3)说明该同学进行实验装置改进的目的_____;
(4)写出检验b中已集满二氧化碳气体的方法_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上以高纯度的二氧化锰为原料制备高锰酸钾的主要流程如下:

已知相关物质的溶解度(20℃)如下表:
物质 | K2CO3 | K2SO4 | KMnO4 |
溶解度/g | 111 | 11.1 | 6.34 |
(1)KMnO4中锰元素的化合价为_____.
(2)操作I的名称是_____.“干燥”过程中温度不宜过高的原因是_____(用化学方程式表示).
(3)“通CO2酸化”,反应的化学方程式为:3K2 MnO4+2CO2═2KMnO4+MnO2↓+2K2CO3;不用稀H2SO4酸化,反应的化学方程式为:3K2 MNO4+2H2SO4═2KMnO4+MnO2↓+2K2SO4+2H2O;工业上不采用稀H2SO4酸化的原因是_____.
(4)电解法也可以实现由K2MnO4向KMnO4的转化,反应的化学方程式为:2K2 MnO4+2H2O![]() 2KMnO4+2KOH+H2↑,与“通CO2酸化”相比,其优点是_____.
2KMnO4+2KOH+H2↑,与“通CO2酸化”相比,其优点是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】能源是人类社会发展的基础,化石燃料是目前人类应用最广泛的能源物质,请回答下列问题:
(1)石油除含有碳、氢元素外,还含有少量的硫、氮等.下列有关石油说法不正确是(___)
A. 石油属于化合物
B. 石油是不可再生资源
C. 石油不充分燃烧会生成一氧化碳、二氧化硫等有害气体
D. 石油分馏可以制得焦炭和煤焦油
(2)为减少污染、提高煤的利用率,可将其转化为可燃性气体,此过程可认为是碳在高温下与水的反应,其微观示意图如右所示:通过观察图你能获得的信息是(写出两条即可):
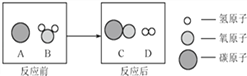
①__________________;②___________________.
(3)为减少CO2的排放,人们积极寻找不含碳元素的燃料,经研究发现NH3气在氧气中燃烧的产物没有污染,生成水和空气中含量最多的一种气体,且释放大量的热,有一定应用前景.则NH3在氧气中燃烧的化学方程式为_______________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题。
[猜想与假设]溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
[资料查阅]上述四种物质的相关信息如下:
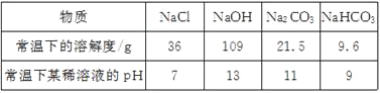
[探究过程]如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是________________________________________________________________________;在进行操作②时有无色无味的气体产生,由此又可排除假设物质中的____________。
[探究结论]你认为该溶液中的溶质可能是上述假设物质中的________,你的判断依据是________________________________________________________________________。
[探究反思](1)若上述探究结论是正确的,操作②产生的气体应是________(写化学式),实验室检验该气体的实验操作及现象是_________________________________________________。
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述表列信息.请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由:____________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习结晶时,同学们对硝酸钾的制备产生浓厚兴趣.
(一)通过查阅资料发现硝酸钾在农业市场用途十分广泛.工业上常采用硝酸钠与氯化钾在一定条件下反应制得硝酸钾和氯化钠.然后再利用硝酸钾和氯化钠在不同温度下的溶解度不同可将其分离,具体流程可以表示为:
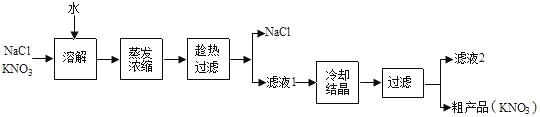
(1)溶解时需要不断搅拌,其目的是_____.
(2)化学实验室蒸发操作所需的玻璃仪器除玻璃棒外还有_____.
(3)分离氯化钠晶体和滤液1时需要趁热过滤的目的是_____.
(4)滤液1一定是_____的饱和溶液.
(5)冷却结晶后获得的硝酸钾晶体中还混有少量的NaCl,为获得更纯净的KNO3,还应进行的操作是洗涤、干燥,洗涤最佳的洗涤剂为_____.
A 常温下的蒸馏水 B 饱和的NaCl溶液 C 饱和的KNO3溶液
(6)洗涤后的液体应该_____.
A 不经处理直接排放到下水道
B 不经处理直接排放到农田
C 倒入原混合溶液中,节约资源并提高产率
(二)为测定洗涤前的粗产品中硝酸钾的质量分数,设计如下实验:取5g粗产品配成50g溶液,然后加入过量的硝酸银溶液(已知NaCl+AgNO3═AgCl↓+NaNO3,硝酸钾和硝酸银不反应),根据沉淀质量先求出NaCl质量,再确定硝酸钾的质量分数.
(7)硝酸银溶液需要过量的原因是_____,证明硝酸银已过量的方法是:静置后,在上层清液中加入硝酸银溶液,如果观察到_____(填有或无)沉淀生成,则已过量.
(8)在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液中的硝酸钾的质量分数_____(填偏大、偏小或无影响),对所测定的粗产品中硝酸钾的质量分数_____.(填偏大、偏小或无影响)
(9)经精确测定AgCl沉淀的质量为1.435g,则5g粗产品配成的50g溶液中NaCl的质量分数为_____;该粗产品中硝酸钾的质量分数_____.(写出计算过程,相关物质的相对分子质量:NaCl 58.5,AgCl 143.5).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现在,全国正在集中整治酒后驾驶违法行为,酒后驾驶对人民生命财产造成极大伤害.乙醇(俗名“酒精”) 会导致触觉能力、判断能力和操作能力降低、反应能力下降等.乙醇可以通过淀粉进行发酵蒸馏得到.已知乙醇的化学式为 C2H5OH,淀粉的化学式为(C6H10O5)n.试根据题意回答下列问题:
(1)淀粉属于_____(填“有机物”、“无机物”或“混合物”之一).
(2)乙 醇分子中 C、H、O 原子个数比为_____,氧元素的质量分数为_____(计算结果精确到 0.1%).
(3)喝 酒的人往往能闻到其浑身的酒味,这反映了分子的什么性质_____.
(4)欲检验某食物中是否含有淀粉,下列试剂中,最宜选用的是_____(填序号).
A 石蕊试液 B 氯化钠溶液 C 稀盐酸 D 碘水 E 氢氧化钠溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
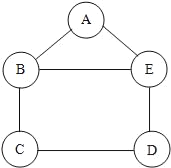
【题目】小吴用铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五中物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生反应。其中C物质的溶液呈蓝色,A与E 反应产生的气体是光合作用的原料之一。
(1)C物质是_____,A物质的用途是_____。
(2)D与E反应的化学方程式为_____,反应的基本类型是_____。
(3)B与E反应的现象为_____。
(4)B物质是_____,按游戏规则,下列能替代B物质的是_____(填序号)。
①银 ②氯化铁 ③氯化钡 ④氧化铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com