
【题目】为了研究物质的溶解现象,设计并进行了如下实验。
实验 |
① |
② |
③ |
现象 | 固体完全溶解, 形成紫色溶液 | 固体少量溶解, 形成浅黄色溶液 | 固体完全溶解, 形成棕色溶液 |
(1)设计实验①、②的目的是______。
(2)依据实验②、③的现象,可得出的结论是______。
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
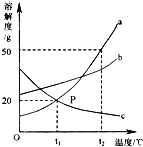
(1)P点的含义是_____.
(2)t1℃时a、b、c三种物质的溶解度按由小到大的顺序排列是_____.
(3)t1℃时30ga物质加入到50g水中不断搅拌,充分溶解并恢复到原温度后,得到溶液的质量为_____g.
(4)将t1℃时a、b、c三种物质的饱和溶液的温度升高到t2℃时,此时溶液中溶质质量分数的大小关系是_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。
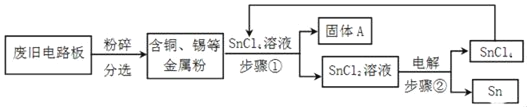
已知:Sn+SnCl4=2SnCl2
(1)SnCl4中锡元素的化合价是_____。
(2)铜的金属活动性比锡的_____(填“强”或“弱”),固体A中一定含有的金属元素是_____。
(3)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是_____(回答一点即可)。
(4)计算步骤②中电解380kgSnCl2理论上可以得到Sn的质量。_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小昊同学欲通过化学实验验证“质量守恒定律”,进行了下列实验探究。
(实验设计)根据实验目的,小昊确定以“铁和硫酸铜溶液”为研究对象,设计的实验装罝如图二所示。
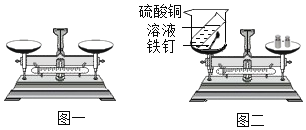
(进行实验)
实验步骤 | 实验现象与记录 | 解释或结论 |
①调零 |
| 如图一所示,调节平衡螺母天平无法平衡的原因是 _________; |
②称量铁钉的质量 | 记录称量数据为5.6g |
|
③称量硫酸铜溶液和烧杯的总质量 | 记录称量数据为113.2g |
|
④铁钉放入盛有硫酸铜溶液的烧杯中 | _____________________________________________ | 该反应的化学方程式为__________________________; |
⑤充分反应后,按如图二方式放好仪器和药品并称量 | 记录称量数据为_____________ | 该反应遵守质量守恒定律 |
(交流反思)(1)下列物质的溶液可以替代硫酸铜溶液直接利用图二装置完成上述实验的是______(填序号)。 A.硫酸铝 B.稀硫酸 C.硝酸银 D.乙醇
(2)实验结束后,过滤步骤⑤烧杯中的混合物,洗涤和干燥后称量固体的质量为5.8g,则该实验中生成铜的质量为___________g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣A组的同学们利用废硫酸液制备K2SO4,设计的流程如下图所示:
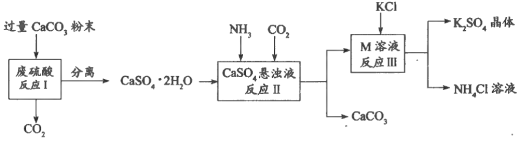
(1)写出反应Ⅰ的化学方程式:___________________________________________。
(2)反应Ⅱ生成了一种可用作氮肥的物质M,M的化学式为_________________。
(3)上述流程中可循环使用的物质有CO2和_____________________(填化学式)。
(4)反应Ⅲ中相关物质在25℃时的溶解度如下表。
物质 |
|
|
|
|
溶解度/g | 34.0 | 11.1 | 37.2 | 19.5 |
反应Ⅲ在常温下(25℃)能实现的原因是___________________________________。
(5)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是_____________;为了检验此晶体是否洗涤干净,常取最后一次洗涤液于试管中,先加入过量的_____________(选填字母),振荡、静置, 再向上层清液中滴加_____________(选填字母),观察现象即可判断该晶体是否洗涤干净。
A AgNO3溶液 B BaCl2溶液 C Ba(NO3)2溶液
D Ba(OH)2溶液 E NaOH溶液 F KOH溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属钨(W)可做白炽灯泡的灯丝。用黑钨矿(主要含FeWO4)制得金属钨的工艺流程如下图所示:
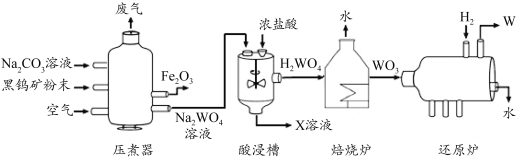
(1)将黑钨矿石碾成粉末,目的是______。
(2)酸浸槽中,Na2WO4溶液和浓盐酸发生复分解反应生,则X的化学式为______。
(3)还原炉中,发生反应的化学方程式为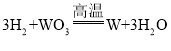 ,该反应中化合价改变的元素是______。
,该反应中化合价改变的元素是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】依据实验目的设计切实可行的实验方案是科学探究中的重要环节.
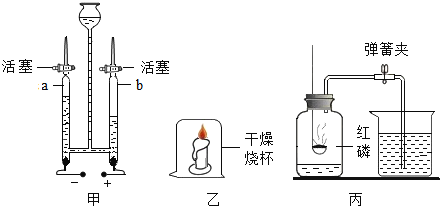
(1)用甲装置电解水. a管中收集到的气体是______,开启b管活塞,用燃着的木条接近b管尖嘴口观察到的现象是______.
(2)用乙装置进行探究实验,观察现象得出结论.
①蜡烛中含有氢元素,依据的现象是______;
②一段时间后蜡烛熄灭,由此得出可燃物燃烧必须具备的条件之一是______;
(3)用丙装置测定空气中氧气的含量,下列有关该实验的说法中,不正确的是______.
A 实验时红磷一定要足量 B 点燃红磷前先用弹簧夹夹紧橡皮管
C 燃烧匙中的红磷可以换成木炭 D 红磷熄灭并冷却后打开弹簧夹
E 最终进入瓶中水的体积约为消耗氧气的体积.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某密闭容器中有X、氧气、二氧化碳三种物质,在一定条件下充分反应,反应前后各物质质量的数据记录如下:
物质 | X | O2 | CO2 | H2O |
反应前的质量/g | 46 | 128 | 1 | 0 |
反应后的质量/g | 0 | 待测 | 89 | 54 |
在下列判断中,正确的是( )
A. 物质X由碳、氢元素组成 B. 物质X由碳、氢、氧元素组成
C. 充分反应后剩余氧气质量为16克 D. 生成CO2与H2O的质量比是89:54
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146 mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表
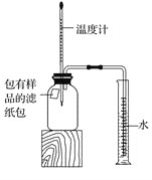
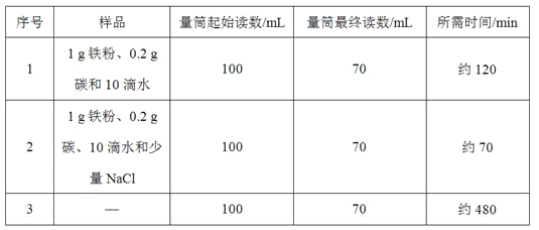
(1)实验①和②说明NaCl可以____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是______。
(4)已知碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成___。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是___(小数点后保留1位)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com