
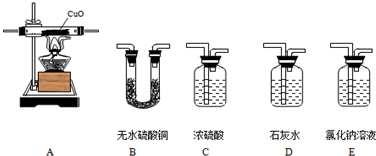
分析 根据无水硫酸铜遇水变蓝色,混合气通过氢氧化钙会携带水蒸气,检验水要放在检验二氧化碳的前面,混合气通过石灰水后,要用浓硫酸将水蒸气除去,防止对氢气的检验造成干扰等知识进行分析.
解答 解:(1)无水硫酸铜遇水变蓝色,混合气通过氢氧化钙会携带水蒸气,检验水要放在检验二氧化碳的前面,混合气通过石灰水后,要用浓硫酸将水蒸气除去,防止对氢气的检验造成干扰,然后再用无水硫酸铜检验水的生成,即混合气中是否含有氢气,所以设计的实验气体通过各装置的先后顺序是:BDCAB;
(2)二氧化碳和氢氧化钙反应生成碳酸钙沉淀,所以装置D的作用是:检验混合气中是否含有二氧化碳.
故答案为:(1)BDCAB;
(2)检验混合气中是否含有二氧化碳.
点评 本题考查装置的选择及连接,学生应注意利用物质的性质及气体在检验时的相互影响来分析解答.


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
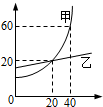 如图是甲、乙两种固体的溶解度曲线(横轴表示温度,纵轴表示溶解度),回答下列问题.
如图是甲、乙两种固体的溶解度曲线(横轴表示温度,纵轴表示溶解度),回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
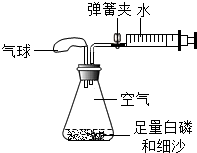 课外活动小组的同学们利用锥形瓶、注射器、白磷等仪器和药品,对“测定空气里氧气含量”进行了创新实验探究.
课外活动小组的同学们利用锥形瓶、注射器、白磷等仪器和药品,对“测定空气里氧气含量”进行了创新实验探究.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.生活常识 | B.健康问题 |
| 用洗洁精去除油污 用生石灰作干燥剂 | 用Al(OH)3治疗胃酸过多 用亚硝酸钠做调味品 |
| C.安全问题 | D.农业生产 |
| 氢气制取时要避免火种 加热液体时试管口不能对着人 | 用波尔多液杀菌 熟石灰改良酸性土壤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1、2 | B. | 2、3 | C. | 3、4 | D. | 2、1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com