
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:不详 题型:计算题
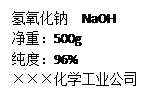
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
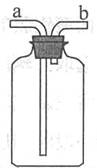
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
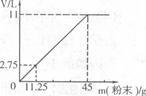
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| 正常情况下胃液中HCl的质量范围 | |
| 该患者胃液中HCl的质量 | |
| 该患者至少要除去的HCl的质量是 | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| 实验序号 | 1 | 2 | 3 | 4 |
| 生铁样品的质量/g | 2.88 | 5.76 | 9.24 | 10.28 |
| 生成H2的体积(标准状况下)/L | 1.12 | 2.24 | 3.36 | m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com