
| A. | NO | B. | NO2 | C. | N2 | D. | H2 |
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:初中化学 来源: 题型:解答题
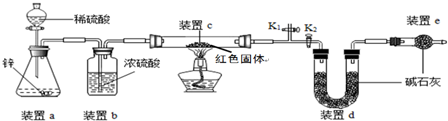
| 实验操作 | 实验现象 | 实验结论 |
| 取少量红色固体加入到足量稀硫酸溶液中 | 若无明显现象 | 假设1成立 |
| 若固体部分(选填“全部”或“部分”)溶解,溶液由无色变蓝色 | 假设2和假设3均成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 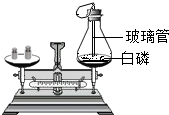 测量白磷燃烧前后质量变化值 | B. | 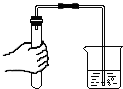 检查装置气密性 | ||
| C. | 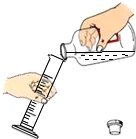 量取液体 | D. | 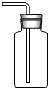 收集CO2气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 二氧化锰与氯酸钾的质量比 | 1:40 | 1:20 | 1:10 | 1:5 | 1:3 | 1:2 | 2:3 | 1:1 | 2:1 |
| 生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
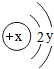
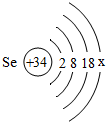 是硒的原子结构示意图,硒元素位于元素周期表的4周期、6主族.
是硒的原子结构示意图,硒元素位于元素周期表的4周期、6主族.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
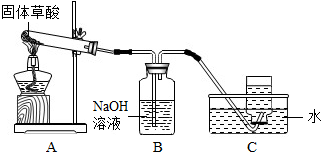 某化学课题小组通过查阅资料得知:固体草酸(H2C2O2•2H2O)受热可分解,其化学方程式(H2C2O2•2H2O═CO↑+CO2↑+3H2O)该课题小组的同学在实验室分别进行了如下实验,请回答下列问题:
某化学课题小组通过查阅资料得知:固体草酸(H2C2O2•2H2O)受热可分解,其化学方程式(H2C2O2•2H2O═CO↑+CO2↑+3H2O)该课题小组的同学在实验室分别进行了如下实验,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com