
����Ŀ����ͭ��п��ͭ�ĺϽ𣬿��������������������ճ���Ʒ��Ϊ�˲ⶨij��ĩ״��ͭ��Ʒ��п������������ȡ10g������Ʒ�����ձ��У��ٽ�40gϡ������Ĵμ��뵽���ձ��У�����ַ�Ӧ����õ�ʵ���������±���
ʵ����� | 1 | 2 | 3 | 4 |
ϡ��������� | 10g | 10g | 10g | 10g |
ʣ���������� | 8.7g | 7.4g | 6.7g | 6.7g |
�����������ݣ�����������⣺
��1���ڵ�_____��ʵ�����ʱ��Ʒ�е�п������ȫ��Ӧ��
��2������û�ͭ��Ʒ��п����������_____��
��3����������ϡ�����������������_____��
���𰸡�3 33% 14.6%
��������
���ݵ����κ͵��Ĵ�ʣ�����������ȿ�֪��ʣ���6.7g���弴Ϊ��Ʒ��ͭ���������ʵ�3��ʵ�����ʱ��Ʒ�е�п������ȫ��Ӧ���ɵ����κ͵��Ĵ�ʣ�����������ȿ�֪��ʣ���6.7g���弴Ϊ��Ʒ��ͭ����������п������Ϊ��Ʒ������ȥͭ���������ٸ���п����������Ʒ�����ȿɼ������ͭ��Ʒ��п���������������ݽ�����Կ�֪��ͭ�����������ϡ���ᷢ����Ӧ���ʷ�����Ӧ����п�����ٵĹ�����������Dzμӷ�Ӧ��п������������Ŀ��֪���ڶ��η�Ӧ����п��������8.7g��7.4g��1.3g�����ݷ�Ӧ�Ļ�ѧ����ʽ���ɼ��������10gϡ���������ʵ������������ʵ�����������ʽ���������ϡ���������ʵ�����������
��1���ɵ����κ͵��Ĵ�ʣ�����������ȿ�֪��ʣ���6.7g���弴Ϊ��Ʒ��ͭ���������ʵ�3��ʵ�����ʱ��Ʒ�е�п������ȫ��Ӧ��
��2���ɵ����κ͵��Ĵ�ʣ�����������ȿ�֪��ʣ���6.7g���弴Ϊ��Ʒ��ͭ����������п������Ϊ��Ʒ������ȥͭ����������Ϊ10g��6.7g��3.3g��
�ʻ�ͭ��п����������Ϊ��![]()
�𣺸û�ͭ��Ʒ��п����������33%��
��3�����ݽ�����Կ�֪��ͭ�����������ϡ���ᷢ����Ӧ���ʷ�����Ӧ����п�����ٵĹ�����������Dzμӷ�Ӧ��п������������Ŀ��֪���ڶ��η�Ӧ����п������Ϊ
8.7g��7.4g��1.3g
��ϡ���������ʵ�����Ϊx

![]()
x��1.46g
ϡ���������ʵ���������Ϊ![]()
������ϡ�������������Ϊ14.6%��


 ������״Ԫ��ҵϵ�д�
������״Ԫ��ҵϵ�д� ��ʱ�ƿ�������ϰϵ�д�
��ʱ�ƿ�������ϰϵ�д� һ��һ��һ��ͨϵ�д�
һ��һ��һ��ͨϵ�д� �㽭֮��ѧҵˮƽ����ϵ�д�
�㽭֮��ѧҵˮƽ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������װ�ý���ʵ�飬�����й�ʵ��ͽ�����ȷ����
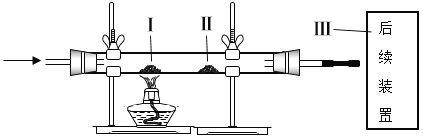
A. ����ͨ��N2���ټ��Ȣ�̼����泥��ɹ۲쵽��ɫʯ����ֽ�����ɫ
B. �Ȼ���ͨ��CO2���ټ��Ȣ�̿�ۣ�һ���۲쵽����������ĩ�ɺ�ɫ��ɺ�ɫ
C. �Ȼ���ͨ��������ټ��Ȣ��ף����ݢ�ȼ�ն����ײ�ȼ��˵����ȼ��ȼ��һ����Ҫ�������Ӵ�
D. �Ȼ���ͨ��������ټ��Ȣ�8.00 g��������Ʒ(��Ҫ�ɷ�ΪFeS2�����ʸ����²���Ӧ����Ӧ����ʽΪ��4FeS2 +11O2![]() 2Fe2O3+8SO2)����â�ʯ������6.40 g��������FeS2��= 75%
2Fe2O3+8SO2)����â�ʯ������6.40 g��������FeS2��= 75%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������зḻ��NaCl�����Դ��NaCl��һ����Ҫ�Ļ���ԭ�ϣ��������������ռ��������Ҫ�Ļ�����Ʒ��ij����������һ����NaClΪ��Ҫ�ɷֵ�ԭ�ϣ���������ȫ��ΪCaCl2��������Ա���ⶨԭ����NaCl�������������ȳ�ȡ60.0g��Ʒ��������ˮ����ܽ����������Һ�м���������������������Ϊ10����Na2CO3��Һ����ַ�Ӧ������2.0g��ɫ����������֪��CaCl2+Na2CO3===2NaCl+CaCO3����
�Իش��������⣨д��������̣���
��1��ԭ����NaCl�����������Ƕ���_____?
��2����ǡ����ȫ��Ӧʱ����Na2CO3��Һ�������Ƕ���_____?
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D����ѧ��ѧ���������ʣ������������о�����ͬһ��Ԫ�ء�����AΪ���ʣ�B��CΪ�������BΪ�ж����壬D��һ�ֽ������ϡ�����֮��IJ���ת����ϵ��ͼ��ʾ��ͼ�з�Ӧ���������ַ�Ӧ���������ʡ�ԣ�
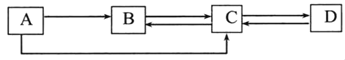
�ش�����
��1������B�Ļ�ѧʽΪ_____�������������е�Ӧ��_____��дһ����
��2������Bת��Ϊ����C�ķ�Ӧ�У�_____������һ��û��������������������һ���������������ɡ�����Cת��Ϊ����B���ù�����_____���������ȷ�Ӧ���������ȷ�Ӧ����
��3������B������C�Ļ�ѧ���ʲ�ͬ��������_____��
��4������Cת��Ϊ����D���÷�Ӧ�Ļ�ѧ����ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ǽס������ֹ������ʵ��ܽ�����ߡ�

��1��_____��ʱ���ס����������ʵ��ܽ����ȡ�
��2��t2��ʱ�����������ļס����������ʼ�ˮ�ܽ����Ƴɱ�����Һ��������Һ�����Ĵ�С��ϵΪ����_____�ң�����������������������������
��3���Ѽ����ʵIJ�������Һ��Ϊ������Һ�������й�˵����ȷ����_____������ţ���ͬ��
A �ܼ�������һ����С
B ���ʵ��������ܲ���
C ���ʵ���������һ�����
D ��Һ������һ�����
E �ñ�����Һ�������ܽ���������
��4���ڼ������л������������ʣ����Բ���_____�����ᴿ�����ʡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��С�ͻ��������Դ���ʹ���ʯΪ��Ҫԭ�ϣ������¹������������ռNaOH����
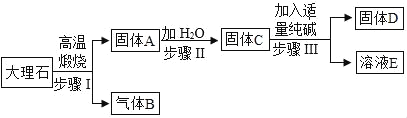
��1������C�Ļ�ѧʽ��_____û�ڲ������Ҫ���еķ��������_____��
��2��д�������Ļ�ѧ����ʽ_____��
��3��д�������Ļ�ѧ����ʽ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ϡ���������Դ������������ء�
��1���ճ���Ʒ�������ס�����������ֵ������������У���Ҫ���л��ϳɲ����Ƴɵ���__________
��2��Ϊ�˼���ȼ�ջ�ʯȼ�϶Ի�����Ӱ�죬����һ���濪����������Ч������Դ��______(дһ��)����һ�����ᳫ����̼�����������з�������̼����������������__________��(���������)��
�����ߵ��𣻢�����һ���Կ��ӣ��۶�ʹ�ÿյ������¶ȣ����ᳫ���У�����������
��3��Ŀǰ����ȼ�ϵ���Ѿ�������ɴ��Ⱥ�������ʵ��ʹ�ã����ܰ�������������Ӧ�Ļ�ѧ��ת��Ϊ____�ܣ�����ȼ�ϵ���ڷ�Ӧ�Ļ�ѧ����ʽ��____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͪ(C4H6O2)�����ǹ�����������й��ڶ���ͪ��˵������ȷ����( )
A. ����ͪ���ĸ�̼ԭ�ӡ�������ԭ�Ӻ�������ԭ�ӹ���
B. ����ͪ�к���������
C. ����ͪ����Ԫ�ص������������
D. ����ͪ����Ԫ�ص���������Ϊ6.98%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���ڣ������г����η��ϡ���̼���С����������һЩ�����˵�ϲ����

��1����ͨ���г��ķ�����Ҫ�ɷ���������ҵ����һ����̼�ͳ�������Ҫ�ɷ�����������ұ�����Ļ�ѧ����ʽΪ_____��
��2���ڽ���Ұ�����Ѽ�������֦�ܿգ�ʹ��ȼ�ո�����ԭ����_____��
��3���ڽ���Ұ�����á��������ס������Dz�����ѡ��������ʾ��Ԫ�ؾ��п�˥�ϡ����ư�ϸ���Ĺ��ܡ���Ԫ����Ԫ�����ڱ�������ͼ��ʾ��Ϣ�������й�˵������ȷ����_____������ĸ��ţ���
A �����ڽ���Ԫ��
B ����ԭ�Ӻ�����34������
C �������ԭ������Ϊ78.96g
D ��ԭ�ӵ�ԭ�Ӻ�����34������
��4����һЩ����ɨ�����г��ϵĶ�ά������á���������������ά�����������һ����PVC��PVC�Ļ�ѧʽΪ��C2H3Cl��n����PVC��̼Ԫ�غ���Ԫ�ص�������Ϊ_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com