
【题目】烧杯盛有一定质量的氢氧化钠和氢氧化钾的固体混合物,向其中加入100 g质量分数为7.3%的稀盐酸,恰好完全反应,得到109.6 g该温度下的不饱和溶液。则原固体混合物中金属元素的质量分数与下列数据最接近的是
A. 57.5% B. 64.6% C. 67.7% D. 69.6%
【答案】B
【解析】根据氢氧化钠和氢氧化钾与盐酸反应的化学方程式:NaOH+HCl![]() NaCl+H2O、KOH+HCl
NaCl+H2O、KOH+HCl![]() KCl+H2O以及质量守恒定律,可知氢氧化钠和氢氧化钾混合物的质量为109.6 g﹣100 g=9.6 g。根据酸碱中和反应的实质是OH-+H+
KCl+H2O以及质量守恒定律,可知氢氧化钠和氢氧化钾混合物的质量为109.6 g﹣100 g=9.6 g。根据酸碱中和反应的实质是OH-+H+![]() H2O,且氢氧化钠、氢氧化钾电离出的阴离子全是OH-,阳离子均为金属离子,求出氢氧根离子的质量,既能求出金属元素的质量。反应的氯化氢质量为100 g×7.3% =7.3 g,设反应中消耗氢氧根离子的质量为x。
H2O,且氢氧化钠、氢氧化钾电离出的阴离子全是OH-,阳离子均为金属离子,求出氢氧根离子的质量,既能求出金属元素的质量。反应的氯化氢质量为100 g×7.3% =7.3 g,设反应中消耗氢氧根离子的质量为x。
OH-~HCl~H2O
17 36.5
x 7.3 g
x=3.4 g
故钠元素和钾元素质量和为:9.6 g﹣3.4 g=6.2 g。则原固体混合物中金属元素的质量分数为![]() ×100%≈64.6%,故选B。
×100%≈64.6%,故选B。


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:初中化学 来源: 题型:
【题目】某学生测定的下列数据中不合理的是
A.用pH试纸测得某地水的pH为5.2
B.用10mL的量筒量取7.5mL的水
C.用托盘天平称得小苏打样品的质量为16.7 克
D.测得某粗盐中氯化钠的质量分数为90.5%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶未用完的长期敞口放置的氢氧化钠样品(不考虑水的存在),质量是9.3g,与一定质量分数的稀盐酸92.9g恰好完全反应,产生气体的质量为2.2g。试计算完全反应后所得溶液中溶质的质量分数。(写出具体计算过程)__________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某矿石主要成分是 MgO,含少量的 Fe2O3、CuO 和 SiO2 杂质。用该矿石制备 Mg(OH)2 的工艺流程简图如下, 回答下列问题:
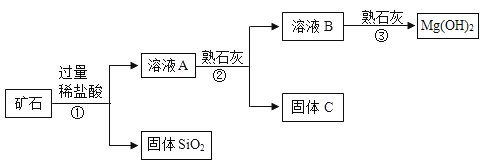
对应离子 | Fe3+ | Cu2+ | Mg2+ |
开始沉淀时的 pH | 1.9 | 4.2 | 9.1 |
完全沉淀时的 pH | 3.2 | 6.7 | 11.1 |
(1)步骤①和步骤②均用到的操作是_____;
(2)溶液 A 中所含的阳离子有 Fe3+、Cu2+、Mg2+和_____(填离子符号);
(3)已知部分金属阳离子以氢氧化物形式形成沉淀时溶液的 pH 如上表所示,则步骤②中加入熟石灰,调节溶液的 pH 范围为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下图回答问题:
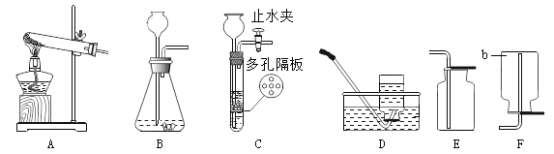
(1)用高锰酸钾制氧气,应选用的发生装置是_____(填字母序号),该反应的化学方程式为_____。
(2)常温下,用锌和稀硫酸反应制取氢气,若要随时控制反应的发生和停止,应选用的发生装置是_____(填字母序号),反应的化学方程式为 _____ ;点燃氢气前必须验纯, 为确保安全,最好选用装置 _____ (填字母序号)所示方法收集氢气。
(3)小涵通过观察发现纯锌粒与硫酸的反应明显比粗锌粒慢。通过查阅资料得知粗锌中含有一些不活泼金属,她猜想可能是粗锌中不活泼金属促进了锌与硫酸的反应。为了验证小涵的猜想,你认为应该在盛有纯锌粒和稀硫酸的试管中,加入少量的 _____溶液。
A 盐酸 B 氯化铜 C 氯化钠 D 氯化钙
(4)小川同学想通过用一定质量粗锌与足量的硫酸反应,测量生成氢气的体积来计算粗锌的纯度,于是设计了如图所示的实验装置。
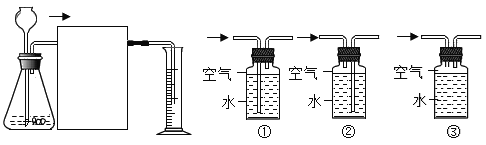
在实线框中应接入如图中的_____,广口瓶上方残留的空气_____(填“会”或“不会”)对氢气体积的测量造成影响。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钠的化合物在日常生活中有着广泛的应用。
(1)若将100g 9%的氯化钠溶液稀释为0.9%的氯化钠溶液,需要加入水的质量为____g。
(2)过氧化钠(Na2O2)和CO2反应,可以生成纯碱和氧气,所以可作为呼吸面具和潜水艇的供氧剂,请写出该反应的化学方程式:_______。
(3)《四川盐法志》记载,“敞锅熬盐”主要步骤为:①将黄卤和黑卤按比例混合;②放入敞口锅中加热浓缩,析出粗盐;③用“花水”冲洗粗盐得精品盐。请回答,步骤①中,黄卤所含杂质BaCl2和黑卤所含杂质MgSO4反应生成白色沉淀,该反应的化学方程式为________。步骤②中,析出粗盐的过程称为_______。步骤③用“花水”冲洗粗盐,既可除去表面的MgSO4和MgCl2杂质,又不损失NaCl.则“花水”应当是_____(填标号)
A蒸馏水 B饱和 NaCl溶液 C饱和NaOH溶液 D饱和BaCl2溶液
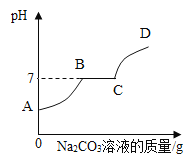
(4)某同学对实验室制取CO2后的剩余液体进行探究。首先向废液中滴加少量紫色石蕊试液,然后再逐滴加入Na2CO3溶液,溶液pH的变化如图所示。BC段的现象是______。向C点所示溶液中加入硝酸银溶液,发生反应的化学方程式________。
(5)食用纯碱中常含有少量的氯化钠。现取某食用纯碱样品10g,加入一定量的稀盐酸恰好完全反应,同时生成了3.3g气体。试计算该食用纯碱中Na2CO3的质量分数。_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质的性质和用途是化学的重要研究内容。
(1)浓硫酸具有吸水性,在实验室中常用它做 剂。
(2)用石灰浆粉刷墙壁,干燥后墙面就变硬了,用化学原理解释该现象。
(3)图中,用滤纸做成的小花喷洒某溶液后放在烧杯上方,片刻后变成红色。请推测喷洒液和烧杯中溶液可能是什么?(写出一组即可)
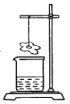
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】AE 为初中化学五种不同类别的常见物质。已知 C 含有三种元素,E 为世界年产量最高的金属,A 是相对分子质量为 160 的蓝色溶液。它们之间相互关系如图所示,图中“”表示相连的物质能相互反应,“→”表示种物质转化成另一种物质(部分反应物、生成物及反应条件已略去)。请回答下列问题:
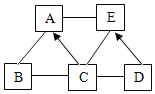
(1)物质 E 是_____。
(2)写出下列反应的化学方程式:A+E:__________;B+C:________________。
(3)图中相互关系涉及基本反应类型有_____种。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对久置于空气中的“生石灰”干燥剂的组成成分及含量进行探究
(查阅资料)Ca(OH)2加热到一定温度时会发生分解反应,生成两种氧化物。
(实验探究)该小组称取15.2g干燥剂样品于控温电加热器中,按如图所示装置进行实验(装置气密性良好,A、B、C中药品足量,实验操作正确)
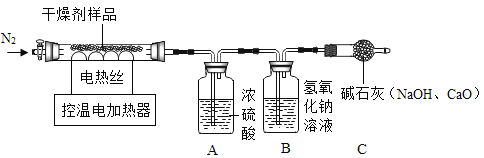
(数据记录)充分反应后,产物被完全吸收,A装置增重1.8g,B装置增重2.2g。
(分析结论)该包干燥剂的成分是_____(填化学式),
(数据处理)该15.2g干燥剂样品,若加入过量稀盐酸后,蒸发至干,得到氯化钙固体质量是_____g。
(反思拓展)①停止加热后,需要通入N2一段时间的目的是_____。
②若没有C装置,会导致含量测定结果偏小的成分是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com