
【题目】对久置于空气中的“生石灰”干燥剂的组成成分及含量进行探究
(查阅资料)Ca(OH)2加热到一定温度时会发生分解反应,生成两种氧化物。
(实验探究)该小组称取15.2g干燥剂样品于控温电加热器中,按如图所示装置进行实验(装置气密性良好,A、B、C中药品足量,实验操作正确)
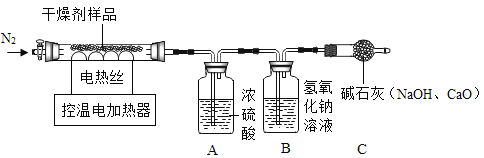
(数据记录)充分反应后,产物被完全吸收,A装置增重1.8g,B装置增重2.2g。
(分析结论)该包干燥剂的成分是_____(填化学式),
(数据处理)该15.2g干燥剂样品,若加入过量稀盐酸后,蒸发至干,得到氯化钙固体质量是_____g。
(反思拓展)①停止加热后,需要通入N2一段时间的目的是_____。
②若没有C装置,会导致含量测定结果偏小的成分是_____。
【答案】CaO、Ca(OH)2、CaCO3 22.2g 使反应生成的水、二氧化碳全部被浓硫酸、氢氧化钠溶液吸收 CaO
【解析】
生石灰久置于空气中,氧化钙能与空气中的水蒸气反应生成氢氧化钙,氢氧化钙能与空气中的二氧化碳反应生成碳酸钙,将干燥剂样品于控温电加热器中,充分反应后,产物被完全吸收,A装置增重1.8g,B装置增重2.2g,浓硫酸具有吸水性,A装置增重,说明干燥剂中含有氢氧化钙,Ca(OH)2加热到一定温度时会发生分解反应,生成氧化钙和水,B装置增重,说明生成了二氧化碳,说明干燥剂中含有碳酸钙,碳酸钙在加热的条件下分解生成了氧化钙和二氧化碳。
设该干燥剂样品中,氢氧化钙的质量为x
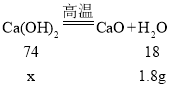
![]() x=7.4g
x=7.4g
设该干燥剂样品中,碳酸钙的质量为y
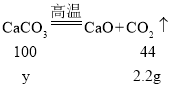
![]() y=5g
y=5g
故该干燥剂样品中还含有氧化钙,氧化钙的质量为:15.2g-7.4g-5g=2.8g,
故该包干燥剂的成分是:CaCO3、CaO、Ca(OH)2;
数据处理:向该干燥剂样品中加入过量稀盐酸,发生以下化学方程式:
![]()
![]() ,
,![]() ,由化学方程式可知,该干燥剂中的钙元素都转化到了氯化钙中。
,由化学方程式可知,该干燥剂中的钙元素都转化到了氯化钙中。
碳酸钙中钙元素的质量:
![]() ;
;
氧化钙中钙元素的质量:![]() ;
;
氢氧化钙中钙元素的质量:
![]() ;
;
得到氯化钙固体的质量为:
![]()
反思拓展:①停止加热后,需要通入N2一段时间的目的是:使反应生成的水、二氧化碳全部被浓硫酸、氢氧化钠溶液吸收;
②若没有C装置,空气中的二氧化碳会被氢氧化钠吸收,导致测定的二氧化碳质量偏大,从而碳酸钙的测定结果偏大,由于浓硫酸中吸收的水分含量不变,故氢氧化钙的测定值不变,从而导致氧化钙的测定结果偏小。


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:初中化学 来源: 题型:
【题目】烧杯盛有一定质量的氢氧化钠和氢氧化钾的固体混合物,向其中加入100 g质量分数为7.3%的稀盐酸,恰好完全反应,得到109.6 g该温度下的不饱和溶液。则原固体混合物中金属元素的质量分数与下列数据最接近的是
A. 57.5% B. 64.6% C. 67.7% D. 69.6%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示:
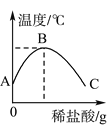
(1)由图可知,稀盐酸与氢氧化钠溶液发生的反应是________(填“放热”或“吸热”)反应。
(2)从A到B过程中,烧杯中溶液的pH逐渐________。
(3)______点时恰好完全反应,C点的溶液中含有的溶质为________。
(4)如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,
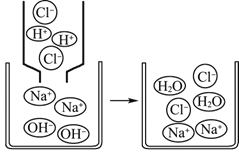
由此得出该反应的实质是____。写出另一个符合该反应实质的化学方程式______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业产品过氧化钙晶体(CaO2·8H2O)较稳定,呈白色,微溶于水,广泛用于环境杀菌、消毒。以贝壳(主要成分是 CaCO3,杂质不参加反应也不溶于水)为原料制备 CaO2的流程如下:
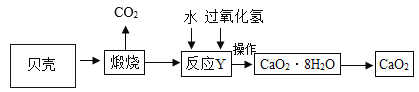
(1)CaO2中氧元素的化合价为___________;
(2)上述流程中将过氧化钙晶体从溶液中分离的步骤是过滤,该操作中用到的玻璃仪器有玻璃棒、 烧杯和_______________,其中玻璃棒的作用是_______________;
(3)反应 Y 需要在低温条件下进行,其原因是_________________;
(4)获取的 CaO2 中常含有 Ca(OH)2 杂质,原因是_______________(用化学方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合下列实验常用装置,回答有关问题。
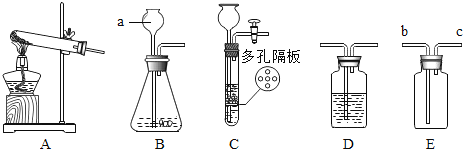
(1)图中标有字母的仪器的名称:a _____;
(2)实验室用高锰酸钾制取氧气,反应的化学方程式是_____。
(3)实验室制取氢气,反应的化学方程式是_____。
(4)实验室制取二氧化碳的反应方程式为_____;如果用E装置收集该气体,则气体从_____端进入(填“b”或“c”),若要用E装置验证二氧化碳能否与水反应,瓶中需装_____ ,且气体从_____端进入(填“b”或“c”)。
(5)实验室常用装置C代替装置B制取气体,该装置的优点是_____,下列反应适用于该装置的是_____(填序号) 。
a.大理石和稀盐酸 b.锌粒与稀硫酸 c. 过氧化氢溶液与二氧化锰粉末
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某市售某浓盐酸试剂瓶标签上的有关数据如图1所示。小张同学取5mL该浓盐酸加入锥形瓶中,加水稀释后,再逐滴滴加溶质质量分数为5%的NaOH溶液,反应过程中溶液的酸碱度变化如图2所示。
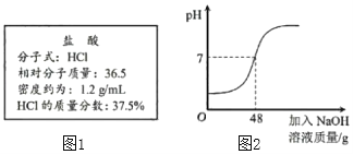
(1)小张同学所取的5mL浓盐酸的质量为_____克。
(2)通过计算,判断该浓盐酸中HCl的质量分数是否与试剂瓶标签上的数据相符_____(需要计算过程,计算结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向氢氧化钠溶液中滴入酚酞试液,可以看到溶液变______色,再向溶液中逐滴滴入稀盐酸,当观察到溶液变______色时,表明反应已经完成。反应的化学方程式是_____________,此时反应物的物质的量之比为_______,该反应属于______________反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在氢氧化钠溶液中加入 X 溶液并插入温度计,逐滴加入硫酸溶液,观察到红色褪去,温度计示数上升。证明碱与酸能发生反应,且放出热量。
(1)加入的 X 溶液应该是_____溶液;
(2)甲同学提出滴入的硫酸不能用浓硫酸,他的理由是_____;
(3)乙同学提出红色褪去不能说明酸和碱恰好反应完全,为了证明是否恰好反应,可取上述反应后的无色溶液少许加入_____即可(填序号)。
①铜 ②镁 ③氧化铜 ④BaCl2 溶液 ⑤Na2CO3 溶液
(4)若取10%的氢氧化钠溶液100g和10%的硫酸溶液100g混合后,加入紫色石蕊,则此时溶液呈_____色(填序号)。
①紫 ②红 ③蓝
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“舌尖上的化学”。以下是厨房中一些实物图。

(1)牛肉富含的营养物质是________。
(2)食用碘盐是为了预防___________疾病(填字母)。
a 贫血 b 甲状腺肿大 c 夜盲症
(3)为保障“舌尖上的安全”,下列做法合理的是_________ (填字母)
a 霉变大米蒸煮后食用
b 甲醛溶液浸泡虾仁防腐
c 适当使用食品添加剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com