
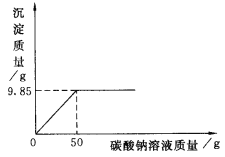
【题目】为了测定某化工厂由氯化钡和氯化钠组成的产品中氯化钠 的成分。小明取16.25g固体样品,全部溶于143.6g水中,向所得到的混合溶液中逐滴加入溶质质量分数为10.6%的碳酸钠溶液,记录如下图所示的曲线关系。
求:(1)产品中氯化钠的质量分数;
(2)当氯化钡与碳酸钠恰好完全反应时,所得溶液中
溶质的质量分数。
【答案】(1)36% (2)5.85%
【解析】
试题分析:在氯化钡和氯化钠的混合溶液中逐滴加入碳酸钠溶液,发生反应:BaCl2+Na2CO3==BaCO3↓+2NaCl;故结合图像可知:当加入的碳酸钠溶液质量为50g时,反应刚好结束,所得BaCO3沉淀质量为9.85g,
解:设样品中BaCl2的质量为x,生成NaCl的质量为y.
Na2CO3 + BaCl2 = BaCO3↓+2NaCl
106 208 117
50g×10.6% x y
(1)106:208= 50g×10.6%:x
x=10.4g
产品中NaCl的质量分数=(16.25g-10.4g)/16.25g×100%=36%
(2)106:117=50g×10.6%:y
y=5.85g
溶液中溶质NaCl的总质量=16.25g-10.4g+5.85g=11.7g
溶液的总质量=16.25g+143.6g+50g-9.85g=200g
所得溶液中溶质的质量分数=11.7g/200g×100%=5.85%
答:略


科目:初中化学 来源: 题型:
【题目】(10分)用化学符号或名称表示:
(1)一个铜原子 ;
(2)两个氮分子 ;
(3)三个钠离子 ;
(4)ZnCl2 ;
(5)+6价Cr的氧化物________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于水的叙述,错误的是
A、电解水时,与电源正极相连的玻璃管内得到的气体能在空气中燃烧
B、水是由氢元素和氧元素组成的
C、生活中通过煮沸可降低水的硬度
D、净化水的方法有吸附、沉淀、过滤和蒸馏等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用化学反应中气体产生的压力,可使多个化学反应依次发生。下图所示装置气密性良好,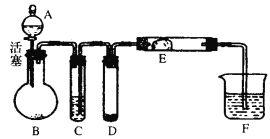
A~F各装置中盛放的物质分别为:
A.5%的双氧水;
B.二氧化锰;
C.足量某盐溶液;
D.能溶于水的固体;
E.浸有无色酚酞溶液的棉花;
F.足量稀硫酸。
将A中溶液加入B中,关闭活塞,多个反应依次发生,反应完毕,D中有白色沉淀,E中棉花呈红色。
(1)B中产生的气体是 (写化学式,下同);
(2)若向D中滴加过量的稀硝酸,沉淀不消失,则该沉淀是 。C、D中的原物质是:C 、D 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在载人宇宙飞船中,一般都安装盛放过氧化钠(Na2O2)颗粒的装置,它的作用是再生氧气,供宇航员呼吸,反应的化学方程式为2Na2O2+2CO2═2X+O2.则X的化学式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(7分)一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如下图所示。
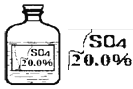
要求同学们进行探究:
确认这瓶溶液到底是什么溶液?
提出猜想:王老师提示:这瓶无色溶液只能是以下四种溶液中的一种:
①硫酸镁溶液、 ②硫酸钠溶液、
③硫酸溶液、 ④硫酸铵溶液。
查阅资料:
A:常温下,相关物质的溶解度如下
物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
溶解度 | 35.1g | 19.5g | 75.4g | 与水任意比互溶 |
B:(NH4)2SO4的水溶液显酸性
【实验探究】
(1)通过查阅资料,小明同学认为猜想 (填序号)不成立,原因是 。
(2)为确定其它几种猜想是否正确,小明同学继续进行探究:
实验步骤 | 实验现象 | 实验结论 |
a取该溶液少许于试管中,向其中滴加几滴氢氧化钠溶液 | 溶液中有白色沉淀生成 | 猜想①成立 |
b取该溶液少许于试管中,向其中滴加几滴紫色石蕊溶液 | 猜想③成立 |
小芳同学认为小明实验步骤b的结论不正确,她的理由是 ;
(3)请你设计实验方案,确认该溶液是硫酸铵溶液并完成实验报告:
实验操作 | 实验现象 | 实验结论 |
取该溶液少许于试管中,再往该溶液加入 溶液,加热。 | 猜想④成立,该反应的化学方程式为 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)黄铜矿(主要万分CuFeS2)经初步处理后,所得溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4。某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜。主要步骤如图所示:
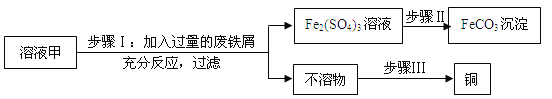
(1)Fe2(SO4)3与铁反应的化学方程式: x Fe2(SO4)3+ y Fe= z FeSO4,其中x、y、z为化学计量数,z的值为_____________。
(2)步骤Ⅰ中,生成铜的化学方程式:__________________________。
(3)步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是______________________。
(4)步骤Ⅱ中加入一种可溶性可实现其转化,从复分解反应发生的条件分析,该试剂可以是________。
(5)步骤Ⅲ回收铜的方法为___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(9分)现有工厂丢弃的废铜屑(铜屑表面呈绿色,其中混有少量生锈铁屑)。课外活动小组同学欲利用其制取胆矾,他们设计了下面的两种制取流程。
已知Cu+Fe2(SO4)3=2FeSO4+CuSO4 ,请回答:
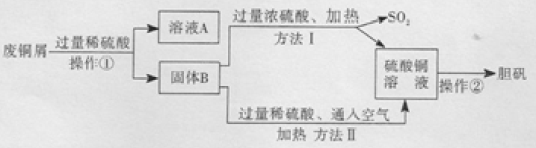
(1)铜屑表面呈绿色的物质化学式是Cu2(OH)2CO3,俗称 ,操作所用到的玻璃仪器有:烧杯、玻璃棒和 。
(2)溶液A的溶质有 (只写一种);铁锈与稀硫酸反应的化学方程式为: 。
(3)两种方法比较,符合绿色化学要求的是方法 ;方法II 的化学方程式为:
2Cu + 2H2SO4 + = 2CuSO4 +
操作②实验步骤为: ,
降温结晶。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com