
| A. | 食物的酶促褐变一定有酶的参与 | B. | 除去氧气可以防止食物酶促褐变 | ||
| C. | 温度越高去皮的山药越容易变褐色 | D. | 食物的酶促褐变属于化学变化 |
分析 经查阅资料后才知是与空气中的氧气化合变成了褐色,这种变化称为食物的酶促褐变,条件有:①氧的存在;②酶的作用;因此食物的酶促褐变一定有酶的参与;除去氧气可以防止食物酶促褐变正确;温度越高去皮的山药越容易变褐色错误,温度越高不易发生酶促褐变;食物的酶促褐变生成了新物质,属于化学变化.
解答 解:A、正经查阅资料后才知是与空气中的氧气化合变成了褐色,这种变化称为食物的酶促褐变,条件有:①氧的存在;②酶的作用;因此食物的酶促褐变一定有酶的参与,确但不符合题意,故选项错误;
B、酶促褐变的条件有:①氧的存在;②酶的作用;因此除去氧气可以防止食物酶促褐变正确,正确但不符合题意,故选项错误;
C、温度越高去皮的山药越容易变褐色错误,温度越高不易发生酶促褐变,错误符合题意,故选项正确;
D、食物的酶促褐变生成了新物质,属于化学变化,正确但不符合题意,故选项错误;
故选C
点评 本考点考查了酶促褐变的概念和条件.食品在现实生活中应用很广泛,应该好好把握.要合理膳食,均衡营养,保证身体健康.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
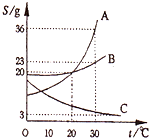 如图是物质 A、B、C在水中的溶解度曲线图,试回答:
如图是物质 A、B、C在水中的溶解度曲线图,试回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盐酸能与锌粒反应生成气体 | |
| B. | 稀硫酸能与氯化钡溶液反应生成白色沉淀 | |
| C. | 醋酸能除水垢(主要成分是碳酸钙) | |
| D. | 稀盐酸能除铁锈 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
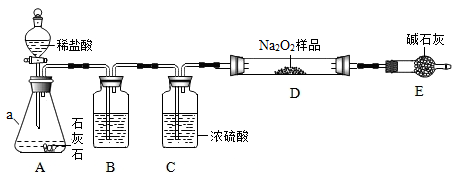
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
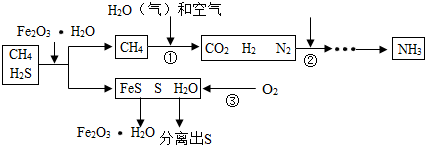
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷燃烧产生大量白色烟雾 | |
| B. | 铁丝在空气中剧烈燃烧,火星四射 | |
| C. | 硫在氧气中燃烧发出明亮的蓝紫色火焰 | |
| D. | 木炭在空气中充分燃烧生成二氧化碳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com