
 胆矾晶体部分失水后得到某硫酸铜晶体(CuSO4?xH2O),华雪同学为研究CuSO4?xH2O加热后所得物质的组成,做了以下实验:取10.7gCuSO4?xH2O晶体加热使其分解,绘制出固体的质量随温度的变化关系图.如图所示,到t1℃时该固体完全失去结晶水,化学方程式为:CuSO4?xH2O
胆矾晶体部分失水后得到某硫酸铜晶体(CuSO4?xH2O),华雪同学为研究CuSO4?xH2O加热后所得物质的组成,做了以下实验:取10.7gCuSO4?xH2O晶体加热使其分解,绘制出固体的质量随温度的变化关系图.如图所示,到t1℃时该固体完全失去结晶水,化学方程式为:CuSO4?xH2O
| ||
| 相对原子质量×原子个数 |
| 相对分子质量 |
| ||
| 160 |
| 8g |
| 18x |
| 2.7g |
| 64 |
| 64+32+16×4 |
| 64 |
| 80 |


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:初中化学 来源: 题型:
| A、①②③ | B、②③④ |
| C、①②④ | D、①③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:
 如图是A、B、C三种固体物质的溶解度曲线.
如图是A、B、C三种固体物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | 第Ⅳ组 | |
| 稀盐酸的质量/g | 15 | 30 | 45 | 60 |
| 生成气体的质量/g | 1.8 | n | 4.4 | 4.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 热水瓶用久后,瓶胆内壁常附着一层水垢(主要成份是CaCO3和Mg(OH)2,其它成份忽略不计).某兴趣小组的同学为了探究水垢中Mg(OH)2的含量,取10g水垢样品,向样品中加入足量的稀盐酸,其变化关系如图所示,试计算:
热水瓶用久后,瓶胆内壁常附着一层水垢(主要成份是CaCO3和Mg(OH)2,其它成份忽略不计).某兴趣小组的同学为了探究水垢中Mg(OH)2的含量,取10g水垢样品,向样品中加入足量的稀盐酸,其变化关系如图所示,试计算:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
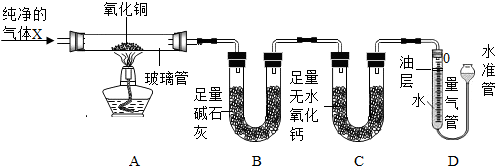
| 数据编号 测量项目 | Ⅰ | Ⅱ |
| 玻璃管(含药品)的质量/g | 52.40 | 51.92 |
| B装置(含药品)的质量/g | 102.00 | 102.54 |
| 氮气的体积/mL | / | 243.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:
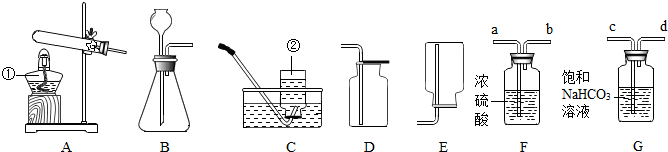
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com