
【题目】将30g黄铜(Cu﹣Zn合金)与100g稀硫酸在烧杯中恰好完全反应,反应后测得烧杯中剩余物的总质量为129.6g。已知锌与硫酸反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑。求:
(1)反应生成氢气的质量为_____g
(2)稀硫酸的溶质的质量分数(计算结果精确到0.1%)。_____。
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】如图是A、B两种固体物质的溶解度曲线,下列说法正确的是( )
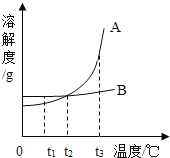
A. A的溶解度都大于B的溶解度
B. t2℃时,A、B两种饱和溶液中,溶质的质量分数相等
C. t1℃时,用等质量水配制的A、B饱和溶液中,所含溶质的质量:A>B
D. A、B两种饱和溶液都从t3℃降温到t2℃,析出的晶体的质量一定是:A>B
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站。“2—5号站”各站的对应物质属于不同类别的纯净物。

(1)若列车上的物质为“碳酸钠溶液”。
①列车途经“1号站”时,若指示剂为紫色石蕊溶液,溶液变 色。
②列车途经“2号站”时,若氧化物为二氧化碳,二氧化碳与碳酸钠溶液反应生成碳酸氢钠(NaHCO3)的化学方程式为 。
③列车途经“3号站”时,反应的化学方程式为 (写一个)。
(2)“碳酸钠溶液”列车抵达“4号站”时,将列车上的物质更换为“稀盐酸”后出发。
①与“碳酸钠溶液”和“稀盐酸”都能反应的“4号站”的对应物质为 (填一种)。②“稀盐酸”列车途经“5号站”时,反应的化学方程式为 (写一个)。
③“稀盐酸”列车途经“1、2、3号站”时,原“碳酸钠溶液”列车途经某站的对应物质必须更换为 (写一种物质),“稀盐酸”列车方能走完。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有如下仪器或装置,请回答下列问题:
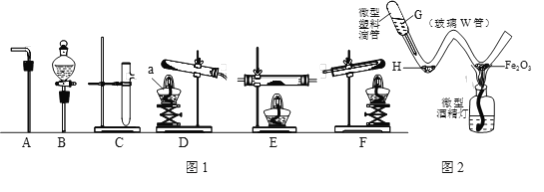
(1)仪器a的名称为______。
(2)用高锰酸钾制取氧气的化学方程式为_________________,选用装置D来进行制取时,通常要在试管口处放上_____________。
(3)草酸(H2C2O4)固体在浓硫酸作用下发生反应:H2C2O4=CO2↑+CO↑+H2O,
若用该反应来制取CO,制气装置应选____(填字母)和C进行组合;除去其中的CO2可选仪器A和C进行组合,C中最好装入下列试剂中的____(填小写字母)。
a. 烧碱溶液 b. 浓硫酸 c. 澄清石灰水
(4)若用CO还原氧化铜粉末,应选装置_____,反应的化学方程式为_______________。
(5)图2为某种“微型”实验装置。如果G处装稀盐酸,H处放少量铁屑,挤出少量盐酸使反应发生一段时间后,加热处出现的现象是____________。“微型塑料滴管”的功能相当于图1中的_____(填字母)。用微型仪器进行实验的优点很多,除试剂用量极少以外,还有____________(答一条)等等。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以实验事实和化学原理为依据进行科学推理是学习化学的重要方法之一,下列推理得出的相关结论正确的是( )
A. 气体的溶解度随压强增大而增大,CO2是气体,所以CO2的溶解度随压强的增大而增大
B. 酸能使紫色石蕊溶液变红,将二氧化碳通入紫色石蕊溶液中也变红,所以二氧化碳也是酸
C. 置换反应的生成物是单质和化合物,有单质和化合物生成的反应一定是置换反应
D. 化学变化过程中常伴有发光发热等现象,所以凡是有发光发热现象发生的变化一定是化学变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组同学利用右图装置探究可燃物燃烧的条件。
实验过程:
1将红磷和白磷分别放入两只试管中,一段时间后,A、B 试管中无明显现象。
2用气囊鼓入空气至白磷和红磷露出水面,A中白磷燃烧,B中无明显现象。
已知:红磷的着火点为240℃,白磷的着火点为40℃。
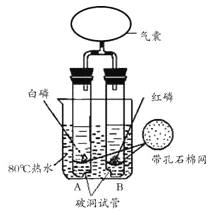
(1)仅通过对比实验②中露出水面的白磷和红磷可得到的结论是_____。
(2)实验过程中,能说明可燃物燃烧需要氧气的实验现象是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在探究金属与酸的反应时,发现铜片与20%的硫酸溶液不反应。有同学提出疑问“在一定条件下铜与硫酸能否发生反应”,并进行了系列实验。
(查阅资料)SO2能让红色的品红溶液褪色,能被NaOH溶液吸收。
(进行实验)(夹持仪器略)
实验1:初步实验(所用溶液均为硫酸溶液)
实验序号 | 1﹣1 | 1﹣2 | 1﹣3 | 1﹣4 | 1﹣5 |
装置 |
|
|
|
|
|
主要现象 | 铜片a附近溶液逐渐变蓝,铜片b附近产生无色气泡。 | 无明显现象 | 无明显现象 | 无明显现象 | 铜片溶解,溶液变蓝,生成有刺激性气味的无色气体 |
经检验实验1﹣1中产生的气体是氢气。
实验2:在实验1﹣5的基础上深入探究,装置如图。

(解释与结论)
(1)实验1﹣1中,能证明铜发生反应的现象是_____。
(2)实验1中,欲得出“升高温度可使铜与硫酸反应”需对比的实验是_____(填实验序号)。
(3)补全实验1﹣5和实验2中铜与硫酸反应的化学方程式:![]() _____
_____
(4)与实验1﹣5相比,实验2的优点有_____(写出一条即可)。
(5)通过上述实验能得出的结论是_____。
(反思与评价)
(6)下列说法不正确的是_____。
A 对比实验1﹣2和1﹣5,可得出“增大浓度可使铜与硫酸反应”
B 通电可促进一些化学反应的发生
C 铜与硫酸只能发生一种化学反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)汽车是现代生活中不可缺少的交通工具。
(1)下列汽车部件所用的主要材料属于合金的是 (填字母序号)。
A. 橡胶轮胎 B. 钢板车门 C. 玻璃风挡
(2)对汽车的部分钢铁部件进行喷漆可以防止其生锈,原因是 。
(3)汽车制造需要消耗大量的钢铁。工业炼铁时,CO和赤铁矿(主要成分是Fe2O3)发生的主要反应的化学方程式为 。
(4)目前,CNG双燃料环保汽车已经投入使用,这种汽车所用的燃料是汽油和压缩天然气。天然气的主要成分燃烧的化学方程式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】相同质量的M、N两种活泼金属,分别与足量质量分数为8%的盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如图.下列叙述正确的是
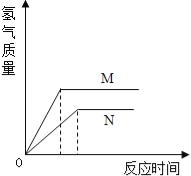
A. 金属的活泼性N>M
B. 两个反应生成H2的体积相等
C. 相对原子质量N>M
D. 两个反应消耗盐酸的质量一定相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com