
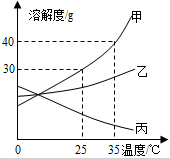
 甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而丙的溶解度随温度的升高而减少;若甲固体中含有少量乙,则提纯甲的方法是降温结晶,因为甲的溶解度受温度的影响变化比乙大;将25℃时乙的饱和溶液升温到35℃,则其溶液的溶质质量分数不变,因为乙的溶解度随温度升高而增大,升温后乙有饱和变为不饱和;25℃时,甲的溶解度是30g,因此将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量=15g+50g=65g.
解答 解:(1)若甲固体中含有少量乙,则提纯甲的方法是降温结晶,因为甲的溶解度受温度的影响变化比乙大;故答案为:降温结晶;
(2)将25℃时乙的饱和溶液升温到35℃,则其溶液的溶质质量分数不变,因为乙的溶解度随温度升高而增大,升温后乙有饱和变为不饱和;故答案为:不变;
(3)25℃时,甲的溶解度是30g,因此将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量=15g+50g=65g;故答案为:65;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.


科目:初中化学 来源: 题型:选择题
| A. | 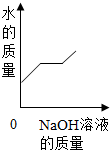 | B. | 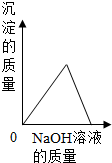 | C. |  | D. |  |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
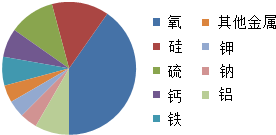 据报道:一颗陨石在俄罗斯中部乌拉尔山区坠落,陨石进入大气层时,速度达到了音速的40倍,而落地前的速度减小到了30千米/时,由此引发的“陨石雨”导致1200多名当地居民受伤.
据报道:一颗陨石在俄罗斯中部乌拉尔山区坠落,陨石进入大气层时,速度达到了音速的40倍,而落地前的速度减小到了30千米/时,由此引发的“陨石雨”导致1200多名当地居民受伤.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
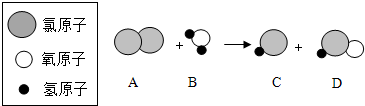
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 在杠杆的两端挂着质量和体积都相同的铁球和铝球,这时杠杆平衡,将两球分别浸泡在质量相同、溶质质量分数也相同的稀硫酸中(如图所示)直至两个烧杯中均没有气泡产生为止,两球的外形变化不大且无孔洞出现,下列推测中不正确的是:(金属球上附着的液体忽略不计,下同)( )
在杠杆的两端挂着质量和体积都相同的铁球和铝球,这时杠杆平衡,将两球分别浸泡在质量相同、溶质质量分数也相同的稀硫酸中(如图所示)直至两个烧杯中均没有气泡产生为止,两球的外形变化不大且无孔洞出现,下列推测中不正确的是:(金属球上附着的液体忽略不计,下同)( )| A. | 若铝球是空心的,则铁球一定也是空心的 | |
| B. | 拿掉烧杯后,杠杆仍然平衡 | |
| C. | 拿掉烧杯后,要想使杠杆平衡,支点应向N端移动 | |
| D. | 拿掉烧杯后,放铁球的那个烧杯中溶液质量大 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
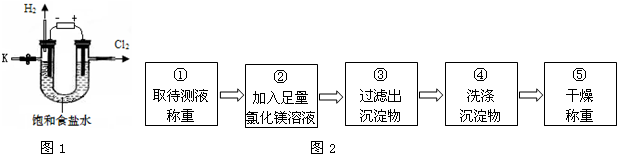
| 实验步骤 | 实验现象 | 实验结论 |
向待测液中滴加几滴酚酞试液 | 酚酞试液变红色 | 待测液呈碱性,表明含有氢氧化钠 |
| 加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
| 烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com