
| 实 验 操 作 | 实 验 现 象 | 结 论 |
| ①把品红试纸放入水中 | 试纸不褪色 | 猜想1不成立 |
| ②把品红试纸放入干燥的氯气中 | 试纸不褪色 | 猜想2不成立 |
| ③把品红试纸放入干燥的盐酸中 | 试纸不褪色 | 猜想3不成立 |
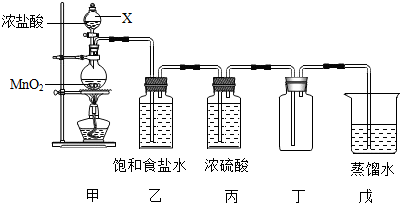
分析 (1)熟练掌握常见的化学仪器名称和用途;
(2)根据氯化钠能够和氯化氢、次氯酸反应防止对实验干扰分析;
(3)根据导气管的位置分析收集方法;
(4)【猜想】根据氯气溶于水后所得到的物质来完成猜想;
【实验探究】根据猜想和表格中所给的实验现象和结论来完成该题的解答;
【反思】根据盐酸对指示剂及次氯酸的漂白作用分析并写出反应的方程式.
解答 解:(1)X是分液漏斗;
(2)氯化钠能够和氯化氢、次氯酸反应防止对实验干扰;
(3)因为收集氯气的导气管伸入到集气瓶的底部,把空气通过短管排出,故是向上排空气法收集;
(4)【猜想】氯水是指氯气溶于水,既有物理变化(氯气和水),又有化学变化(生产盐酸和次氯酸),所以结合其它猜想我们可以作出是次氯酸使品红褪色的猜想,次氯酸的化学式为:HClO;
【实验探究】猜想1不成立,说明品红没有褪色;
要证明猜想3不成立,只要把品红试纸伸入到盐酸中,现象是无变化就可以了,故答案为:把品红试纸伸入到盐酸中;
【反思】因为氯水中有HCl和HClO,酸性溶液可使石蕊变红,而HClO具有漂白作用,故向氯水中滴加紫色石蕊试液,观察到的现象是:先变红色后褪色;
故答案为:(1)分液漏斗;(2)吸收HCl和HClO;(3)向上排空气法;
(4)HClO; 试纸不褪色;把品红试纸放入干燥的盐酸中; 氯水先变红后褪色;Ca(OH)2+2HCl═CaCl2+2H2O; 2HClO+Ca(OH)2=Ca(ClO)2+2H2O.
点评 本题考查了是在气体制取的已有能力的基础上进行拓展运用来探究氯气的制取和性质的探究,既有气体的制取、性质又有气体与水反应后生成物的检验,综合性比较强.本题根据题目提供的信息,结合实验探究的一般步骤和酸的性质等知识来解决.


科目:初中化学 来源: 题型:选择题
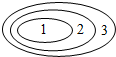 下列选项中,各概念之间能构成图中包含关系的是( )
下列选项中,各概念之间能构成图中包含关系的是( )| 选项 | 1 | 2 | 3 |
| A | 悬浊液 | 乳浊液 | 溶液 |
| B | 蛋白质 | 脱氧核糖核酸 | 染色体 |
| C | 昆虫 | 脊椎动物 | 动物 |
| D | 种群 | 群落 | 生态系统 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
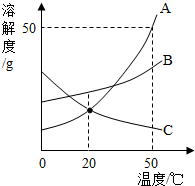 如图是A、B、C三种物质的溶解度曲线,下列分析不正确的是( )
如图是A、B、C三种物质的溶解度曲线,下列分析不正确的是( )| A. | 50℃时A、B、C三种物质的溶解度由大到小的顺序是A>B>C | |
| B. | 50℃时把50gA放入50g水中能得到A的饱和溶液,其中溶质与溶剂 的质量比为1:2 | |
| C. | 20℃时,A、C溶液中溶质的质量分数相同 | |
| D. | 将50℃时A、B、C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A>C |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| NaHCO3 | Na2CO3 | |
| 加入稀盐酸 | 产生气泡 | 产生气泡 |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 实验步骤 | 实验现象 | |
| ①取少量样品溶于水,加入过量的氯化钙溶液. | 有白色沉淀产生 | 该反应的方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl |
| ②将上述反应后的混合液过滤,取滤液滴加稀盐酸 | 有气泡冒出 | 该反应的方程式: Na2CO3+2HCl═2NaCl+H2O+CO2↑ 证明猜想②成立. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
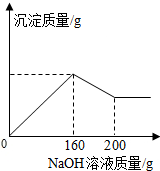 已知氢氧化铝能溶解在过量的氢氧化钠溶液中生成偏铝酸钠(NaAlO2)溶液,有关化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.现有160.0g某无色溶液,可能含有稀硫酸、硫酸镁、硝酸钾、硫酸亚铁、氯化铝、碳酸钾中的一种或数种.取100.0g该溶液于烧杯中,往其中逐滴加入20.0%的NaOH溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图所示.下列有关的判断正确的个数是( )
已知氢氧化铝能溶解在过量的氢氧化钠溶液中生成偏铝酸钠(NaAlO2)溶液,有关化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.现有160.0g某无色溶液,可能含有稀硫酸、硫酸镁、硝酸钾、硫酸亚铁、氯化铝、碳酸钾中的一种或数种.取100.0g该溶液于烧杯中,往其中逐滴加入20.0%的NaOH溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图所示.下列有关的判断正确的个数是( )| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③ | C. | ③④ | D. | ②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com