
【题目】通过一学期的化学学习,相信你已经初步掌握了实验室制取气体的有关知识。请结合图示回答问题。

(1)写出图中标示的仪器名称:A______,②______。
(2)实验室制取![]() ,应选用的发生装置为______(填字母序号,下同),收集装置一般不建议使用F原因是______,但是小明同学用F确实能收集满瓶
,应选用的发生装置为______(填字母序号,下同),收集装置一般不建议使用F原因是______,但是小明同学用F确实能收集满瓶![]() ,请写出可能的原因(一条即可)______,写出实验室制取
,请写出可能的原因(一条即可)______,写出实验室制取![]() 反应的化学方程式______。
反应的化学方程式______。
(3)用F收集氧气时观察到______,可以开始收集,观察到______,表示装置已经集满气体。利用G或H收集气体时导气管都要接近集气瓶底原因是______。
(4)实验室用装置E制取![]() 时,如用注射器C替换长颈漏斗,优点是______。
时,如用注射器C替换长颈漏斗,优点是______。
【答案】酒精灯 水槽 E 二氧化碳能溶于水 二氧化碳能溶于水,但溶解能力较小(二氧化碳逸出的速度大于生成碳酸的速度) CaCO3+2HCl==CaCl2+H2O+CO2↑ 导管口的气泡连续均匀放出 集气瓶口有大气泡生成 让空气充分排出,收集到较纯的气体 能控制反应的速率
【解析】
(1)图中标示①的仪器名称是酒精灯,图中标示②的仪器名称是水槽;
(2)实验室制取CO2,是用大理石或石灰石与稀盐酸制取,该反应的反应物的状态是固体和液体,不需加热,属于固—液常温型,可选用发生装置E;实验室制取CO2,收集装置一般不建议使用F原因是二氧化碳能溶于水,小明同学用F确实能收集满瓶CO2,可能的原因二氧化碳能溶于水,但溶解能力较小(或二氧化碳逸出的速度大于生成碳酸的速度);大理石或石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)用F收集氧气时观察到导管口的气泡连续均匀放出,可以开始收集,观察到集气瓶口有大气泡生成,表示装置已经集满气体。利用G或H收集气体时导气管都要接近集气瓶底原因是为了让空气充分排出,收集到较纯的气体;
(4)注射器能控制液体的滴加速率,能控制反应的速率。实验室用装置E制取CO2时,如用注射器C替换长颈漏斗,优点是能控制反应的速率。


科目:初中化学 来源: 题型:
【题目】对下列事实的微观解释正确的是![]()
![]()
选项 | 事实 | 解释 |
A | 体温计中的水银 | 分子间间隔随温度改变 |
B | 氧气能压缩在蓝色钢瓶中 | 氧分子大小随压强变大而减小 |
C | 金刚石、石墨性质存在明显差异 | 碳原子的排列方式不同 |
D | 氮气是无色的 | 氮分子是无色的 |
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碘是人体必需的微量元素之一。下图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图。下列说法错误的是
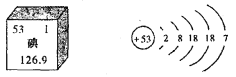
A.碘的相对原子质量为126.9,原子核内质子数为53
B.碘原子核外共有53个电子,最外层有7个电子
C.碘元素属于非金属元素,碘原子在化学反应中易得电子
D.碘盐中含有碘酸钾(KIO3),KIO3中碘元素的化合价为一1价
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“美丽乡村”建设是精准扶贫的民心工程,在农村推广家用沼气池建设是改善农村能源结构和环境卫生的重要举措。如图甲是沼气的主要成分:乙是最常见的液体;丁是白色难溶固体,其中金属元素的质量分数为40%,试剂B具有刺激性气味,则甲的化学式为_____。②③反应的化学方程式分别为:②_____,③_____。
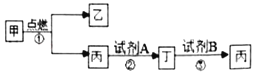
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图回答问题。
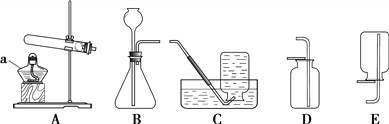
(1)仪器a的名称是_____________。
(2)用高锰酸钾制取氧气的化学方程式为______________________________,用C装置收集的气体应具有的性质是______________________。
(3)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是___________,用D装置收集二氧化碳的验满方法是_____________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂,高温燃烧12.5t石灰石(主要成分是CaCO3),完全反应后只生成生石灰(CaO)固体和二氧化碳气体(已知石灰石中的杂质都是固体且都不参与反应)最后得到固体质量为8.1t。试计算:
(l)CaCO3中氧元素的质量分数______。
(2)求生成二氧化碳多少______t?
(3)该工厂所用石灰石中碳酸钙的质量分数(即石灰石中CaCO3含量)是多少______?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了解甲酸的分解产物,实验小组进行了以下探究:
【查阅资料】甲酸(HCOOH)的熔点为8.6℃,能分解生成两种物质。
【提出猜想】实验小组对甲酸的分解产物提出了猜想:
猜想1.H2和CO2;猜想2.CO和H2O。
【设计实验】20℃时,甲酸的状态为______;从图一装置中选择合适的装置______(填序号)对甲酸进行加热。为了加快分解速率,实验小组加入了催化剂,反应后将分解产物通入图二装置进行实验。
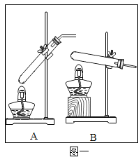
【实验预测】若猜想l成立,则D中的实验现象应为______。
【进行实验】实验中观察到C处瓶内出现大量水珠,F处玻璃管中出现的现象为______,甲酸分解的化学方程式为______。
【交流拓展】资料表明,不同条件下,甲酸的分解产物不同,猜想1和猜想2均能成立。据此小新对甲酸的分解产物又提出新猜想:猜想3.H2O和CO2;猜想4.CO和H2。经讨论认为无需进行实验就能确定猜想3和猜想4都错误,理由是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲乙丙丁四位同学正在讨论某化学方程式表示的意义,他们的描述如下:
甲说:反应在点燃条件下进行
乙说:各物质的分子个数比为2:1:2
丙说:是化合反应
丁说:各物质的质量比为7:4:11
他们所描述的化学方程式是( )
A. 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
B. 2CO+O2![]() 2CO2
2CO2
C. 2H2+O2![]() 2H2O
2H2O
D. CH4+2O2![]() CO2+2H2O
CO2+2H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定实验室中氯酸钾样品的纯度,取5g该样品与1g二氧化锰均匀混合,依次加热该混合物,经t1、t2、t3、t4时间后分别冷却,称量剩余圊体质量,记录的有关数据如表(样品中杂质不参加化学反应)
加热时间 | t1 | t2 | t3 | t4 |
剩余固体(g) | 4.24 | 4.16 | 4.08 | 4.08 |
(1)完全反应后产生氧气的总质量为_____。
(2)样品中氯酸钾的纯度是__________?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com