
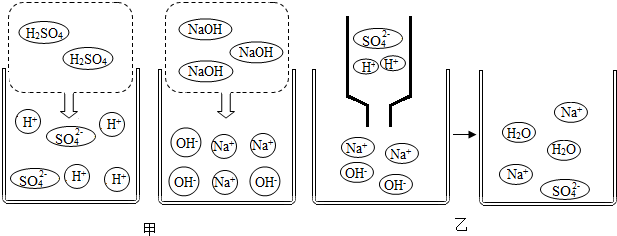
 某组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中,有一瓶溶液未盖瓶盖且标签破损(如图),于是决定对这瓶溶液进行实验探究:
某组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中,有一瓶溶液未盖瓶盖且标签破损(如图),于是决定对这瓶溶液进行实验探究:分析 【实验推断】
(1)根据氯化钠、氢氧化钠、碳酸钠三种溶液的酸碱性进行分析;
(2)根据碳酸钠溶液与盐酸的反应进行分析;
(3)根据氢氧化钠与空气中二氧化碳反应进行分析.
【继续探究】
根据碳酸钠与CaCl2溶液或氯化钡溶液的反应进行分析.
【实验结论】综合分析得出结论.
【探究启示】根据氢氧化钠溶液易与空气中的二氧化碳反应,得出实验取完药品后应注意的事项.
解答 解:【实验推断】(1)氢氧化钠和碳酸钠溶液都呈碱性能使酚酞试液变红色,氯化钠溶液呈中性,所以,小亮取样滴加无酚酞试液,溶液呈红色,得出结论:该溶液不可能是氯化钠溶液;
(2)若有碳酸钠存在,滴加盐酸,发生反应Na2CO3+2HCl=2NaCl+H2O+CO2↑,有气泡产生.所以,小辉另取样滴加稀盐酸有气泡产生,小辉得出结论:该溶液是碳酸钠溶液;
(3)因为该试剂是敞口放置于空气中,若是氢氧化钠可能会和空气中二氧化碳反应变质生成部分碳酸钠,所以,小磊认为小辉的结论不完全正确,理由是露置于空气中的NaOH溶液与空气中的CO2反应也生成碳酸钠.
【继续探究】要证明原来是氢氧化钠,可先加过量氯化钡或氯化钙溶液溶液除尽碳酸根,再用酚酞检验氢氧化钠的存在.所以,另取样加入过量的CaCl2溶液,观察到有白色沉淀产生,设计这一步骤的目的是完全除去溶液中的CO32-,避免其对OH-检验造成干扰;静置后,取上层清液,滴入酚酞试液,溶液呈红色.
【实验结论】因为碳酸根已转变为碳酸钙沉淀,滴加酚酞变红色,证明氢氧根的存在,即氢氧化钠的存在,所以,这瓶溶液是:NaOH溶液(填变质的NaOH溶液也可).
【探究启示】由于氢氧化钠易与空气中的二氧化碳反应,所以,实验取完药品后应立即盖好瓶盖.
故答案为:【实验推断】(1)氯化钠;氯化钠溶液呈中性,不能使酚酞试液变红;
(2)气泡;Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(3)露置于空气中的NaOH溶液与空气中的CO2反应也生成碳酸钠.
【继续探究】白色沉淀; 完全除去溶液中的CO32-,避免其对OH-检验造成干扰.
【实验结论】NaOH溶液(填变质的NaOH溶液也可).
【探究启示】密封保存.
点评 本题是缺失标签的实验探究题,相当于物质鉴别题,在鉴别几种物质时要从物质的不同性质入手,但试题涉及知识点多,要加强知识的全面性和系统性.


科目:初中化学 来源: 题型:选择题
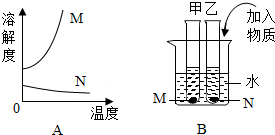 A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,加入的物质可能是( )
A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,加入的物质可能是( )| A. | 冰水 | B. | NH4NO3 | C. | NaCl | D. | NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是a、b、c三种物质的溶解度曲线:
如图是a、b、c三种物质的溶解度曲线:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 溶液中可能含有的离子 | 实验步骤、现象与结论 |
| 可能含有CO32- |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
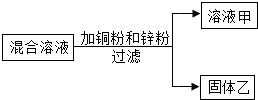 某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示:
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示:| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com