
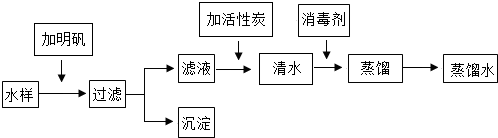
分析 (1)明矾能够吸附水中的悬浮物,可以据此答题;
(2)根据过滤操作所需的仪器来补充合适的仪器;
(3)根据化合物中各元素的化合价的代数和为0进行解答;
解答 解:
(1)明矾溶于水后生成的胶状物对杂质的吸附,使杂质沉降来达到净水的目的;
(2)过滤需要烧杯、漏斗、玻璃棒等玻璃仪器;
(3)在Na2FeO4中由于钠显+2价、氧显-2价,由化合物中正负化合价的代数和为零可知,高铁酸钠中铁元素的化合价为x
(+1)×2+x+(-2)×4=0
x=+6
氯气和水反应生成HCl和HClO,方程式为Cl2+H2O═HCl+HClO,故答案为:Cl2+H2O═HCl+HClO;
答案:
(1)吸附悬浮的固体杂质,加速沉降;
(2)玻璃棒;
(3)+6; Cl2+H2O═HCl+HClO
点评 熟练掌握净化水的方法,要充分理解明矾、活性炭的性质及它们的作用,并能熟练的运用.


科目:初中化学 来源: 题型:解答题
 某实验小组的同学用氢氧化钡溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钡溶解加入一定量稀盐酸后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.
某实验小组的同学用氢氧化钡溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钡溶解加入一定量稀盐酸后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2O→CO2 | B. | (NH4)2SO4→NH3 | C. | Cu→Cu(NO3)2 | D. | MgO→MgCl2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 化学式 | 条件 | 1 mol气体体积/L |
| H2 | 0℃,101 kPa | 22.4 |
| O2 | 22.4 | |
| CO | 22.4 | |
| H2 | 0℃,202 kPa | 11.2 |
| CO2 | 11.2 | |
| N2 | 273℃,202 kPa | 22.4 |
| NH3 | 22.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | PM2.5主要是由于化石燃料的大量燃烧引起的,所以,为了降低空气中PM2.5的含量,我们应该马上停止使用化石燃料 | |
| B. | 鼻腔内的绒毛对空气中较粗的颗粒物具有一定的阻挡作用,这属于特异性免疫 | |
| C. | PM2.5主要是通过消化道进入人体内部的 | |
| D. | 减少PM2.5对保护环境,维持生态系统的稳定性将起到重要作用 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是某硫酸试剂瓶标签上的部分文字说明.
如图是某硫酸试剂瓶标签上的部分文字说明.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com