
【题目】如图是实验室制取和收集气体的常用装置图,请根据所给的装置图回答下列问题:
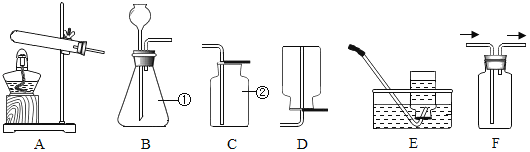
(1)请写出装置图 C 中标号②的仪器名称:___;
(2)大理石与稀盐酸反应制取二氧化碳时应选用的发生装置和收集装置是___(填字母序号),检验二氧化碳的方法是___;
(3)在常温下,用固态的亚硫酸钠和液态的稀硫酸反应制取二氧化硫气体,应选用的发生装置是___;通常情况下,二氧化硫是一种易溶于水、密度比空气大的有毒气体,排放在空气中会造成空气污染,应选用___装置进行收集,以便将多余的二氧化硫进行吸收处理。
【答案】集气瓶 BC或BF 将气体通入澄清的石灰水中,石灰水变浑浊,说明是二氧化碳 B F
【解析】
(1)仪器②是集气瓶;
(2)实验室中制取二氧化碳常用大理石和稀盐酸反应来制取,反应物是固体和液体,不需要加热,属于固—液常温型,所以应该选择B装置来制取二氧化碳气体;二氧化碳密度比空气大,能溶于水,应用向上排空气法收集,所以应该选择C或F(长导管是进气管)装置来收集二氧化碳。大理石与稀盐酸反应制取二氧化碳时应选用的发生装置和收集装置是BC或BF;二氧化碳能使澄清石灰水浑浊,常用澄清的石灰水检验二氧化碳气体。检验二氧化碳的方法是将气体通入澄清的石灰水中,石灰水变浑浊,说明是二氧化碳;
(3)在常温下,用固态的亚硫酸钠和液态的稀硫酸反应制取二氧化硫气体,反应物是固体和液体,不需要加热,属于固—液常温型,所以应该选择B装置来制取;二氧化硫是一种易溶于水、密度比空气大的有毒气体,应选用向上排空气法收集。排放在空气中会造成空气污染,应选用F装置进行收集,以便将多余的二氧化硫进行吸收处理。


科目:初中化学 来源: 题型:
【题目】分类、类比是学习化学常用的方法。
(1)初中化学实验可以按照实验目的分为:“物质含量的探究”、“探究反应条件实验”、“混合物的分离提纯”等。因此应将下列实验中的B与实验____(填“A”或“C”或“D”)归为一类,分类依据是_________。

(2)甲烷、乙烷、丙烷、丁烷等分子结构相似的一类有机化合物,统称为“烷烃”
物质 | 甲烷 | 乙烷 | 丙烷 | 丁烷 | … |
化学式 | CH4 | C2H6 | C3H8 | … |
根据上表“烷烃”化学式排列规律,你认为丁烷的化学式为_________,丙烷燃烧与甲烷燃烧类似,丙烷完全燃烧的化学方程式是___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分)同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应? 在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应。
(1)实验装备
①查阅资料:NaHCO3+NaOH=====Na2CO3+H2O
②用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考。
NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅱ |
加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
表中的现象Ⅰ为_________,现象Ⅱ对应反应的化学方程式为_________。
(2)实验过程
【实验1】证明反应生成了Na2CO3
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是__________。 有同学提出这个实验不足以证明有Na2CO3生成,其理由是_________。为了证明有Na2CO3生成,需要继续进行的操作是____________。
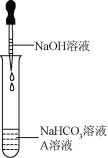
【实验2】证明反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是_________。
(3)实验反思
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过对化学的学习,你已掌握了实验室制取气体的有关规律,请结合如图回答有关问题:
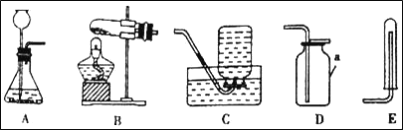
(1)图中标有a的仪器名称是_____。
(2)实验室用氯酸钾制取氧气,反应的化学方程式为_____,可选择的收集装置是D或_____(填字母,下同)。
(3)实验室用锌和稀硫酸制取氢气,应选择的发生装置是_____,反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将铜和氧化铜混合物粉末11.2g放入烧杯中,当加入稀硫酸100g时,氧化铜与硫酸恰好完全反应(CuO+H2SO4=CuSO4+H2O),过滤后所得溶液的质量为108g.(结果精确到0.1)
(1)铜 (填“能”或“不能”)与稀硫酸反应,因为 .
(2)求原混合物中铜的质量.
(3)求反应后滤液中溶质的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与化学反应基本类型间的关系如图所示,下列方程式属于阴影3的是( )
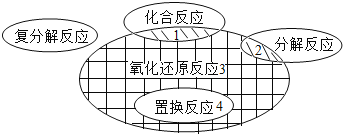
A. C+O2![]() CO2
CO2
B. CuO+CO![]() Cu+CO2
Cu+CO2
C. Mg(OH)2+2HCl=MgCl2+2H2O
D. Fe+CuSO4=FeSO4+Cu
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】整理、归纳物质性质之间的相互联系,是化学学习的一种有效方法.小丽在复习单质、氧化物、酸、碱、盐性质时,构建了以下知识网络图,图中短线“﹣﹣”表示相连的两种物质能在一定条件下发生反应.我能帮小丽在单质、氧化物、酸、碱、盐五类物质中分别选取一种物质,将它们的化学式填写在下图圆圈中,并符合以上要求.
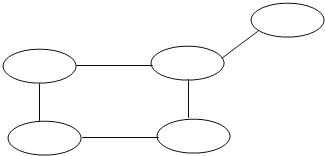 _____
_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上以半水煤气(主要成分是 N2、H2、CO、CO2和H2O)、食盐等为原料制取纯 碱的流程如图 1:
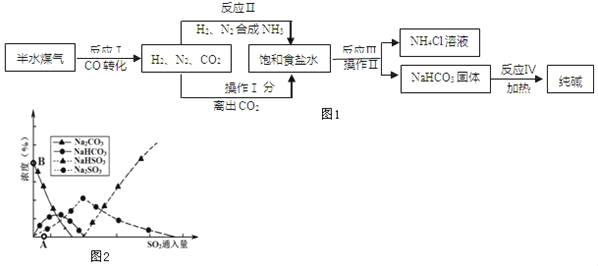
(1)反应Ⅰ是在使用铜催化剂和加热条件下,半水煤气主要成分间发生反应,实现了 CO 转化,化学方程式是_____。
(2)将反应Ⅱ生成的 NH3和操作Ⅰ分离出的CO2通入饱和食盐水中即可得 NaHCO3固体,下列两种操作,你觉得更为合理的是_____。
a先通 NH3再通入CO2 b先通 CO2再通入 NH3
(3)操作Ⅱ的名称是_____,实验室进行该项操作时,需要用到的玻璃仪器有:普通漏斗、烧杯和_____,该仪器在此操作中的作用是_____。
(4)反应Ⅲ的成功实现说明该实验条件下,NaHCO3的溶解度_____(填“>”“<”或“=”)NH4Cl 的溶解度。
(5)纯碱用途广泛。工业上可用废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2,制备无水Na2SO3,达到减少污染、节约资源的目的。反应过 程中溶液组成变化如图 2 所示。
①吸收初期(图2中A点以前)反应的化学方程式为_____。
②不断通入 SO2,最终产物是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请用化学用语填空:
(1)氩的元素符号_____。
(2)两个亚铁离子_____。
(3)标出碳酸钾中碳元素的化合价_____。
(4)地壳中含量最多的元素_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com