
【题目】化学实验室常常产生许多废液,经无害化处理后可防止对环境的破坏。化学兴趣小组同学设计了四组实验对NaOH溶液和Ca(OH)2溶液进行鉴别,请你参与实验,并对废液的成分展开探究。
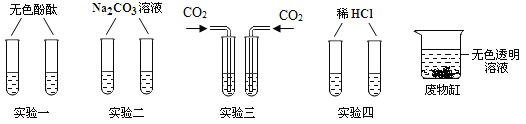
(1)上述四组实验不能达到鉴别目的的是_____。
(2)实验中产生白色沉淀H属于复分解反应的化学方程式_____。
(3)将上述四组实验的八支试管中的废液倒入一个洁净的大烧杯中 ,先有大量的气泡,后沉淀消失,得到澄清无色透明溶液。那么,该废液中含有哪些物质呢(酚酞除外) ?
(查阅资料) NaCl、 CaCl2溶液呈中性
(猜想)A: NaCl、CaCl2、NaOH B: NaCl、 CaCl2 C:______。
大家经认真思考后,认为猜想______一定是错的。理由是______。
(设计实验)
实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案一 | 取废物缸中少量试液于试管,滴入含有稀HNO3的AgNO3溶液 | _____。 | 猜想C正确 |
方案二 | 另取废物缸中少量试液于另一试管中,加入少量_______固体。 | 固体溶解消失, 溶液变成蓝色 |
(反思)大家交流后,认为实验方案一 有问题,你认为原因是_____。
另外,大家共同决定在废液中加入适量的碳酸钠溶液,恰好完全反应后,过滤。再将废液进行______(填实验操作),就可以将废液处理并回收得到NaCl。
【答案】实验一和实验四 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH NaCl、CaCl2、HCl A 反应后澄清无色透明溶液,说明反应后溶液呈中性或酸性,氢氧化钠呈碱性,所以反应后溶液中溶质一定不存在氢氧化钠 产生白色沉淀 氢氧化铜或氧化铜 氯化钙和盐酸都能与硝酸银产生白色沉淀 过滤
【解析】
(1)实验一:NaOH溶液和Ca(OH)2溶液都呈碱性,加入酚酞后溶液都呈红色,现象相同,不能鉴别;
实验二:碳酸钠溶液与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠与碳酸钠溶液不能反应,加入碳酸钠溶液后产生白色沉淀的是氢氧化钙,无明显变化的是氢氧化钠溶液,现象不同,可以鉴别;
实验三:二氧化碳与氢氧化钠溶液能反应,没有明显的实验现象,二氧化碳能使澄清石灰水变浑浊,现象不同,可以鉴别;
实验四:NaOH溶液和Ca(OH)2溶液都以能与盐酸反应,但没有明显的现象,现象相同,不能鉴别。四组实验不能达到鉴别目的的是实验一和实验四;
(2)实验中产生白色沉淀H的反应是二氧化碳与氢氧化钙反应生成碳酸钙和水,碳酸钠溶液与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,其中二氧化碳与氢氧化钙反应由于没有相互交换成分,不属于复分解反应,碳酸钠溶液与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,该反应是由两种化合物互相交换成分,生成另外两种化合物的反应属于复分解反应,反应的化学化学方程式是:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)猜想:
将上述四组实验的八支试管中的废液倒入一个洁净的大烧杯中 ,先有大量的气泡,后沉淀消失,得到澄清无色透明溶液,说明废液中存在盐酸,反应后溶液呈中性或酸性,盐酸可能有剩余,反应过程中钠离子、钙离子、氯离子没有形成沉淀、气体,在溶液一定存在,所以猜想C可能是NaCl、CaCl2、HCl;猜想A一定是错的。理由是反应后澄清无色透明溶液,说明反应后溶液呈中性或酸性,氢氧化钠呈碱性,所以反应后溶液中溶质一定不存在氢氧化钠;
设计实验:
盐酸与硝酸银反应生成氯化银沉淀和硝酸钠,氯化钙与硝酸银反应生成氯化银和硝酸钠,氢氧化铜与盐酸反应生成蓝色氯化铜溶液和水,氧化铜与盐酸反应生成蓝色氯化铜溶液和水。因此:
实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案一 | 取废物缸中少量试液于试管,滴入含有稀HNO3的AgNO3溶液 | 产生白色沉淀 | 猜想C正确 |
方案二 | 另取废物缸中少量试液于另一试管中,加入少量氢氧化铜或氧化铜固体。 | 固体溶解消失, 溶液变成蓝色 |
反思:实验方案一有问题,原因是氯化钙和盐酸都能与硝酸银产生白色沉淀;
碳酸钠溶液与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,碳酸钠溶液与盐酸反应生成氯化钠、水和二氧化碳。大家共同决定在废液中加入适量的碳酸钠溶液,恰好完全反应后,过滤。再将废液进行过滤,就可以将废液处理并回收得到NaCl。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:初中化学 来源: 题型:
【题目】对于一些没有明显现象的化学反应,在设计实验时常常会利用转换法,将现象变得直观。根据如图所示的实验回答问题。
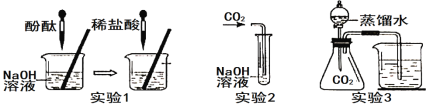
(1)实验1中,烧杯内发生反应的化学方程式为_____________________________,当观察到实验1烧杯内液体的颜色刚好由________色变成无色时,说明NaOH与HCl发生了反应。
(2)实验2中,试管内发生反应的化学方程式是_______________________________,下列试剂不能验证反应是否发生的是___________(填序号,后同)。
A 稀盐酸 B 无色酚酞溶液 C CaCl2溶液 D Ba(NO3)2溶液
(3)实验3为了证明CO2能与水反应,可向右侧烧杯内装入________。
A 水 B 稀盐酸 C 紫色石蕊溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中国是最早发明火药的国家。据史书记载,我国古代的炼丹家在长期炼制丹药过程中,发现硝、硫磺和木炭的混合物点燃时会发生爆炸,其反应原理是:2KNO3+S+3C![]() K2S+N2↑+3CO2↑,下列有关该反应说法正确的是( )
K2S+N2↑+3CO2↑,下列有关该反应说法正确的是( )
A. 反应前后元素的化合价都发生了改变
B. 该反应中没有氧气参加,不属于燃烧
C. 反应生成大量气体,放热,体积急剧膨胀,引起爆炸
D. 反应物和生成物中均有单质和化合物,属于置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢氧化钠在空气中不仅吸收水分,还会与二氧化碳反应。有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品,向其中滴加溶质质量分数为7.3%的稀盐酸,只放出二氧化碳气体,且二氧化碳质量与加入稀盐酸的质量关系如图所示。
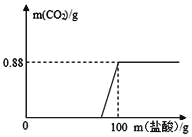
(1)写出氢氧化钠在空气中变质的化学方程式:_____。
(2)计算样品中碳酸钠的质量_____________(写出计算过程)。
(3)计算稀盐酸和样品恰好完全反应时所得溶液溶质质量分数______________(结果精确到0.1%,写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】可燃物在不同条件下燃烧会产生不同的现象,如木炭在氧气中燃烧没有火焰产生,在空气中燃烧却有火焰产生;蜡烛在氧气中燃烧无黑烟(主要成分为炭黑)生成,在空气中却有黑烟生成。同学们对此开展了以下探究:
(1)写出木炭在氧气中完全燃烧的化学方程式:_____。
(查阅资料)木炭在空气中发生不完全燃烧会生成一氧化碳。
(2)木炭在空气中燃烧产生火焰的原因是:_____;
(3)蜡独在空气中燃烧有黑烟生成,说明蜡烛中一定含有:_____;
(提出问题)导致蜡烛发生不完全燃烧的原因有哪些?
甲同学:可能与氧气的接触面积有关;
乙同学:可能与氧气的含量有关;
你认为还可能与_____(写出一种即可)有关。
(设计实验)甲同学设计的实验如下:收集体积分数为52%的氧气于钟罩中,再将蜡烛点燃立即罩上钟罩;几秒钟后,用白瓷板压住蜡烛火焰。发现刚开始时白瓷板上没有明显现象,过一会后有大量的炭黑出现,证明甲同学的猜想正确。
(4)用白瓷板压住蜡烛火焰的目的是_____;
乙同学直接将点燃的蜡烛放在钟罩中,再利用数字化实验测出氧气和一氧化碳的含量的变化曲线(如图所示)。
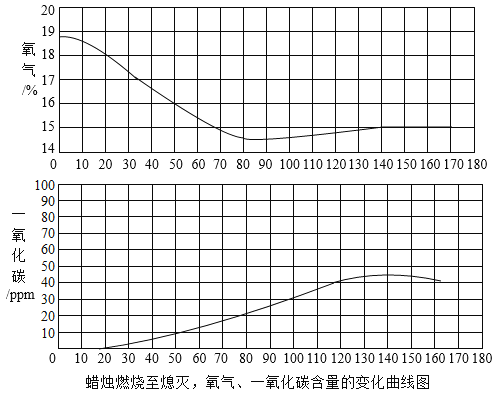
(5)初始阶段蜡烛发生的是完全燃烧,结合曲线说明理由:_____;后续阶段氧化碳含量逐渐升高的原因是:_____;
(6)可燃物发生不完全燃烧,会造成极大的危害除浪费资源外,还会造成的危害是_____(写一种即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气和水是人类无法离开的物质。
(1)空气中________含量升高会造成“温室效应”。
(2)如图1是测定空气中氧气含量的实验装置:
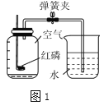
①红磷足量的原因是____________;
②燃烧产生的现象为发出白光,放出热量,产生大量的________。
(3)生活中可用活性炭净水,是利用活性炭的________性。生活中可用________的方法降低水的硬度。
(4)t2 ℃时,将甲、乙各80 g分别放到盛有100 g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图2,甲和乙的溶解度曲线如图3。请结合图示回答下列问题:
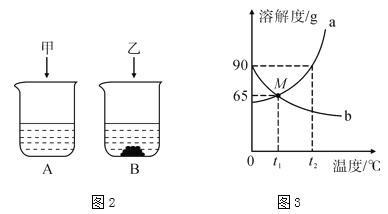
①固体甲对应的溶解度曲线是______(填“a”或“b”)。
②M点的含义_______。
③向烧杯A的溶液中继续加入15 g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体析出,你认为“全部溶解”的原因是___________。
④将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,所得溶液的有关说法正确的是______(填字母)。
a.甲溶液仍为饱和溶液
b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙
d.两溶液溶质质量分数甲>乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,易溶于水,与AgNO3不反应),另外还含有NaCl,其它成分不考虑。请回答下列问题:
(1)味精中至少含有__________(填数字)种元素。
(2)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是_________(填字母)。
A.5mL B. 10 mL C. 50 mL D. 100 mL
(3)下图是配制过程,正确的操作顺序为_______(填字母) 。
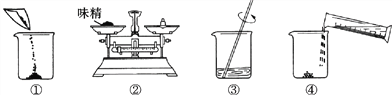
A.①②③④ B.②①④③ C.②④①③
(4)为测定NaCl在味精中的质量分数,进行如下实验:
①向所配制的50g溶液中加入AgNO3溶液充分反应,检验沉淀是否完全的方法是:静置后,在上层清液中加入______(填化学式)溶液,观察是否有沉淀生成。
②在其它操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液中,谷氨酸钠的质量分数____(填“偏大”、“偏小”或“无影响”),所测定的味精中NaCI的质量分数___(填“偏大”、“偏小”或“无影响”)。
③精确测定AgCl沉淀质量为2.87 g,则该味精中NaCl的质量分数为___。(计算结果精确到0.1%。有关物质的相对分子质量:NaCl-58. 5 , AgCl-143. 5 )
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图,下列说法正确的是( )

A. t1℃时,甲、乙两种溶液的溶质质量分数相同
B. t1℃时,取少量甲的饱和溶液,加入少量乙,不能再溶解
C. t1℃时,取少量甲的饱和溶液升温到t2℃,变成不饱和溶液
D. t2℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量甲>乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com