
【题目】如图表示某些物质间转化关系(“→”表示物质之间存在转化关系,部分反应的条件已略去)。其中B、C是由相同元素组成的无色液体,且B具有消毒杀菌作用;D、H、I为气体单质,其中H是空气中含量最多的气体;M为有刺激性气味的气体,A、E、F为固体,F呈红棕色。
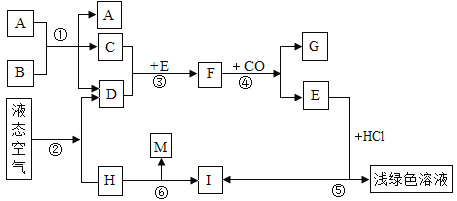
试回答下列问题:
(1)反应①中A的作用是_________________。
(2)在日常生活中为了避免反应③的发生,可采取的措施是_________(任写一种)。
(3)写出反应④的化学方程式:________________。
(4)写出反应⑤的化学方程式:___________________。
(5)已知同温同压下不同气体的体积之比等于气体分子个数之比,化合反应⑥是工业上的重要反应,为提高反应物的利用率,反应时应提供H和I的最佳体积比为_________________。
【答案】催化作用 刷漆 3CO+Fe2O3![]() 2Fe+3CO2 Fe+2HCl=FeCl2+H2↑ 1:3
2Fe+3CO2 Fe+2HCl=FeCl2+H2↑ 1:3
【解析】
B、C是由相同元素组成的无色液体,且B具有消毒杀菌作用,D为气体,因此B是过氧化氢溶液,C是水,D是氧气,A是二氧化锰;H是空气中含量最高的气体,所以H是氮气;E、F为固体,F呈红棕色,所以E是铁,铁、氧气、水在一定条件下生锈,所以F是氧化铁,氧化铁和一氧化碳高温生成铁和二氧化碳,E和盐酸反应产生浅绿色的溶液和I,所以G是二氧化碳,E是铁,I是氢气;氢气和氮气产生刺激性气味的M,因此M是氨气,然后将推出的物质进行验证符合转化关系。
(1)二氧化锰在过氧化氢分解中起到催化作用;故填:催化作用;
(2)在日常生活中为了避免铁的腐蚀的发生,可采取的措施是刷漆;
(3)反应④是一氧化碳和氧化铁反应产生铁和二氧化碳,方程式为3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(4)反应⑤是铁和盐酸反应产生氯化亚铁和氢气,方程式为Fe+2HCl=FeCl2+H2↑;
(5)反应⑥是氮气和氢气反应产生氨气,反应的方程式为:N2+3H2=2NH3,同温同压下不同气体的体积之比等于气体分子个数之比;故填:1:3。


科目:初中化学 来源: 题型:
【题目】化学概念在逻辑上存在如图所示关系,对下列概念的说法不正确的是( )
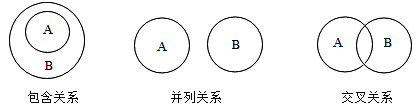
A.单质与化合物属于交叉关系B.化合物与氧化物属于包含关系
C.氧化反应与化合反应属于交叉关系D.分解反应与化合反应属于并列关系
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)“微观—宏观—符号”三重表征是化学独特的表示物质及其变化的方法。请结合图示完成下列问题:
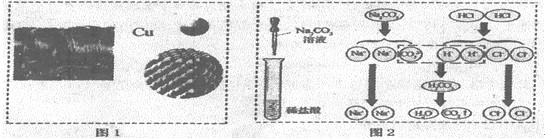
(1)图1中,“Ca”表示多种信息,如表示铜元素、金属铜单质,还能表示 ;
(2)从微粒的角度说明图2反应的实质是 ;
(3)为减少温室气体排放,人们积极寻找不含碳元素的燃料。经研究发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景。其反应的微观示意图如图3所示:
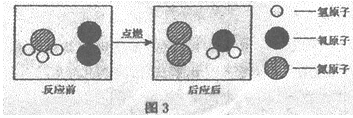
该反应的化学方程式为 ,其基本反应类型属于 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2020年奥运会奖牌制作原料来自于电子垃圾中提炼出来的金属。从废线路板中提炼贵重金属和制备硫酸铜晶体的一种工艺流程如下:
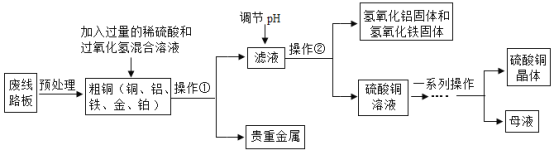
已知:在酸性环境中有过氧化氢存在时,铁和铜分别会转化为铁离子和铜离子。
(1)操作①的名称是_____;
(2)提炼出的贵金属可制作奖牌,其成分是_____;
(3)调节pH的主要目的是除去滤液中_____(填金属离子符号);写出一个符合要求的生成氢氧化铁固体的化学方程式_____,其基本反应类型为_____。
(4)写出粗铜中的铜与过氧化氢和稀硫酸的混合溶液发生反应的化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】医疗上的生理盐水中含有A、B、C、D四种元素A、B、C、D的原子序数依次增大
(1)D元素的名称是______
(2)A与B可形成原子个数比1:1的分子,其化学式为_______,该分子中B的化合价是_______
(3)A、B、C形成化合物X的名称为________,其固体溶于水时要______(填“吸热”或“放热”),在X的水溶液中滴加少量CuSO4溶液,现象是_________,A与D形成化合物Y,Y与X在水溶液中反应的化学方程式为_________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液与人们的生产、生活密切相关。
(1)将少量下列物质分别放入水中,充分搅拌,可以得到溶液的是___________(填字母)。
A 泥土 B 汽油 C 面粉 D 蔗糖
(2)如图1所示为甲、乙两种固体物质的溶解度曲线图。
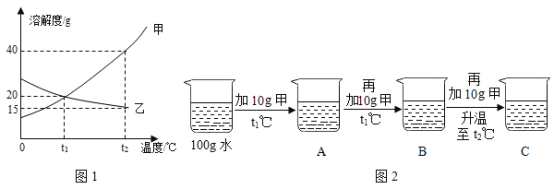
①某同学按图2进行实验,得到相应温度下的A、B、C溶液,A、B、C三种溶液中属于饱和溶液的是____________(填字母)。
②向溶液C中再加入25g甲,充分搅拌,恢复到t2℃时,所得溶液中溶质的质量分数为_________(只列出表达式)。
③将t2℃时的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液中,甲溶液的溶质质量分数____________(选填“>”“=”或“<”)乙溶液。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像中有关量的变化趋势与对应叙述关系正确的是
A.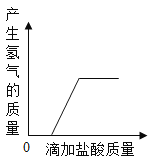 向一定质量表面生锈的铁片中滴加盐酸至过量
向一定质量表面生锈的铁片中滴加盐酸至过量
B.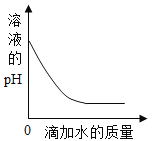 向一定质量的稀硫酸中滴加水
向一定质量的稀硫酸中滴加水
C.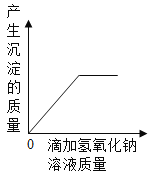 向盐酸和氯化铁的混合溶液中滴加氢氧化钠溶液至过量
向盐酸和氯化铁的混合溶液中滴加氢氧化钠溶液至过量
D.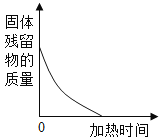 高温煅烧一定质量的石灰石
高温煅烧一定质量的石灰石
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类生活用到的食盐是从自然界获得的,但其中含大量的不溶性杂质和一些可溶杂质,如:MgCl2、Na2SO4、CaCl2。要获得较高纯度的精盐,就必须提纯。某同学设计了提纯食盐的程序,认真阅读解答下列各题。
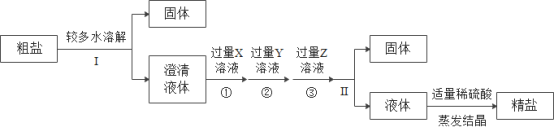
(1)图中Ⅰ、Ⅱ的操作名称是_____。
(2)除去三种可溶杂质可供选择的试剂有:Na2CO3溶液、NaOH溶液、BaCl2溶液。你认为Na2CO3溶液应该是程序中X、Y、Z中的那种_______才合理。
(3)程序中有一处加入的试剂是错误的,你准备更换成_____。(填名称)
(4)若程序中的X试剂是NaOH溶液,则加入时发生变化的化学方程为____;若X试剂是BaCl2溶液,发生变化的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组通过探究活动学习化学知识,请你一起参与探究性学习,并回答有关问题。
探究主题:水溶液中发生复分解反应的实质。
相关信息:一定体积的溶液中,离子的数目越多,其浓度越大。电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小。相同温度下同种溶液电导率越大,离子浓度越大。
(1)实验一:恒温条件下,向一定体积一定浓度的稀Ba(OH)2溶液中滴加2~3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图中甲曲线所示。
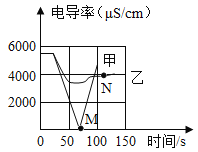
①写出反应的化学方程式:_______________。
②甲曲线M点时混合液体呈____________色。
③通过对甲曲线的分析,下列说法正确的是___________(填字母)。
A、M点前曲线下滑的过程中,H+和OH-结合成H2O,Ba2+和SO42-结合成BaSO4
B、M点时离子浓度几乎为零
C、M点后溶液电导率逐渐增大,仅由于溶液中H+数目在逐渐增大
(3)实验二:恒温条件下,向等量同浓度的稀Ba(OH)2溶液中滴加2~3滴无色酚酞试液,插入电导率传感器,然后滴加稀Na2SO4溶液,测得溶液的电导率变化如图乙曲线所示。
①通过对乙曲线的分析,下列说法错误的是___________(填字母)。
A、开始至完全反应过程中,电导率减小,溶液由红色逐渐变为无色
B、电导率下降到最低点时仍然较大,表明溶液中还存在较多离子
C、整个实验过程中,溶液中Na+数目一直增大
②N点时,溶液中含有的离子是_______________(填离子符号)。
③该实验中实际参加反应的离子是____________________。
实验结论:通过分析可知,溶液中发生复分解反应的实质是参与反应的离子结合生成了难电离的____________,导致溶液中的离子浓度_________(填“增大”或“减小”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com