
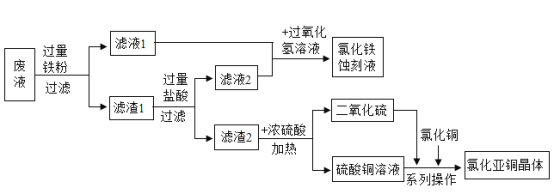
【题目】氮化亚铜(CuC1)常用作有机合成工业中的催化剂。下图是工业上用印刷电路的蚀刻液的废液(含FeCl3、CuCl2、FeCl2) 生产CuCl2的流程并制得FeCl3蚀刻液。
[资料](1)氯化亚铜是一种白色晶体,微溶于水、不溶于乙醇及稀硫酸;
(2)![]()
按要求回答下列问题:
(1)废液中加入铁粉时,滤渣1的成分是____________(填化学式)。
(2)滤液1、2合并后与过氧化氢溶液反应的化学方程式为_________________。
(3)上述流程中化合价发生改变的非金属元素有____________( 填元素符号)。分离、提纯CuCl晶体过程中的“系列操作”包括“调pH、_________洗涤、低温烘干”。为得到纯净的Cucl晶体,可用下列___________(填字母序号)进洗涤。
a.乙醇
b.蒸馏水
c.氯化钠溶液
【答案】Cu、Fe 2FeCl2+2HCl+H2O2=2FeCl3+2H2O O、S 过滤 a
【解析】
(1)废液中加入过量铁粉,氯化铁和铁粉反应生成氯化亚铁,氯化铜和铁粉反应生成氯化亚铁和铜,故滤液1为氯化亚铁溶液,滤渣1为铜和铁粉,故填:Cu、Fe。
(2)滤渣1加入过量稀盐酸,稀盐酸和铁反应生成氯化亚铁和氢气,滤液2为氯化亚铁溶和稀盐酸混合溶液,滤液1和滤液2混合后溶质是氯化亚铁和氯化氢,氯化亚铁氯化氢混合溶液和过氧化氢反应生成氯化铁,根据质量守恒,生成物中除了氯化铁以外,必须含有氢元素,氧元素,故生成物必须有水,故化学方程式为2FeCl2+2HCl+H2O2=2FeCl3+2H2O,故填:2FeCl2+2HCl+H2O2=2FeCl3+2H2O。
(3)反应过程中过氧化氢中氧元素为-1价变为了-2价,滤渣2加浓硫酸生成二氧化硫,硫元素由+6价变为+4价,化合价发生改变的非金属元素有O、S,分离、提纯CuCl晶体过程中的“系列操作”包括“调pH、过滤、洗涤、低温烘干”。为得到纯净CuCl晶体,可用下乙醇洗涤,因为CuCl在乙醇中不溶解,故填:O、S;过滤;a。


科目:初中化学 来源: 题型:
【题目】随着经济的发展,能源与环境问题日益受到人们的关注和重视。
(1)目前,人类以化石燃料为主要能源。化石燃料有煤、_____和天然气,它们都属于_____(填“可再生”或“不可再生”)能源。甲烷完全燃烧的化学方程式为_____。
(2)三大化石燃料的大量使用,会产生_____和二氧化氮等气体污染物,这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨。防治酸雨产生的措施是_____。(写出一点)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】芬太奴(C20H24N2O)是医疗上常用的麻醉剂,下列说法正确的是( )
A.芬太奴的相对分子质量是308g
B.芬太奴中含有24个氢原子
C.芬太奴中氢元素的质量分数最大
D.芬太奴是一种有机物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年7月28日中国海军“西安舰”参加了俄罗斯海军节庆典海上阅兵。建造西安舰的特种钢材需要用富铁矿石(含铁量高于50%)来冶炼。研学实践小组为测出某地赤铁矿石(主要成分是Fe2O3)中的含铁量,进行实验:取10g赤铁矿石样品,逐渐加入稀硫酸,充分反应后过滤,实验测得相关数据如图所示(假设杂质不溶于水,也不与酸反应)。
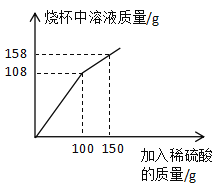
(1)该赤铁矿石样品中铁元素的质量为____g,由此可判断出该赤铁矿石属于富铁矿石。
(2)计算实验中所用稀硫酸中溶质的质量分数(写出计算过程)。
(3)溶质质量分数为10%硫酸铁溶液可用于各种工业废水与城市污水净化处理。实验中恰好完全反应后,过滤,用所得滤液配制溶质质量分数为10%的硫酸铁溶液,需要加水_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明利用下图中装置进行“硫燃烧”实验,探究硫分别在空气和氧气中燃烧的现象,下列说法错误的是
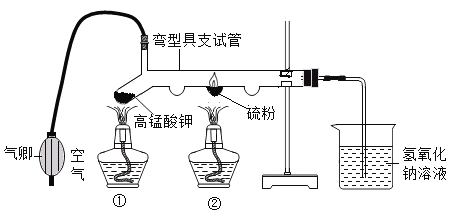
A.实验开始时先点燃酒精灯①,然后用气卿鼓入空气,再点燃酒精灯②
B.氢氧化钠和二氧化硫反应生成Na2SO3和H2O
C.该实验装置的优点之一是在同一装置中可以观察两个不同的实验现象
D.实验中可以将氢氧化钠溶液换成氢氧化钾溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学学习者常用化学思维去认识和理解世界。下列选项正确的是
A.元素是质子数相同的一类原子的总称,因此质子数相同的微粒一定属于同种元素
B.金刚石和石墨物理性质不同,是由于构成它们的原子的排列方式不同
C.依据化学方程式: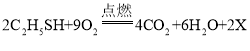 ,可推测 X 的化学式为SO3
,可推测 X 的化学式为SO3
D.探究氧化铜能否作为过氧化氢分解的催化剂,只需设计实验证明氧化铜能否改变反应速率
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】研究金属的腐蚀对资源的利用和保护意义重大。
(1)为了探究铁锈蚀的条件,进行如图 1 所示实验。
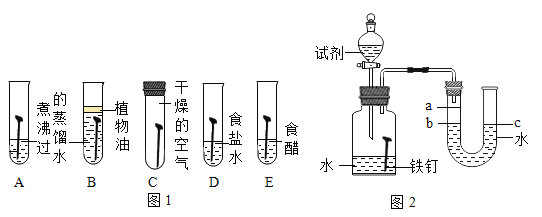
①通过观察实验 A、B、C 中的现象,经过科学严谨的推理得出结论:铁锈蚀是铁与____________发生化学反应的过程。
②实验 D 和 E 的目的是进一步探究铁在盐溶液和酸的环境中是否更容易锈蚀。铁跟醋酸(CH3COOH) 反 应生成醋酸亚铁[ (CH3COO)2Fe ]和氢气 ,请写出反应的化学方程式____________________。
(2)家中的刀具若沾有食盐水锈蚀更快。为了进一步探究影响铁锈蚀速率的因素,做了如下的实验。
(提出问题)铁锈蚀速率与哪些因素有关。
(查阅资料)氯化钠溶液能导电;乙醇溶液不能导电。
(猜想假设)铁的锈蚀速率与下列因素有关:
I._________________;
II.氧气的含量;
Ⅲ.水溶液的导电性。
(实验探究)每次取两套如图 2 所示的装置,编号为甲、乙。向两套装置中分别装入质量、大小相同的铁钉和等体积的蒸馏水,进行如下三组对比实验(实验开始时,各瓶内气体压强保持一致)。
影响 因素 | 实验设计 | 实验现象 | 实验结论及解释 |
I. | 装置甲放入 25℃恒温环境中, 装置乙放入 40℃恒温环境中。 | 两套装置中铁钉均锈蚀,且 U型管中液面均由 b 处上升至 a处,所需时间甲>乙 | ____________ |
II. | 在相同温度下,向甲、乙两套装置的集气瓶中分别通入氧气和空气。 | 铁钉均锈蚀,且 U 型管中液面由 b 处上升至 a 处,所需时间甲___________乙 | 铁的锈蚀速率与氧气的含量有关,氧气的含量越多,铁的锈蚀越快。 |
Ⅲ. | ______________________ | 两套装置中铁钉均锈蚀,且 U 型管中液面均由 b 处上升至 a 处,所需时间甲<乙 | 铁的锈蚀速率与水溶液的导电性有关,在能导电的溶液中,铁的锈蚀速率加快。 |
(反思与提高)根据该探究实验以及你所学的知识,判断下列说法正确的是___________(填序号)。
A 金属的腐蚀是指金属单质与其它物质发生化学反应的过程
B 金属腐蚀不一定要有氧气参加
C 金属越活泼,就越容易被锈蚀
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Cl2是黄绿色气体,水溶液叫氯水,把品红试纸伸入氯水中,品红试纸褪色。
[提出问题]氯水中的哪些成分能使品红试纸褪色呢?
[查阅资料]氯气溶于水,部分与水反应,方程式为![]() 。HClO(次氯酸)是一种弱酸,具有强氧化性。
。HClO(次氯酸)是一种弱酸,具有强氧化性。
[猜想假设]猜想1:氯水中的水使品红褪色;猜想2:氯水中的Cl2使品红褪色;
猜想3:氯水中的__使品红褪色;猜想4:氯水中的HClO使品红褪色。
[实验探究]
实验操作 | 实验现象 | 实验结论 |
1.把品红试纸伸入水中 | 没有褪色 | 猜想1__ |
2.____ | 没有褪色 | 猜想2不成立 |
3.把品红试纸伸入稀盐酸中 | _ | 猜想3不成立 |
[实验结论]综合分析判断:氯水中的__(填化学式)使品红褪色,具有漂白作用(能使品红等有色物质褪色)。
[拓展应用]①向氯水中滴加紫色石蕊溶液,观察到的现象是___;②氯水中加人AgNO3溶液有白色沉淀生成,化学方程式为__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示装置回答有关问题:
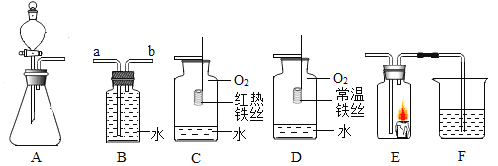
(1)装置 A 的优点是_________。
(2)若用装置 B 排水法收集氧气,气体从______________(填“a”或“b”)端导管通入瓶内。
(3)对比装置 C 和 D,可以得出可燃物燃烧的条件是______________。
(4)某同学连接 A、E、F 进行实验,A 中所加药品不同,F 中所加药品相同。
①若实验时 E 中蜡烛熄灭,F 中溶液变浑浊,则 A 中反应的化学方程式为______________;
②若实验时 E 中蜡烛燃烧更旺,F 中溶液变浑浊,则 A 中反应的化学方程式为______________;
③实验时 F 中溶液的作用是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com