
【题目】用图所示装置研究二氧化碳的性质。其中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。
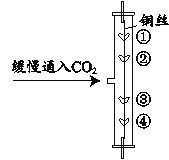
(1)说明CO2密度大于空气的实验现象为_____;除此之外,该实验还能研究的二氧化碳的性质是_____。
(2)某同学将变红了的棉球用吹风机烘干后,观察到棉球又变回紫色。但是,他认为此现象不足以说明“碳酸受热发生化学反应”,理由是_____。
 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:初中化学 来源: 题型:
【题目】2017年10月27日央视财经报道:王者归“铼”,中国发现超级金属铼,制造出航空发动机核心部件。如图是铼在元素周期表中的相关信息,下列有关说法不正确的是( )
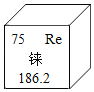
A. 铼原子的核内质子数为75 B. 铼的相对原子质量为186.2g
C. 铼的元素符号是Re D. 铼原子的核外电子数为75
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某纯碱样品中含有少量氯化钠.为测定样品中碳酸钠的质量分数,现称取该样品11g,加入到盛有50g稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为56.6g.计算:
(1)产生二氧化碳的质量是_____g
(2)纯碱样品中碳酸钠的质量分数;____
(3)反应后所得溶液中溶质的质量分数.____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用如图所示实验验证可燃物燃烧的条件。已知:白磷的着火点为40℃。
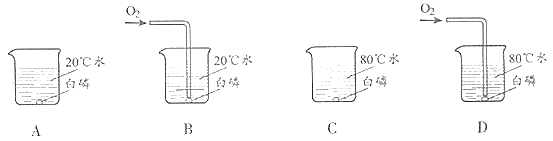
(1)设计B、D的目的是_____;对比____中的现象可以得出可燃物燃烧的另一个条件。
(2)为了防止失火造成生命财产的损害,加油站等场所常贴有图2图标,其中表示“禁止吸烟”的是______ (填字母序号)。

(3)恰当的安全措施能减少生命财产损失。下列措施正确的是_____ (填字母)。
A 燃气泄漏,立即关闭阀门并开窗通风 B 电器着火,立即用水浇灭
C 点燃氢气前,先检验气体纯度 D 住房着火,立即打开所有门窗
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】膨松剂是一种食品添加剂,它受热分解产生的气体,能使面胚在焙烤过程中变得松软、多孔。碳酸氢钠(NaHCO3)受热后发生分解反应生成二氧化碳、水和碳酸钠,是常用的膨松剂之一。它既可以作为碱性膨松剂单独使用,也可以与酒石酸氢钾、淀粉按一定比例混合制成复合膨松剂。复合膨松剂遇水会产生二氧化碳,起到膨松作用。下列说法正确的是

A. 任何受热分解能产生气体的物质都可以做食品膨松剂
B. 碳酸氢钠受热分解的化学方程式为:NaHCO3![]() CO2↑+ H2O + Na2CO3
CO2↑+ H2O + Na2CO3
C. 碳酸氢钠做膨松剂时,必须与酒石酸氢钾、淀粉混合使用
D. 复合膨松剂应在干燥的环境中保存
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染。同学们对废旧手机中的金属回收产生兴趣。

(提出问题)从废旧手机中可以回收到哪些有价值的金属?如何回收?
(查阅资料)
i.手机电路板中的金属及其价格如下表所示:
种类 | Fe | Cu | Al | Ni | Au | Ag | Pd(钯) |
市场价格($/t) | 365 | 7175.5 | 1710.5 | 14235 | 4.7×107 | 7.6×105 | 2.7×107 |
矿石中含量 | 72.4 | 0.87 | 29.1 | 1.02 | 4 | 120 | 0.4 |
手机电路板中含量 | 5 | 13 | 1 | 0.1 | 350 | 1380 | 210 |
说明:Fe、Cu、Al、Ni的含量用质量分数(%)表示,Au、Ag、Pd的含量的单位为“g/t”。
ii.Ni的金属活动性位于氢前;Pd的金属活动性位于氢后;NiCl2溶液为绿色。
Iii.2Cu+O2+2H2![]() 2CuSO4+2H2O
2CuSO4+2H2O
(实验方案)
第一步:选择值得回收的金属。
依据资料i中的数据,废旧手机中有回收价值的金属有Au、Ag、Cu、Pd,原因是:①它们的市场价格较高;②_____。
第二步:设计实验分离、回收部分金属。
序号 | 实验步骤 | 实验现象 |
I | 取一废旧手机电路板,用电吹风机靠近电路焊接点的焊锡吹热风,一段时间后,用镊子将金属电路从塑料板中拽出 | 焊锡熔化 |
II | 将金属电路放入烧杯中,加入足量稀盐酸浸泡 | _____ |
III | 取II中未溶解的金属电路,用蒸馏水洗净后,放入如图所示装置中,进行实验。
| 溶液逐渐变成蓝色,仍有微量金属固体未溶解 |
IV | 过滤III中烧杯中的物质,洗涤滤纸上的物质 | 滤纸上仍有微量金属固体 |
V | _____ | 得到红色固体 |
(问题讨论)
(1)由步骤I中的现象,可推知的焊锡的物理性质是_____。
(2)步骤II对应的实验现象是_____。
(3)步骤II所得溶液中,一定含有的金属元素是_____。
(4)步骤V的操作是_____。
(反思交流)
为了确认步骤IV中滤纸上的金属成分,应进一步查阅的资料为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】近日,网上的一段视频中一名空乘人员和一名乘客用矿泉水和咖 啡等液体,扔向起火的充电宝,最终将火扑灭。一些网友认为,电器类火灾应 该用干粉灭火器,而不是用水来直接灭火。也有一些网友认为,空乘人员处理 的没错。
(1)网友认为锂电池着火不能用水扑灭的原因是锂的化学性质非常活泼,遇 水时会与水反应生成氢气和氢氧化锂(LiOH),写出锂与水的化学方程式:______________________________。
(2)请消防员进行实验验证:消防员手拿干粉灭火器迅速的扑向起火的充电 宝。只喷了没几下,火焰就被扑灭了。然而,仅仅过了几秒钟,锂电池的残骸 再一次燃烧了起来,而且比第一次的燃烧还要猛烈。消防员对于火焰用大量清 水持续浇灭。大约一分钟左右,用红外线测温计检查充电宝的温度居然还有200 多摄氏度的高温。随后,消防员将充电宝泡入水盆中,才表示已经安全了。
①只喷了没几下,火焰就被扑灭了的灭火原理是_________________________。
②锂电池的残骸再一次燃烧了起来的原因是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上利用生产钛白的副产品硫酸亚铁制备还原铁粉的流程如图
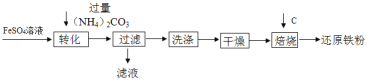
下列说法不正确的是
A. “转化”时在溶液中生成了FeCO3沉淀,该反应的基本反应类型是复分解反应;
B. “过滤”后得到的滤液中的溶质只有(NH4)2SO4;
C. “干燥”过程中有少量的FeCO3转化为FeOOH和CO2,此时与FeCO3反应的物质有O2和H2O;
D. 取14.06g还原铁粉(仅含有Fe和少量FexC)在氧气流中充分加热,得到0.22gCO2,另取相同质量的还原铁粉与足量稀硫酸充分反应(FexC与稀硫酸不反应),得到0.48gH2,则FexC的化学式是Fe3C。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验小组研究制备Cu(OH)2的条件并探究其稳定性。
(查阅资料)两种含铜化合物的部分性质如下表所示。
化合物 | Cu(OH)2 | Cu4(OH)6SO4 | CuO |
颜色 | 蓝色 | 绿色 | 黑色 |
在水中的溶解性 | 难溶 | 难溶 | 难溶 |
(进行实验)
实验1:室温下,取16%CuSO4溶液和4%NaOH溶液进行实验。
| 序号 | CuSO4溶液体积/mL | NaOH溶液体积/mL | 实验现象 |
1-1 | 2 | 2 | 产生浅绿色沉淀 | |
1-2 | 2 | 4 | 产生蓝色沉淀 混有少量浅绿色沉淀 | |
1-3 | 2 | 6 | 产生蓝色沉淀 |
实验2:将1-3所得混合物过滤,得到蓝色沉淀,将沉淀洗涤、干燥后置于恒温烘箱中,3h后观察并记录实验现象。
序号 | 2-1 | 2-2 | 2-3 | 2-4 | 2-5 |
烘箱温度/oC | 40 | 50 | 60 | 70 | 80 |
固体是否变黑 | 不变黑 | 不变黑 | 不变黑 | 变黑 | 变黑 |
实验3: 重复实验1-3,将所得混合物置于不同水浴温度下,记录实验现象。
序号 | 3-1 | 3-2 | 3-3 | 3-4 |
水浴温度/oC | 0 | 30 | 60 | 90 |
出现黑色沉淀的时间 | 1h | 3min | 25s | 2s |
(解释与结论)
(1)CuSO4溶液与NaOH溶液反应制Cu(OH)2的化学方程式为_____。
(2)实验1-1反应得到浅绿色沉淀的主要成分是______。
(3)由实验1
(4)实验2固体变黑的原因是_____(用化学方程式解释)。
(5)实验3的结论是_____。
(反思与评价)
(6)对比实验2和实验3,得出的结论是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com