
【题目】分类、类比是学习化学常用的方法。
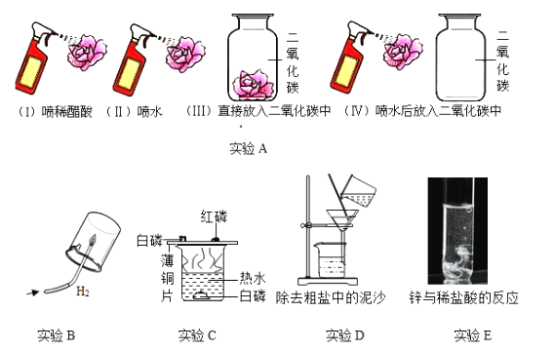
(1)初中化学实验可以按照实验目的分为:“混合物的分离提纯实验”、“探究反应条件实验”“探究物质性质实验”等。据此我们可以将实验A与实验①_____(填字母)分为一类,分类依据是②_____。
(2)在金属活动性顺序中,排在前面的“钾、钙、钠”三种金属与盐溶液接触时先与溶液中的水反应生成碱和氢气。已知金属钾与水反应的化学方程式为:2K+2H2O═2KOH+H2↑.现将金属钠加入硫酸铜溶液中,请写出发生总反应的化学方程式为①_____。金属钠很容易被空气中的氧气氧化,由此推测实验室保存金属钠的注意事项是②_____。
【答案】BE 都是探究物质化学性质的实验 2Na+2H2O+CuSO4═Na2SO4+Cu(OH)2↓+H2↑ 与水和空气隔绝
【解析】
解:(1)A实验是通过颜色变体探究物质的化学性质;B实验是探究氢气的可燃性性质;C实验是探究燃烧的条件;D实验是过滤实验操作;E实验是根据锌与盐酸的反应来探究锌的化学性质;由此可知,B和E两个实验都与A实验相似,都是探究物质化学性质的实验;
故填:BE;都是探究物质化学性质的实验;
(2)由题目信息可知,“钾、钙、钠”三种金属与盐溶液接触时先与溶液中的水反应生成碱和氢气,然后再与盐反应,故将金属钠加入硫酸铜溶液中,反应物有钠、水、硫酸铜,生成物是氢氧化铜、硫酸钠和氢气;发生总反应的化学方程式为:2Na+2H2O+CuSO4═Na2SO4+Cu(OH)2↓+H2↑;金属钠能与水反应,且很容易被空气中的氧气氧化,由此推测实验室保存金属钠的注意事项应该是使钠与水和空气隔绝;
故填:2Na+2H2O+CuSO4═Na2SO4+Cu(OH)2↓+H2↑;与水和空气隔绝。


科目:初中化学 来源: 题型:
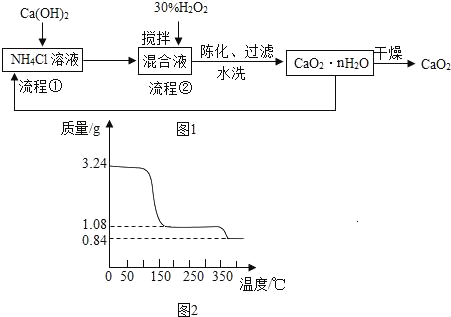
【题目】过氧化钙(CaO2)是一种白色、无毒、难溶于水的固体,加热至350℃左右开始分解放出氧气。过氧化钙能杀菌消毒,广泛用于果蔬保鲜、空气净化、污水处理等方面。其工业制备的主要流程如图1:
已知:CaCl2+H2O2+2NH3+nH2O=CaO2nH2O↓+2NH4Cl。
(1)搅拌的目的是_____。
(2)流程②中没有采用加热措施的可能原因是_____。
(3)整个流程中,除水外还可以循环使用的物质是_____。
(4)过滤操作中需要的玻璃仪器有漏斗、烧杯和_____,该仪器的作用是_____,检验CaO2nH2O是否洗涤干净的方法是_____。
(5)取上述制得的CaO2nH2O晶体进行热重分析,其热分解时晶体的质量分数随温度变化的曲线如图2,通过计算可得出n=_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学为了测定生铁样品中铁的质量分数,将60g 稀盐酸分3次加入到盛有4g 该样品的烧杯中(样品中只有铁与稀盐酸反应),所得数据如表,则下列说法中正确的是( )
实验次数 物质质量 | 第1次 | 第2次 | 第3次 |
加入稀盐酸的质量/g | 20 | 20 | 20 |
充分反应后剩余固体的质量 | 2.6 | 1.2 | 0.1 |
A. 第1次和第2次产生氢气的质量不同
B. 第2次和第3次剩余固体中均有铁
C. 第3次充分反应后溶液中溶质只有FeCl2
D. 生铁样品中铁的质量分数为97.5%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列应用、原理(用化学方程式表示)以及基本反应类型均正确的是( )
A. 用磁铁矿石炼铁 4CO+Fe3O4![]() 3Fe+4CO2 置换反应
3Fe+4CO2 置换反应
B. 溶洞的形成 Ca(HCO3)2=CaCO3↓+H2O+CO2↑ 分解反应
C. 探究铜和银的活动性 Cu+2AgCl=2Ag+CuCl2 置换反应
D. 用含有氢氧化铝的药物治疗胃酸过多症 Al(OH)3+3HCl=AlCl3+3H2O 复分解反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列应用合理,反应的化学方程式及基本反应类型都正确的是( )
A. 比较铜和银的活动性Cu+Ag(NO3)2═Cu(NO3)2+Ag 置换反应
B. 用纯碱制烧碱:2KOH+Na2CO3═K2CO3+2NaOH 复分解反应
C. 用含氢氧化铝的药物治疗胃酸过多症:3HCl+Al(OH)3═AlCl3+3H2O 复分解反应
D. 用过氧化氢溶液制氧气:H2O2═H2O+O2↑ 分解反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有A、B、C、D、E五种初中化学常见的物质,其中B、D是由三种元素组成的化合物,C、E是由两种元素组成的化合物,C在通常状况下为气体,A的粉末是黑色的,D可以用来配置波尔多液,D、E含有相同的两种元素。用两圆间的短线“﹣”表示两种物质可以发生化学反应,箭头“→”表示一种物质能转化为另一种物质。请回答下列问题:(以上反应均在初中知识范围内)

(1)在图中标出C和D物质的化学式________;
(2)写出B和E反应的化学方程式为_____;
(3)过量A与B反应的实验现象为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水和溶液在生产、生活中起着十分重要的作用,请回答下列问题。
(1)自来水厂主要通过①沉淀②吸附③过滤④投药消毒(用漂白粉等)等对自然水进行净化,其合理的步骤顺序是_____(填序号);可用_____来检测水的酸碱度是否达到标准
(2)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。
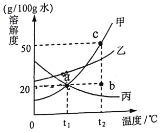
①t1℃时,甲、乙、丙三种物质的溶解度大小关系_____。
②t1℃时,完全溶解5g丙物质至少需要水_____g。
③t2℃时,将20g甲加入到100g水中,充分搅拌后所得溶液是甲的_____溶液(填“饱和”或“不饱和”),可以用图中_____点(填“a”、“b”、“c”)表示。
④将甲、丙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述不正确的是_____。
A都是饱和溶液 B溶剂质量:甲<丙
C析出固体质量:甲>丙 D溶质质量分数:甲=丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表是KNO3、NaCl在不同温度下的溶解度。
温度(℃) | 0 | 20 | 30 | 40 | 60 | 80 | |
溶解度 | KNO3 | 13.3 | 31.6 | 45.8 | 63.9 | 110 | 169 |
NaCl | 35.7 | 36.0 | 36.3 | 36.6 | 37.3 | 38.4 | |
(1)根据表中的数据,在坐标纸上绘制出氯化钠和硝酸钾两种物质的溶解度曲线。(在答题卡的坐标纸上绘图)____
①两种物质中,溶解度受温度的影响变化较大的是_____。
②根据绘制的溶解度曲线可知,50℃时,硝酸钾的溶解度约为_____。
③将接近饱和的KNO3溶液转化为饱和溶液的一种方法是_____。
④从较浓的NaCl溶液中得到NaCl晶体,较好的方法是_____(填“蒸发结晶”或“降温结晶”)。
(2)A是80℃含有120g水的KNO3溶液,经过如下操作,得到102gKNO3固体。
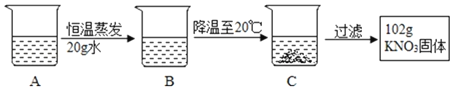
①A溶液为_____(选填“饱和”或“不饱和”)溶液。
②对以上过程的分析,正确的是_____(选填编号)。
a.A到B的过程中,溶质质量没有改变
b.B中溶质与溶剂的质量比为169:100
c.开始析出KNO3固体的温度在60℃至80℃之间
d.A溶液的质量等于222g
(3)烧杯内原有某物质,向其中加入物质X,X的质量与变量Y的关系如图,下列一定能正确反映X、Y对应关系的是_____。
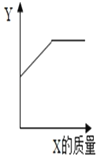
选项 | 烧杯内原有物质 | X | Y |
A | NaCl饱和溶液 | NaCl固体 | NaCl溶液的溶质质量分数 |
B | 水 | NH4NO3固体 | 溶液的温度 |
C | 氯化亚铁溶液 | 锌粉 | 溶液的质量 |
D | 稀硫酸 | 铁粉 | 溶液中氢元素的质量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com