
【题目】空气的主要成分是氧气和氮气。
(1)空气属于________(填“混合物”或“纯净物”)。
(2)用“”表示氮原子,“●”表示氧原子。
①用“![]() ”可表示的微粒是______(填名称)。
”可表示的微粒是______(填名称)。
②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,如图可表示空气微观模型的是____(填标号)。

(3)下图是氧元素在元素周期表中的信息及微粒结构示意图。
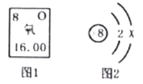
①从图1中可获得多条信息,其一是__________。
②若图2中表示氧原子,在化学反应中,氧原子容易______(填“得”或“失”)电子。
③若图2中,x=8时,该微粒是_________(写微粒符号)。
(4)以下是利用空气制取氮肥过程中重要的一步化学反应微观示意图。
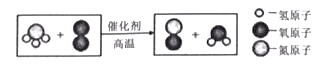
①该反应的化学方程式是________。
②物质所含元素化合价发生变化的反应属于氧化还原反应。该反应_______(填“属于”或“不属于”)氧化还原反应。
【答案】 混合物 氮分子 C 氧的相对原子质量为16.00 得 O2- 4NH3+5O2![]() 4NO+6H2O 属于
4NO+6H2O 属于
【解析】(1)空气中含有氧气、氮气、二氧化碳等物质,属于混合物;
(2)①分子是由原子构成的,用“![]() ”可表示的微粒是氮分子;
”可表示的微粒是氮分子;
②同温同压下,气体的体积比等于分子数目比。氧气约占空气体积的1/5,若空气中其它成分忽略不计,微观上氮分子与氧分子的个数比为4:1,图中可表示空气微观模型的是C;
(3)①元素周期表中包含信息较多,例如氧的相对原子质量为16.00、氧元素的元素符号为O、质子数为8等;
②氧原子的最外层电子数是6,可知氧原子在化学反应中容易得到两个电子形成稳定结构;
③若图2中,x=8时,电子数=2+8=10>质子数=8,该微粒是离子,可表示为:O2-;
(4)①由微观示意图可知,反应是氨气和氧气在高温和催化剂的作用下生成一氧化氮和水,其反应的化学方程式为4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
②氮元素反应前化合价为-3价,反应后化合价为+2价,氧元素反应前化合价为0价,反应后化合价为-2价,属于氧化还原反应。


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:初中化学 来源: 题型:
【题目】如图是自然界中碳、氧循环简图(X为H2CO3,Y为C6H12O6)。下列说法不正确的是

A. 图一中的转化1是酸雨形成的主要原因
B. 图二中可实现有机物与无机物的相互转化
C. 绿色植物通过光合作用,将太阳能转化成化学能
D. 碳循环和氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组利用废硫酸液制备K2SO4并研究CaSO42H2O加热分解的产物。
(一)K2SO4的制备
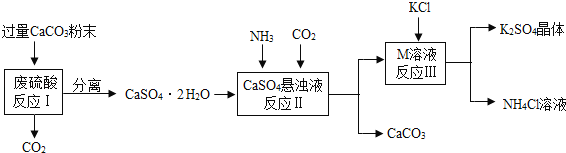
(1)将CaCO3研成粉末的目的是___________________________________。
(2)M物质的化学式为__________。
(3)反应Ⅲ中相关物质的溶解度如下表。
物质 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
反应Ⅲ在常温下能实现的原因是_______________________________________。
(4)上述流程中可循环使用的物质有CO2和_____________(填写化学式)。
(二)研究CaSO42H2O加热分解的产物
(5)分离出的CaSO42H2O中常含有CaCO3,可用盐酸除去CaCO3,
该反应的化学方程式_______________________________________________。
(6)为了测定CaSO42H2O和CaCO3的质量比x:y,实验小组利用如图所示的装置(夹持仪器省略)进行实验。注:碱石灰的主要成分为NaOH和CaO。
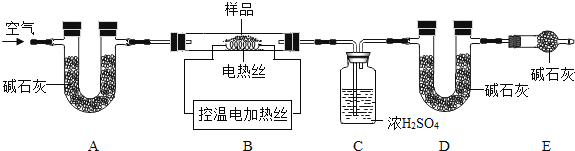
① 实验前首先要________________,再装入样品。装置A的作用是_________________。
② 已知:CaSO42H2O在160℃生成CaSO4,1350℃时CaSO4开始分解; CaCO3在900℃时分解完全。
现控制B装置温度900℃进行实验并采集了如下数据:
a.反应前玻璃管与样品的质量m1g b.反应后玻璃管中固体的质量为m2g
c.装置C实验后增重m3g d.装置D实验后增重m4g
某同学选用b、d或c、d数据组合求出x:y的值,若无装置E,则实验测定结果将______。(填“偏大”、“偏小”或“无影响”)你认为还可选用上述的________________(选填序号)两个数据组合也可求出x:y的值。
(7)CaSO42H2O受热会逐步失去结晶水。取纯净CaSO42H2O固体3.44g,放在(5)的实验装置B中进行加热,测定固体质量随温度的变化情况如图所示。
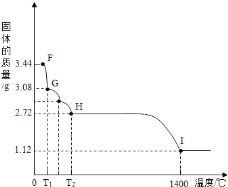
则G点固体的化学式是_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表列出了部分元素原子结构示意图。下列叙述错误的是
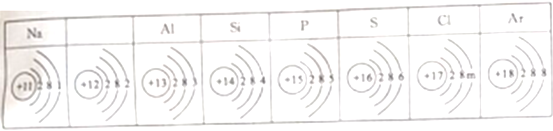
A. 在不显电性的情况下,表中m的值为7
B. 如果失去第三层电子,上表空格内的微粒符号可表示为Mg2+
C. 上表中所列元素在元素周期表中属于同一周期
D. 钠原子在化学反应中易得电子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是A、B、C三种固体物质的溶解度曲线,请根据图示回答:
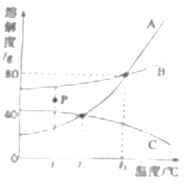
(1)t3℃时,将60gB物质加入到50g水中,充分搅拌后,所得溶液的质量是_________g。
(2)图中P点所表示的B物质的溶液为_________(填“饱和”或“不饱和”)溶液,欲将t1℃时C物质的不饱和溶液变为饱和溶液,可采用的方法是__________(任写一种)。
(3)将t2℃时A、B、C三种物质的饱和溶液分别升温到t3℃(忽略水的蒸发),三种溶液的溶质质量分数由大到小的顺序是___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )
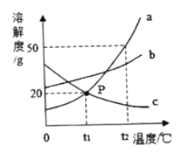
A. t2℃时,a,b,c三种物质的溶解度由大到小的顺序是a>b>c
B. t2℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液
C. t1℃时a,b,c三种物质的溶液中溶质质量分数关系是b>a=c
D. 从a、c的混合溶液中提取a物质,可采用降温结晶的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用适当的化学方程式说明或解释下列问题:
(1)用石灰浆粉刷墙面,干燥后变得坚硬_______________________________
(2)服用Al(OH)3的药丸治疗胃酸过多症_________________________
(3)生活中铝锅表面易形成有较强的抗腐蚀性的氧化膜 _____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】盐酸是实验室常用的试剂,也是重要的化工原料,茜茜同学归纳出盐酸的五条化学性质(如图1所示,连线表示相互反应);林林同学为表示反应实质绘制了图2。
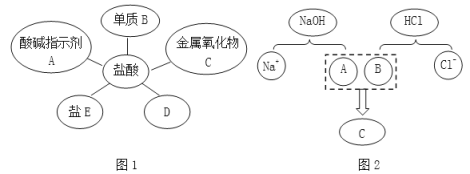
请根据图示回答下列问题。
(1)如图1所示。①若将紫色石蕊溶液滴加到盐酸溶液中,溶液变__________色。
②B不可能是__________(填序号)。 a.Mg b.Fe c.Ag d.Zn
③若C为铁锈,C与盐酸反应的化学方程式是__________。
④D所表示的物质类别是__________。
⑤若E为碳酸钠,D与E反应的化学方程式是__________。
(2)如图2所示。该图描述了氢氧化钠溶液与盐酸反应的微观实质,在图2中,A、B、C处应填入微粒的化学式依次为__________,写出该反应的化学方程式__________。
(3)向稀盐酸中分别逐渐加入下列物质,溶液pH几乎不发生变化的是__________(填序号)。A.AgNO3固体 B.浓盐酸 C.Ca(OH)2固体 D.H2O
(4)完全中和一定量的某盐酸溶液,需要50g 8%的NaOH溶液,若改用50g 8%的KOH溶液,则反应后溶液的pH__________7(填“>”、“=”或“<”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁是目前世界上使用最多的金属。
(1)认识铁:从宏观看,铁由___________组成;从微观看,铁由___________构成。
(2)生活中:下图是常用的铁锅。把铁制成铁锅利用了铁的延展性和___________性。为防止铁制品锈蚀,可采用的一种防锈方法是___________。
![]()
(3)实验室:细铁丝在氧气中燃烧的现象是________________,放热。该反应的化学方程式是_________________________________。
(4)工业上:用一氧化碳和赤铁矿(主要成分是Fe2O3)炼铁的化学方程式是__________,该反应利用了一氧化碳的哪种化学性质:______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com