
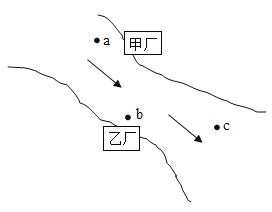
【题目】甲、乙两化工厂分布在某排污渠两岸(如图所示),箭头代表水流方向。若甲厂附近a处水样经检测含有的阴离子是OH-、SO42- ,c处水样经检测pH=7且只含有少量的NaCl,则乙厂排放到b处水中的物质可能是( )
A.BaCl2、HC1
B.H2SO4、Ba(NO3)2
C.MgSO4、NaCl
D.BaCl2、Mg(NO3)2
【答案】A
【解析】
A、a处水样经检测含有的阴离子是OH-、SO42- ,c处水样经检测pH=7且只含有少量的NaCl,如果b处水中的物质是氯化钡、HCl,a处是氢氧化钠和硫酸钠,则氢氧化钠和盐酸反应生成氯化钠和水,硫酸钠和氯化钡反应生成硫酸钡沉淀和氯化钠,如果恰好完全反应,则c处只有氯化钠,且pH=7,符合题意;
B、如果b处水中的物质是H2SO4、Ba(NO3)2,氢离子能与氢氧根离子结合成水,钡离子能与硫酸根离子结合成硫酸钡沉淀,但是硝酸根离子无法形成沉淀,故c处一定含硝酸根离子,与事实不符,不符合题意;
C、如果b处水中的物质是MgSO4、NaCl,镁离子可以和氢氧根离子结合成氢氧化镁沉淀,硫酸根离子能和钡离子结合成沉淀,但是a处不可能有钡离子,因为钡离子和硫酸根离子不能共存,不符合题意;
D、如果b处水中的物质是BaCl2、Mg(NO3)2,钡离子可和硫酸根离子结合成沉淀,镁离子可和氢氧根离子结合成沉淀 ,但是硝酸根离子无法形成沉淀,故c处一定含硝酸根离子,与事实不符,不符合题意。
故选A。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】A、B、 C、D是初中化学常见的四种不同类别的化合物,其中有一种物质中含有人体中含量最多的金属元素,C和D反应时能生成厨房中常用的一种调味品的主要成分。它们之间的反应和转化关系如图所示(“一”表示两物质能发生化学反应,“→”表示一种物质经一步反应可转化为另一种物质,部分反应物、生成物及反应条件已略去)。回答下列问题。
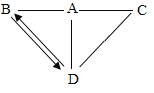
(1) B物质的名称_____。
(2)写出A和D反应的化学方程式_____。
(3)写出A和C的化学方程式_____。
(4)写出A物质的一种用途_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“喝酒不开车,开车不喝酒”。酒中含有乙醇(C2H6O),交通警察执法时让开车者对着便携式酒精检查仪吹气,便携式酒精检查仪内部发生反应的原理为:2K2Cr2O7(橙色) + 3C2H6O+8H2SO4 = 2Cr2(SO4)3(蓝绿色)+3C2H4O2+2K2SO4+11X,据该反应回答下列问题:
(1)如果司机饮了酒,交警观察到仪器内部药品发生反应的现象是______。
(2)便携式酒精检查仪中的铬(Cr)元素在检查前后的质量____(填“增加”、“减少”、“不变”)。
(3)该反应生成物中X的化学式为_____。
(4)Cr元素的化合价在反应前后的变化是______(填由多少价变到多少价)。
(5)乙醇也是一种燃料,在空气中完全燃烧生成水和二氧化碳。乙醇在空气中完全燃烧的化学方程式为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是一种常见水壶,请回答下列问题:

(1)酚醛塑料手柄属于_____材料(选填“合成”“天然”),它具有的性质是_____(选填“热固性”“热塑性”)
(2)不锈钢外壳属于_____(选填“复合材料”“金属材料”)。
(3)这种水壶中含有地壳中含量第二多的金属元素,其元素符号是_____。
(4)水壶烧水后结水垢,水垢的主要成分是Mg(OH)2和_____。可以用盐酸去除水垢,写出其中发生的中和反应的化学方程式_____。
(5)有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与C发生中和反应,D与A反应有CO2气体产生。
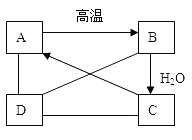
①请根据已知条件推断四种物质的化学式:
A_____B_____C_____D_____。
②请写出B与D反应的化学方程式:_____。
(6)下面是某同学对所学物质的分类归纳,请仔细分析并回答下列问题:
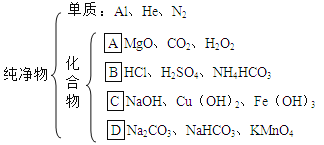
①写出C组物质所属的类别_____。
②在分类所列举的物质中,有一种物质归类错误,这种物质是_____。
③A组物质中的MgO中的阳离子符号为_____。
④D组物质KMnO4中Mn的化合价为_____。
⑤在分类所列举的物质中,单质铝能与足量氢氧化钠溶液反应,方程式为2Al+2NaOH+2H2O=2NaAlO2+3X↑,则X的化学式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们在初中化学实验室中,发现一瓶如图所示久置的无色溶液,瓶口有白色固体、瓶塞丢失,已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定原溶液成分,同学们进行了如下探究:
![]()
(1)小张同学取待测液测得pH=10,他得出的关于溶液成分的结论是_____。他取少量待测液于试管中,加入过量的稀HCl,看到_____,由此小张同学认为该溶液为Na2CO3溶液。
(2)小李同学对小张同学的结论提出疑问,由此进行了以下实验:取少量待测液于试管中,加入过量的CaCl2溶液,生成白色沉淀,该反应方程式为_____,静置,(写出还需进行的操作及现象)_____。
通过实验,小李认为小张结论正确。
二位同学给试剂瓶贴一新标签:Na2CO3。
(3)实验结束后,同学们通过讨论认为试剂瓶原标签仍有可能不是Na2CO3,你猜测他们认为该试剂瓶原标签上的化学式可能是_____;你的理由是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A~F是初中化学常见的几种物质,它们之间存在下图所示的反应关系(图中“一”表示两端的物质在一定条件下能反应,“→” 表示转化关系,且图中反应均为初中常见的反应),其中A、D、E、F是四种不同类别的物质,A是常用于改良酸性土壤的碱,A、B、C含有相同的金属元素,D的溶液显蓝色,E与F反应得到浅绿色溶液,F由两种元素组成。请回答下列问题:
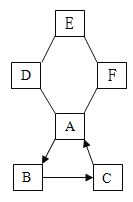
(1)写出E的化学式________。
(2)F的一种用途_______。
(3)用化学方程式表示A→B的反应______。
(4)图中的反应与转化中涉及四种基本反应类型中的______种。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组的同学对“锌与硫酸反应速率的影响因素”进行探究,并利用如图装置收集产生的氢气。
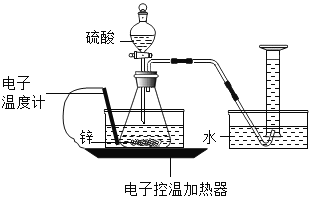
(查阅资料)
圆粒状锌的直径通常为 3-4 毫米,粉末状锌的直径通常为 0.3-0.5 毫米。
(进行实验)
实验 1:在不同温度下,进行锌与硫酸反应的实验。
编号 | 温度/℃ | 硫酸体积/ mL | 硫酸溶质质量分数 | 锌的形状 | 锌的质量 /g | 收集30mL氢气所用的时间/s |
1-1 | 20 | 20 | 10% | 圆粒状 | 1 | 170 |
1-2 | 30 | 20 | 10% | 圆粒状 | 1 | 134 |
1-3 | 40 | 20 | 10% | 圆粒状 | 1 | 107 |
实验 2:在相同温度下,继续进行锌与硫酸反应速率的影响因素的探究。
编号 | 温度/℃ | 硫酸体积/ mL | 硫酸溶质质量分数 | 锌的形状 | 锌的质量 /g | 收集30mL氢气所用的时间/s |
2-1 | 20 | 20 | 10% | 圆粒状 | 1 | 170 |
2-2 | 20 | 20 | 10% | 粉末状 | 1 | 47 |
2-3 | 20 | 20 | 20% | 圆粒状 | 1 | 88 |
2-4 | 20 | 20 | 20% | 粉末状 | 1 | 26 |
(解释与结论)
(1)锌与硫酸反应的化学方程式为_____ 。
(2)能用排水法收集氢气的原因是氢气_____(填“易”或“难”)溶于水。
(3)实验 1 的目的是_____。
(4)实验 2 中,欲得出“其他条件相同时,硫酸的溶质质量分数越大,锌与硫酸反应的速率越快”的结论,需要对比的实验_____(填编号)。
(5)实验 2 中,通过对比 2-1 和 2-2,得出的结论是_____。
(反思与评价)
(6)实验室制取氢气时,通常使用锌粒而不用锌粉的原因为_____。
(7)实验室中若使用 6.5g 锌粒制取氢气,理论上制得氢气的质量为_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)用化学用语填空
①4个氨分子_____;
②3个氢氧根离子_____;
③水银_____;
④氦气_____;
⑤KIO3中碘元素的化合价_____。
(2)写出三大化石燃料中,较清洁燃料燃烧的化学方程式_____。
(3)元素周期表中原子序数为 1、8、20 的元素组成物质的化学式为_____。
(4)如图①②中属阳离子的是_____( 填离子符号),该元素的质子数为_____;17 号元素位于元素周期表第_____周期。
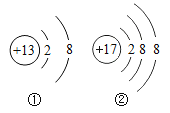
(5)已知 R、M 两种元素离子 R+和 M2-核外电子数相同,且R的核电荷数为 11,则 M原子的质子数为_____。
(6)二氧化碳和氢气在一定条件下转化为化工原料乙烯(C2H4),是我国科学研究的又一重大突破,其反应化学方程式为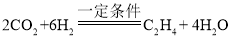
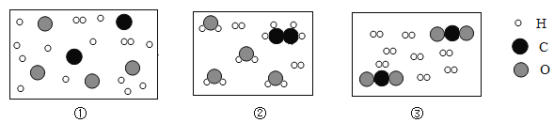
其反应微观过程可以表示为:
请将下图对应序号填入上述反应微观过程的对应框图内_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com