
分析 根据金属活动性可知,金属银不能与稀硫酸发生反应,而锌与稀硫酸放出氢气;固体质量不再减少,可判断锌已完全反应,反剩余固体为不能反应的银;混合物粉末的质量与银的质量差即反应所消耗锌的质量,利用该质量计算出反应生成的氢气的质量.
解答 解:(1)该混合物粉末中银的质量分数=$\frac{5.25g}{15g}$×100%=35%;
混合物中锌的质量分数为:1-35%=65%;
(2)混合物中金属锌的质量=15g-5.25g=9.75g
设生成氢气的质量为的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
9.75g x
$\frac{65}{2}=\frac{9.75g}{x}$
x=0.3g
答:(1)该混合物粉末中银的质量分数是35%,锌的质量分数为65%;
(2)生成氢气的质量为0.3g.
点评 根据金属的活动性,分析题中所发生的反应,判断出所余固体为银,此为本题的突破口.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
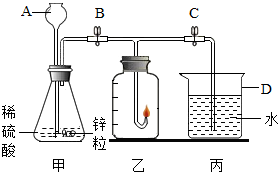 某化学兴趣小组的同学准备用氢气燃烧法测定空气中氧气的体积分数,设计的实验装置如图:
某化学兴趣小组的同学准备用氢气燃烧法测定空气中氧气的体积分数,设计的实验装置如图:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
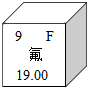 火山灰中含有高浓度的氟,会对人类和其他生物的健康造成很大影响.元素周期表中氟元素的相关信息如图,下列说法正确的是( )
火山灰中含有高浓度的氟,会对人类和其他生物的健康造成很大影响.元素周期表中氟元素的相关信息如图,下列说法正确的是( )| A. | 氟原子的核外电子数为19 | B. | 氟属于金属元素 | ||
| C. | 氟原子的中子数为9 | D. | 氟原子的质子数为9 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 琥珀酸亚铁由4个C原子、4H个原子、4个O原子、1个Fe原子构成 | |
| B. | 琥珀酸亚铁由4种元素组成 | |
| C. | 琥珀酸亚铁中C、O两种元素的质量比为1:1 | |
| D. | 琥珀酸亚铁的相对分子质量为172g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
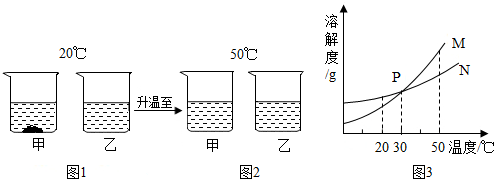
| A. | 图1中甲溶液溶质质量分数比乙溶液大 | |
| B. | 图2中甲、乙溶液一定都是饱和溶液 | |
| C. | 图3中表示甲的溶解度曲线是M | |
| D. | 30℃时,甲、乙溶液溶质质量分数不相等 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com