
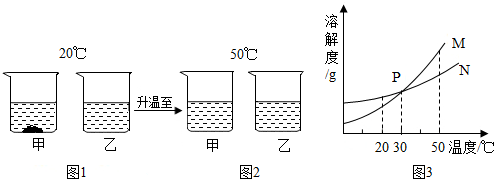
| A. | 图1中甲溶液溶质质量分数比乙溶液大 | |
| B. | 图2中甲、乙溶液一定都是饱和溶液 | |
| C. | 图3中表示甲的溶解度曲线是M | |
| D. | 30℃时,甲、乙溶液溶质质量分数不相等 |
分析 A、根据图1中,溶剂质量相等,甲物质溶解的质量小于乙物质进行分析;
B、根据图2中无溶质剩余,无法判断是否是饱和溶液进行分析;
C、图1中20℃时,将等质量的甲、乙两种固体物质(不含结晶水),分别加入到盛有100g水的烧杯中,甲有固体剩余,说明甲的溶解度小于乙,结合图3完成解答;
D、根据30℃时,甲、乙溶液是否达到饱和状态不能确定进行分析.
解答 解:A、图1中,溶剂质量相等,甲物质溶解的质量小于乙物质,所以乙溶液溶质质量分数比甲溶液大,故A错误;
B、图2中无溶质剩余,无法判断是否是饱和溶液,故B错误;
C、根据图1中信息可以知道20℃时甲的溶解度小于乙的溶解度,而图3中在20℃时,N曲线的溶解度大于M曲线的溶解度,故M表示甲的溶解度曲线,故C正确;
D、30℃时,甲、乙溶液是否达到饱和状态不能确定,所以甲、乙溶液溶质质量分数也不能确定,故D错误.
故选:C.
点评 本题首先要熟记和理解固体溶解度曲线及其使用,溶质质量分数及其有关计算,饱和溶液和不饱和溶液的概念及其相互转变方法,以及物质的溶解和结晶的方法等相关知识;然后,根据所给的问题情景或图表信息,结合所学的相关知识和技能按照题目的要求,认真地进行选择或解答即可.


科目:初中化学 来源: 题型:选择题
| A. | 升高溶液温度 | B. | 降低溶液温度 | ||
| C. | 等温蒸发适量溶剂 | D. | 加入适量Ca(OH)2固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ②④ | B. | ②③④⑥ | C. | ③④⑤ | D. | ①②④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | HCl、NaOH、CuSO4、KCl | B. | KCl、AgNO3、HCl、HNO3 | ||
| C. | CuSO4、NaCl、KNO3、BaCl2 | D. | BaCl2、Na2SO4、Na2CO3、NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
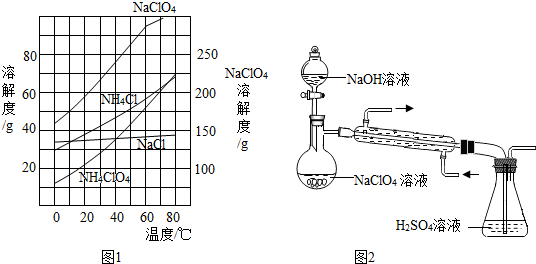
 某课外活动小组同学用图装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体).实验过程是:
某课外活动小组同学用图装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体).实验过程是:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸雨的pH小于7,pH小于7的雨水不一定是酸雨 | |
| B. | 向某无色溶液中滴加酚酞无现象,则溶液一定呈中性 | |
| C. | 在同一化合物中,金属元素显正价,则非金属元素一定显负价 | |
| D. | 酸碱中和反应生成盐和水,则生成盐和水的反应一定是中和反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com