
| A. | 先偏向左边,最后平衡 | B. | 先偏向左边,最后偏向右边 | ||
| C. | 一直平衡 | D. | 先偏向右边,最后偏向左边 |
分析 首先计算生成二氧化碳的质量,通过比较生成二氧化碳的质量,可以知道烧杯内剩余物质的质量的大小,从而确定天平指针向哪个方向偏转.
解答 解:设碳酸钙和碳酸钠的质量均为x,与稀盐酸反应生成二氧化碳的质量分别为y、z.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x y
$\frac{100}{44}=\frac{x}{y}$,y=$\frac{11x}{25}$
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x z
$\frac{106}{44}=\frac{x}{z}$
,z=$\frac{22x}{53}$<$\frac{11x}{25}$说明右边加入碳酸钠的烧杯内产生的二氧化碳少,烧杯内剩余的物质多.
因此右边质量大,右边下沉,指针偏向右边.
故选B.
点评 本题主要考查化学方程式的计算和溶液质量的变化.


科目:初中化学 来源: 题型:选择题
| A. | 两个氮气分子:2N2 | |
| B. | 2N2-2个氮气分子 | |
| C. | 臭氧中氧元素的化合价:$\stackrel{-2}{{O}_{3}}$ | |
| D. | 一氧化碳使氧化铁还原成铁的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 液氧(O2)作为助燃剂使用 | |
| B. | 使用硝酸(HNO3),作为农作物生长的氮肥 | |
| C. | 干冰(CO2)用于人工降雨 | |
| D. | 在豆浆中加入石膏(CaSO4),可以制成豆腐 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用汽油除去衣服上的油渍 | B. | 用洗涤剂除去餐具上的油污 | ||
| C. | 用食醋除去水壶中的水垢 | D. | 用盐酸除去铁栏杆上的铁锈 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | SO42-、Cl-、Na+、K+ | B. | K+、SO42-、Cu2+、N03- | ||
| C. | NH4+、Cl-、SO42-、Na+ | D. | Ca2+、Cl-、CO32-、Na+ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是家庭用电熨斗构件示意图,据图回答下列问题:
如图是家庭用电熨斗构件示意图,据图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:推断题
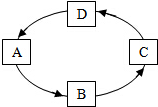 已知A、B、C、D均为初中化学中最常见的物质,它们之间存在如图所示的转化关系,其中A为最常见的溶剂.
已知A、B、C、D均为初中化学中最常见的物质,它们之间存在如图所示的转化关系,其中A为最常见的溶剂.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
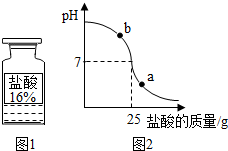
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com