
【题目】某工厂产生的烧渣(主要含FeO、Fe2O3,还有一定量的SiO2)可用于制备七水合硫酸亚铁晶体(FeSO4 ·7H2O),其工艺流程如下:

查阅资料:SiO2不溶于水,也不与稀硫酸反应。
⑴ “浸取”步骤中,FeO、Fe2O3和稀硫酸发生反应的化学方程式分别为FeO+H2SO4=FeSO4+H2O、__________________。
⑵ 过滤用到的玻璃仪器有______________。
⑶ “还原”步骤是将Fe3+转化为Fe2+,试剂X可用SO2或Fe。
① 若试剂X是SO2,转化原理为SO2+Fe2(SO4)3+2H2O=2FeSO4+2Y,则Y的化学式是:____________。
② 若试剂X是Fe,转化原理的化学方程式为______________________。
测得“还原”后溶液的pH明显增大,其原因是______________________。
【答案】Fe2O3+3H2SO4═Fe2(SO4)3+3H2O 烧杯、玻璃棒和漏斗 H2SO4 Fe+Fe2(SO4)3=3FeSO4 铁消耗过量的硫酸,导致溶液酸性减弱
【解析】
(1)“浸取”步骤中,FeO和稀硫酸发生复分解生成硫酸亚铁和水,Fe2O3和稀硫酸发生复分解反应生成硫酸铁和水,化学方程式分别为FeO+H2SO4=FeSO4+H2O、Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
(2)“过滤”操作需要使用的玻璃仪器有烧杯、玻璃棒和漏斗;
(3)①由质量守恒定律可知,反应前后,原子个数不变,反应的化学方程式为:SO2+Fe2(SO4)3+2H2O═2FeSO4+2H2SO4,则Y的化学式是H2SO4;
②若试剂X是Fe,转化原理的化学方程式为Fe+Fe2(SO4)3=3FeSO4;测得“还原”后溶液的pH明显增大,其原因是铁消耗过量的硫酸,导致溶液酸性减弱。


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁是初中化学中常见的物质,其中丙为单质,其余三种物质均为化合物,甲、乙两种物质组成元素相同。如下图所示,请回答下列问题:
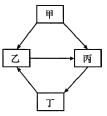
(1)写出甲物质的化学式:____________ 乙物质的化学式:__________________
(2)若丁为无色气体,则乙→丙的化学方程式是_______。丁→乙的化学方程式______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是测定空气中氧气含量的实验装置。下列说法正确的是( )
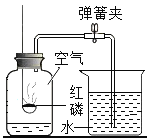
A. 此实验不是制取气体,所以实验前不用检查装置的气密性
B. 实验前没有将弹簧夹夹紧,会导致测定结果偏高
C. 该实验可以说明空气中含有稀有气体
D. 若把红磷换成木炭,也可得到相同实验结果
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请你根据自己所学化学知识回答下列问题:
(1)合成橡胶、棉花、聚乙烯塑料、蚕丝等都是人们生活和生产中常见的有机材料,其中属于天然有机高分子材料的是______。废旧塑料造成的污染被称为“______”。
(2)车用乙醇汽油是将乙醇和汽油以一定的比例混合而成的一种汽车燃料,乙醇完全燃烧的化学反应方程式为______。
(3)过量排放CO2会导致“______”。研究表明:CO2可用来合成多种有机物,在高温高压下,CO2和NH3可以合成尿素[CO(NH2)2],同时生成水,在该反应中CO2和NH3的质量比为______(填最简整数比)。人体排泄的尿液中也含有尿素,它通常是由______(填:“糖类”或“油脂”或“氨基酸”或“维生素”)氧化而成的。
(4)SO2、CO2、O3、NO2几种气体中会导致酸雨的是______,用pH试纸测定雨水酸碱度的具体操作是______。酸雨会造成土壤酸化,人们常用熟石灰来改良酸性土壤,其利用的原理是______;长期使用化肥K2SO4也会导致土壤酸化,用BaCl2溶液可以区分K2SO4和KCl两种钾肥,试写出其对应的化学方程式______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种高效、安全的消毒剂。
⑴ ClO2中氯元素的化合价是______。SO2和ClO2一样都属于氧化物,SO2中氧元素的质量分数为_______。
⑵ 在一定条件下,ClO2与氰化氢(HCN)反应的微观示意图如下:

“![]() ”表示的物质的化学式为____,反应生成的N2与CO2的质量比为____。
”表示的物质的化学式为____,反应生成的N2与CO2的质量比为____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一固体物质A,其可能是NH4Cl、NaCl、Na2CO3中的两种或多种。按如图所示进行探究实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应)。
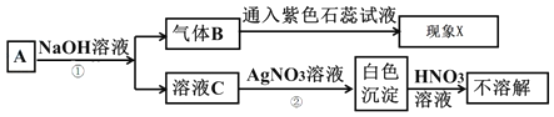
试根据实验过程中发生的现象作出判断,填写以下空白:
(1)气体B的化学式为_____。
(2)现象X为_____。
(3)固体物质A中不存在的物质是_____ (写化学式)。
(4)溶液C中含有的阴离子为_____(写离子符号)。
(5)请写出步骤②中生成白色沉淀的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学探究小组以“寻找过氧化氢分解新的催化剂”为课题,开展了下列实验。
(提出问题)氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
(猜想与假设)_____。
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
Ⅰ.分别量取5mL 5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入a g氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生较多气泡,带火星木条_____,B试管中无明显现象 | ①A试管产生的气体是_____(填化学式)氧化铁可加快过氧化氢的分解速率 |
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 | 氧化铁的_____在反应前后均没有发生变化。 |
Ⅲ.将实验II中的剩余物________(填操作名称),并将所得滤渣进行洗涤、干燥、称量 | 所得固体质量仍为a g | 氧化铁的_____在反应前后均没有发生变化。 |
(实验结论)
(1)实验II、III得出结论:_____。
(2)请写出氧化铁催化过氧化氢溶液分解的化学方程式_____。
(实验拓展)
(3)查阅资料得知,CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是_____。
A MnO2只能作过氧化氢溶液分解的催化剂
B 同一个化学反应可以有多种催化剂
C 催化剂只能加快化学反应的速率
D 用作催化剂的物质不可能是其他反应的反应物或生成物。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如图所示.则有关说法中不正确的( )

A.丁一定是化合物
B.乙可能是这个反应的催化剂
C.生成的甲、丙两物质的质量比为8: 1
D.参加反应的丁的质量一定等于生成甲和丙的质量之和
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们利用如图所示的装置,对质量守恒定律进行了谈究.实验结束后,老师另外提出了几个问题,请你一起参与思考。
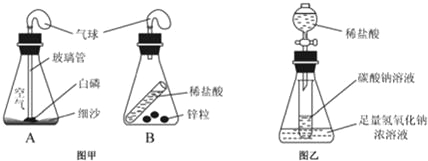
(1)图甲装置内物质充分反应后,冷却至室温,气球仍胀大的是 (选填“A”、“B”或“A和B”)。
(2)若图乙装置内Na2CO3溶液的质量为5克,滴入试管的稀盐酸质量也是5克,装置内物质充分反应后,发现NaOH浓溶液质量增加0.22克,试管中滴入紫色石蕊试液变红。根据上述已知条件,通过分析可以确定的是 (选填序号)。
①原稀盐酸的溶质质量分数 ②原Na2CO3溶液的溶质质量分数
③原NaOH溶液的溶质质量分数 ④反应后试管中NaCl的溶质质量分数
请你选择所填的其中一项,通过计算确定其溶质质量分数是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com