
【题目】酸、碱、盐在生产和生活中有着广泛的应用。
(1)氢氧化钠溶液和氢氧化钙溶液都能使酚酞溶液变红,其原因是二者的溶液中均含有相同的粒子________(填粒子符号)。
(2)钠与水反应,生成一种碱和密度最小的气体,该反应的化学方程式为___________。
(3)向一定量的稀盐酸和氯化镁的混合溶液中,逐滴加入10%的氢氧化钠溶液至过量,并测得溶液的pH随加入氢氧化钠溶液质量的变化曲线如图所示。
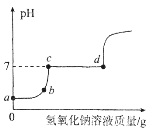
①b点溶液中含有哪些溶质__________________?(写化学式)
②写出c→d段反应的化学方程式__________________。
(4)某同学为了除去食盐水中的MgCl2、CaCl2、Na2SO4等杂质,设计了如图所示的实验方案。
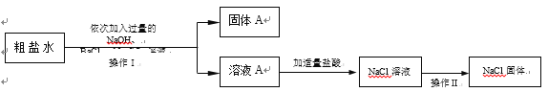
①操作II中玻璃棒的作用是___________?
②加入过量Na2CO3溶液的作用是____________________。
③写出该实验过程中发生的中和反应的化学方程式__________。
(5)为测定某石灰石样品中碳酸钙的质量分数,称取10 g石灰石(杂质不参加反应)放入烧杯中,加入100 g稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为106.7 g(气体的溶解忽略不计)。请计算该样品中碳酸钙的质量分数__________。
【答案】OH- 2Na+2H2O=2NaOH+H2↑ HCl、NaCl、MgCl2 2NaOH+MgCl2=2NaCl+Mg(OH)2↓ 搅拌,防止局部温度过高造成液滴飞溅 除去氯化钙和过量的氯化钡 HCl+NaOH=NaCl+H2O 75%
【解析】
(1)因氢氧化钠溶液和氢氧化钙溶液中都含有相同的氢氧根离子,则它们都能使无色的酚酞试液变红,故答案为:OH-.
(2)钠和水反应生成氢氧化钠和氢气,化学方程式为:2Na+2H2O=2NaOH+H2↑,故填:2Na+2H2O=2NaOH+H2↑。
(3)①向一定量的稀盐酸和氯化镁混合溶液中,逐滴加入氢氧化钠溶液至过量,盐酸会先与氢氧化钠反应生成氯化钠和水,然后氯化镁再与氢氧化钠反应生成氢氧化镁沉淀和氯化钠,b点溶液PH小于7,说明盐酸还有剩余,b点溶液中含有的盐酸、氯化钠和氯化镁;故填:HCl、NaCl、MgCl2。
②c→d段溶液的PH不变,原因是氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,化学方程式为:2NaOH+MgCl2=2NaCl+Mg(OH)2↓;故填:2NaOH+MgCl2=2NaCl+Mg(OH)2↓。
(4)①操作II是蒸发,玻璃棒的作用是搅拌,防止局部温度过高造成液滴飞溅;故填:搅拌,防止局部温度过高造成液滴飞溅;
②碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠,能和过量的氯化钡反应生成碳酸钡沉淀和氯化钠;故填:除去氯化钙和过量的氯化钡;
③写出该实验过程中发生的中和反应是盐酸和过量的氢氧化钠反应生成氯化钠和水,化学方程式为HCl+NaOH=NaCl+H2O。故填:HCl+NaOH=NaCl+H2O。
(5)生成二氧化碳的质量为:10g+100g-106.7g=3.3g
设生成3.3g二氧化碳需要碳酸钙的质量为y

y=7.5g
该样品中碳酸钙的质量分数为:![]() ×100%=75%
×100%=75%
答:该样品中碳酸钙的质量分数为75%。


科目:初中化学 来源: 题型:
【题目】请根据如图所示的实验过程和提供的数据计算。

(1)a、b的数值分别为_____、_____。
(2)合金中锌的质量分数为_____。
(3)第二次加入ag 14.6%的稀盐酸充分反应后所得溶液中溶质的质量分数。_____(写出计算过程,计算结果精确至0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~I是初中化学常见的物质,它们之间的相互关系如图所示(“→”指向生成物),其中B是铁锈的主要成分,A、C常温下是气体,H和I中含有一种相同元素,H不溶于稀硝酸。
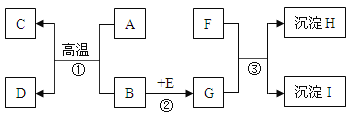
请回答下面问题:
(1)物质I的化学式是____;物质E的化学式是____。
(2)反应②的基本反应类型是_____。
(3)物质F属于____(填“酸”、“碱”、“盐”或“氧化物”)。
(4)反应③的化学方程式为____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】提倡“绿色旅行”,保护“生态环境”,请回答下列问题。
(1)源源一家去“天乐湖”露营,妈妈准备的食物中,富含蛋白质的是___(填字母序号)。
a  香蕉 b
香蕉 b ![]() 面包 c
面包 c![]() 鱼肉 d
鱼肉 d 牛奶
牛奶
(2)用轻便的锂电池电动自行车解决露营地附近的交通问题,该电动自行车骑行过程中,电池内发生化学反应时,将____能转化为电能。
(3)他们到达了露营目的地。
①大家共同搭建好帐篷。下列用品中,由有机合成材料做成是___(填字母序号)。
a尼龙篷布 b钢制撑杆 c羊毛毯子
②源源用便携式微型净水器(如图)去河中取水备用。净水器的滤芯由多种滤材组成,包括PP棉、颗粒活性炭、压缩活性炭棒等,其中活性炭在净水过程中主要起______作用。
![]()
(4)源源捡来了很多树枝,开始生火。
①引燃树枝时,需将树枝架空,其目的是_____。
②大家还准备了一些沙土,用于最后灭火,其灭火原理是____。
(5)他们开始烧烤食物,进行野餐。
①将鱼用铝箔包好进行烤制,在烤制过程中体现了铝箔具有良好的____性。
②烤鱼散发出诱人的香味,能闻到香味的原因是____。(填字母序号)
a分子在不断运动 b分子的质量很小
c分子之间有间隔 d分子的体积很小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲乙两种固体物质的溶解度曲线如图所示。20℃时,等质量的甲和乙的饱和溶液中,分别再加入等质量的甲、乙两种固体,升高温度至40℃,发现甲固体减少,乙固体增多。
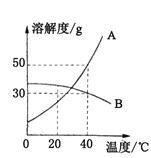
(1)甲物质的溶解度曲线为________(填“A”或“B”)。
(2)若甲中含有少量的乙,可用__________的方法得到较为纯净的甲。
(3)40℃时,60g甲的饱和溶液稀释为20%需加水_______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铝、铁、铜是我们生活中常见的金属.
(1)铝的利用比铜、铁晚是因为金属大规模开发和利用的先后顺序与有关(填字母)_________。
A 金属的活动性 B 金属的导电性 C 金属在底壳中的含量
(2)铝具有很好的抗腐蚀性能,原因是________________。
(3)每年全世界钢铁的产量很高,但钢铁的锈蚀给人类带来了的损失,铁在空气中锈蚀,实际上是铁跟_________和_______ 共同作用的结果;防止铁生锈的方法是______________(写一种);焊接铁制品时,通常先用稀盐酸除去其表面的铁锈,反应的化学方程式为_________。
(4)印发铜制电路板的“腐蚀性”为FeCl3溶液,反应化学方程式分别为①Cu+2 FeCl3=2 FeCl2+CuCl2;②Fe+2 FeCl3=3X.则②中X的化学式为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“○”“●”分别表示不同的原子,如图所示是某化学反应的微观模型,下列各项中对图示模型理解正确的是( )

A.该反应是分解反应B.参加反应分子个数比是2︰3
C.生成物是化合物D.反应中原子的种类发生了变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过海水提取的粗盐中含有 MgCl2、CaCl2、MgSO4.以及泥沙等杂质.以下是一种 制备精盐的实验方案(用于沉淀的试剂均过量).
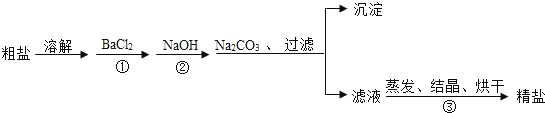
请回答下列问题:
(1)写出②中反应的化学方程式___________________________.
(2)加入 BaCl2、NaOH、Na2CO3 的顺序还可以改变吗?若能改变则写出改变的顺序,若不能改变,请说明理由_______________________________________.
(3)该实验方案还需完善,请写出具体的操作步骤___________________________________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】课外兴趣小组研究发现铜锈 [主要成分Cu2(OH)2CO3,学名:碱式碳酸铜]在加热后,除有二氧化碳和水生成外,在试管底部还有黑色粉末生成,他们对黑色粉末的成分进行了下列探究(不考虑杂质对实验的影响)。
(提出问题)黑色固体的成分是什么?
(提出猜想)①炭粉;②氧化铜;③______________。
(查阅资料)炭粉为黑色固体,不与稀酸反应,也不溶于稀酸。
(进行实验)(1)取少量黑色固体于坩埚中,用酒精灯加热,充分灼烧后,黑色固体无变化,猜想__不成立(填“①”、“②”或“③”,下同);
(2)用试管取少量黑色固体,滴加足量的_____________,振荡,充分反应后,观察到固体全部溶解,溶液显蓝色,猜想_____成立,发生反应的化学方程式是___________________________。
(拓展反思)孔雀石的主要成分与铜锈相同,结合上述实验探究结论,可以得出我国古代用孔雀石与木炭粉混合高温炼铜的反应原理是 __________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com